La desregulación del metabolismo celular es una característica fundamental de las células tumorales, permitiéndoles obtener la energía necesaria para una proliferación descontrolada e invasión de otros órganos, un proceso conocido como metástasis. La investigación en este campo busca comprender los mecanismos moleculares que impulsan estos cambios, con el objetivo de desarrollar nuevas estrategias terapéuticas contra el cáncer.
Alteraciones Metabólicas Fundamentales en el Cáncer
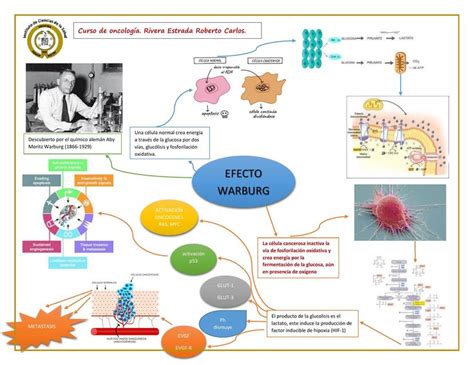
Desde hace casi un siglo, se sabe que las células cancerosas generan energía de manera diferente a las células normales. Mientras que las células sanas utilizan la respiración aerobia, un proceso complejo que requiere oxígeno, las células cancerosas emplean una estrategia metabólica menos eficiente y más primitiva: la fermentación, similar a la de levaduras o bacterias. Este fenómeno, conocido como el efecto Warburg, implica que las células malignas consumen entre 15 y 20 veces más glucosa para producir la misma cantidad de energía. Como consecuencia, el cáncer a menudo agota la glucosa disponible y debe recurrir a otras materias primas como grasas y aminoácidos.
El efecto Warburg no solo conduce a un mayor consumo de glucosa, sino que también genera altos niveles de radicales libres (especies reactivas de oxígeno - ROS) en las células malignas. Estos átomos inestables pueden dañar las células a través de la oxidación, contribuyendo al envejecimiento y al desarrollo de diversas enfermedades. Las células cancerosas han desarrollado mecanismos de defensa, como la producción de antioxidantes, para contrarrestar este daño.
El Papel de Oncogenes y Genes Supresores de Tumores
Tradicionalmente, se ha entendido que los oncogenes y los genes supresores de tumores regulan el ciclo celular. Sin embargo, investigaciones recientes sugieren que estos genes también desempeñan un papel crucial en la reprogramación metabólica de las células tumorales. Mutaciones en oncogenes como PI3K, AKT, mTORC y Myc pueden inducir un aumento en la expresión de isoenzimas de la vía glucolítica y reprimir la fosforilación oxidativa, promoviendo así un metabolismo anabólico que favorece el crecimiento tumoral. Estos cambios se asocian con un mayor consumo de glucosa y la liberación de lactato en el microambiente tumoral.
La activación de la vía de señalización PI3K/AKT, una de las alteraciones más comunes en cánceres humanos, incrementa la utilización de glucosa y activa la vía glucolítica. Esto se logra mediante el aumento de la expresión del transportador de glucosa y la activación de enzimas clave como la hexoquinasa. Adicionalmente, la señalización de AKT promueve el desvío de carbonos de la glucosa hacia vías biosintéticas, como la síntesis de ácidos grasos y colesterol.
Por otro lado, la pérdida de la función de genes supresores de tumores, como el p53, puede incrementar la síntesis anabólica a partir de intermediarios de la vía glucolítica, siendo crítico en el reprogramado metabólico de las células cancerosas. El tratamiento con metformina, un fármaco antidiabético que inhibe la cadena de transporte de electrones en la mitocondria, ha demostrado ser particularmente tóxico para células tumorales con deficiencia de p53.
Isoenzimas Clave en el Metabolismo Tumoral
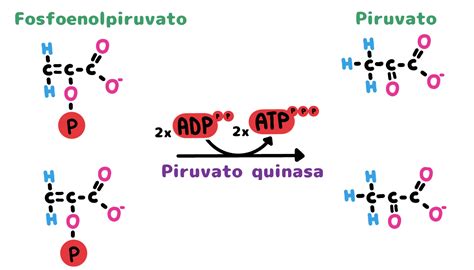
La expresión de isoformas de enzimas que sustentan el metabolismo anabólico es una consecuencia directa de la acción de oncogenes y genes supresores. Un ejemplo destacado es la isoforma M2 de la piruvato quinasa (PKM2). Esta enzima, que cataliza la conversión de fosfoenolpirúvico a piruvato, presenta una menor actividad en comparación con la isoforma M1, presente en células diferenciadas. La menor actividad de PKM2 provoca la acumulación de metabolitos intermedios en la vía glucolítica, que pueden ser desviados hacia otros procesos biosintéticos, satisfaciendo las necesidades anabólicas de las células tumorales.
Otro ejemplo es la sobreexpresión de la fosfofructoquinasa/2,6 bifosfatasa B3 (PFKFB3). Esta isoforma, con una alta actividad quinasa, promueve la acumulación de fructosa 2,6 bifosfato y, consecuentemente, de metabolitos intermedios en la vía glucolítica. Estos metabolitos pueden ser utilizados para la lipogénesis y la síntesis de purinas, ribosa, serina y glicina.
En ciertos tipos de tumores, como los hepatomas, se observa una duplicación de los genes que codifican para enzimas de la vía glucolítica, como la hexoquinasa II, lo que aumenta significativamente el consumo de glucosa. En el cáncer de próstata, se ha detectado un incremento en el número de copias de la enzima ácido graso sintasa. Más recientemente, se ha observado una elevación en la expresión de genes de la enzima fosfoglicerato deshidrogenasa en tumores de mama y melanomas, impulsando las vías de síntesis de serina y glicina.
Regulación Molecular de la Piruvato Quinasa en el Cáncer
Investigadores de la Universidad de Sevilla han participado en estudios que detallan la regulación molecular de la piruvato quinasa, una enzima esencial para el metabolismo de azúcares y estrechamente ligada a la proliferación y crecimiento celular. La acetilación, una modificación química reversible, actúa como un mecanismo de regulación celular. En células normales, estas marcas metabólicas permiten ajustar el metabolismo en respuesta al entorno. Sin embargo, en el cáncer, la pérdida de este control puede desviar el flujo metabólico y favorecer la proliferación celular descontrolada.
Los investigadores demostraron que la acetilación en posiciones específicas de la piruvato quinasa inhibe su función y disminuye su estabilidad. Se identificaron dos variantes principales: PKM1, asociada con tejidos adultos, y PKM2, vinculada tanto con tejidos adultos como embrionarios. Se descubrió que ciertas acetilaciones afectan de manera distinta a cada variante, revelando mecanismos de regulación específicos. Estos hallazgos son cruciales para comprender el comportamiento de la piruvato quinasa en el cáncer y cómo su pérdida de control promueve la proliferación celular.
El Entorno Tumoral y su Influencia en el Metabolismo y la Inmunidad
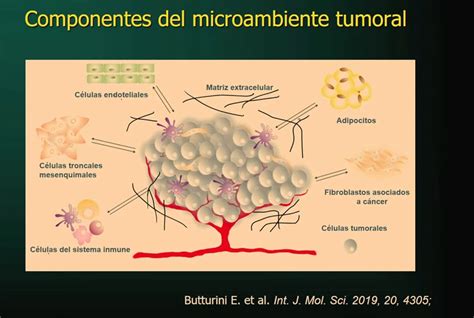
La desregulación del metabolismo en los tumores no solo afecta a las células cancerosas, sino que también modifica su entorno, conocido como microambiente tumoral. Este microambiente puede volverse deficiente en nutrientes, afectando la función de las células inmunitarias, como los linfocitos T citotóxicos, que son enviadas para combatir el tumor. La falta de nutrientes altera su funcionamiento y contribuye al agotamiento de los linfocitos T, incluso en presencia de puntos de control inmunitario como PD-1/PD-L1 y CTLA-4.
La falta de oxígeno (hipoxia) en los tumores también juega un papel importante. La hipoxia persistente puede llevar a la disfunción de los linfocitos T, provocando la producción de especies reactivas de oxígeno (ROS) en sus mitocondrias. Existe un vínculo claro entre las vías de señalización metabólicas e inmunitarias, y controlar la agresión metabólica podría mejorar la funcionalidad de los linfocitos T.
Los linfocitos T reguladores (Treg), que pueden suprimir las respuestas inmunitarias y proteger a los tumores, utilizan lactato, un subproducto del metabolismo de la glucosa en los tumores, para llevar a cabo su función. El lactato también puede reprogramar otras células inmunitarias, como los macrófagos, para que sean más favorables a los tumores. Esto sugiere que la programación metabólica, más que la identidad celular, es fundamental para la función de estas células. Si bien el consumo de lactato es un comportamiento normal en muchas células, en el cáncer resulta contraproducente.
Estrategias Terapéuticas Dirigidas al Metabolismo Tumoral
La comprensión de las alteraciones metabólicas en el cáncer abre la puerta al desarrollo de nuevas terapias dirigidas a explotar estas vulnerabilidades. El objetivo es encontrar medicamentos que actúen sobre el metabolismo de las células cancerosas para destruirlas, minimizando el daño a las células sanas.
Metformina y su Potencial en la Terapia contra el Cáncer
La metformina, un fármaco comúnmente utilizado para tratar la diabetes tipo 2, ha mostrado potencial en la terapia contra el cáncer. En estudios con ratones, la metformina generó un entorno más favorable para los linfocitos T dentro de los tumores, mejorando su respuesta a la inmunoterapia de puntos de control. Se están llevando a cabo ensayos clínicos para investigar este enfoque.
SM-88: Un Nuevo Fármaco Dirigido al Metabolismo Tumoral
El fármaco SM-88 representa un avance prometedor en el tratamiento del cáncer. Este medicamento utiliza una tirosina disfuncional para interferir en el proceso metabólico de las células cancerosas. Al intentar utilizar esta tirosina anómala para producir proteínas, las células cancerosas no lo logran, lo que provoca la descomposición de su capa protectora de mucina. Sin esta defensa, el tumor queda expuesto a los efectos destructivos de los radicales libres y del sistema inmunitario del paciente.
El SM-88 ha demostrado actividad antitumoral en 13 tipos de cáncer, incluyendo cáncer de páncreas metastásico, con perfiles de seguridad alentadores y sin efectos secundarios graves. Los resultados iniciales en pacientes con cáncer de páncreas metastásico han mostrado mejoras significativas en el estado de rendimiento y supervivencia general. Se están realizando ensayos clínicos de fase II para evaluar la eficacia y seguridad del SM-88 en pacientes con cáncer de páncreas metastásico.
Nuevas Herramientas para Visualizar la Actividad Metabólica Celular
Un equipo de científicos del Instituto de Micro y Nanotecnología del CSIC ha desarrollado un innovador método para suprimir el ruido en la microscopía holográfica digital. Esta técnica permite visualizar la actividad metabólica de las células con alta resolución espacial y sensibilidad en pocos minutos. El método es no invasivo y no requiere el uso de moléculas fluorescentes.
Este avance ha revelado que las células de cáncer de mama presentan regiones muy definidas donde se concentra la mayor parte de la actividad metabólica, alimentada por ATP. La capacidad de visualizar la actividad metabólica con alta resolución es crucial, ya que la desregulación metabólica es un factor clave en la progresión del cáncer y la metástasis. Las implicaciones clínicas de esta técnica son significativas, ya que puede mejorar la detección temprana, la evaluación de la progresión de la enfermedad y la personalización de tratamientos oncológicos.
18. “Introducción a la Microscopía Virtual”
Reprogramación Metabólica y su Impacto en la Supervivencia de Pacientes
La investigación sobre la correlación entre la expresión de enzimas metabólicas en el tejido tumoral y la supervivencia de pacientes con diversos tipos de cáncer ha ganado impulso. Los estudios sugieren que las enzimas del metabolismo mitocondrial ofrecen una diana terapéutica prometedora para el desarrollo de tratamientos personalizados en cáncer. Junto con datos genómicos y clínicos, estos hallazgos jugarán un papel importante en el diagnóstico, pronóstico y tratamiento de enfermedades, así como en la estratificación de pacientes.
El concepto de reprogramación metabólica es fundamental para comprender la carcinogénesis. Los cambios metabólicos observados en células tumorales no son meras consecuencias de la proliferación o la hipoxia, sino que son impulsados activamente por las alteraciones en oncogenes y genes supresores de tumores. El metabolismo proliferativo reprograma la mitocondria para que actúe como un organelo biosintético, esencial para la carcinogénesis.
El Papel de la AMPK en la Carcinogénesis
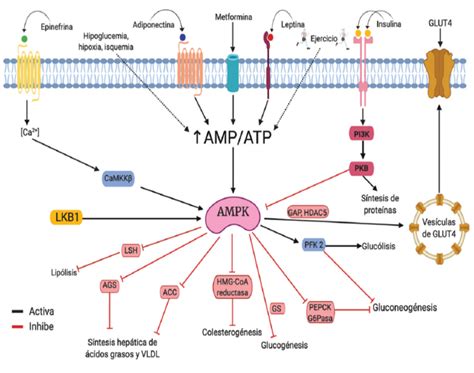
Una investigación liderada por la Universidad Rey Juan Carlos, con la colaboración de grupos de Francia y Reino Unido, explica por qué la proteína AMPK, encargada de controlar la energía y el metabolismo celular, puede pasar de ser un supresor del cáncer a un promotor del crecimiento tumoral. Este trabajo aclara cómo la AMPK se relaciona con su entorno para controlar la expresión de genes relacionados con el desarrollo de tumores.
La AMPK funciona como una "llave maestra" del metabolismo celular, siendo una diana importante para fármacos como la metformina. Sin embargo, los ensayos clínicos con metformina para el cáncer han arrojado resultados contradictorios. El estudio revela que la AMPK es inducida por la glucosa y promueve la proliferación de células tumorales mediante el control de la proteína acetiltransferasa EP300. La interacción entre AMPK y EP300 permite a esta última regular genes clave en la proliferación celular y el metabolismo tumoral.
La activación de la EP300 por la AMPK depende del contexto metabólico, variando según el tipo de cáncer y su estado evolutivo. En células de cáncer colorrectal, una alta disponibilidad de glucosa estimula sorprendentemente la AMPK, promoviendo la proliferación. Este fenómeno se produce a través de especies reactivas de oxígeno (ROS) generadas durante el metabolismo de la glucosa en células que no pueden almacenarla como glucógeno. La capacidad de almacenar glucógeno difiere entre células sanas y tumorales, determinando si la AMPK actúa como supresora o promotora del cáncer.
Análisis de Flujos Metabólicos y Biología de Sistemas
El estudio de la dinámica de los procesos metabólicos y los cambios que experimentan bajo diferentes estímulos ha dado lugar a la disciplina de la Biología de Sistemas. El uso de precursores metabólicos marcados con isótopos estables, como el carbono-13 (¹³C), permite rastrear los flujos metabólicos y determinar su importancia relativa en la síntesis de moléculas. El análisis de la distribución de isotopólogos (MIDA) utiliza fórmulas para calcular medidas relativas de flujos.
Para sistemas complejos, se emplean herramientas matemáticas avanzadas y modelos metabólicos a escala genómica (GSMMs). Estos modelos integran información genómica, transcriptómica, metabolómica y flujómica para predecir las dependencias metabólicas de los sistemas en estudio. La aplicación de estas herramientas computacionales y experimentales es esencial para descubrir nuevos biomarcadores y vulnerabilidades metabólicas específicas de las células tumorales, con el fin de desarrollar métodos diagnósticos y terapias innovadoras contra el cáncer.
tags: #activacion #metabolica #de #carcinogenesis #indol