La anemia es una afección médica común caracterizada por una deficiencia en la cantidad de glóbulos rojos en la sangre o en su capacidad para transportar oxígeno. Los síntomas más frecuentes de la anemia incluyen fatiga y debilidad, palidez observable en encías, uñas y párpados inferiores, así como disnea (dificultad para respirar) y taquicardia (ritmo cardíaco acelerado).
Las causas de la anemia son variadas y dependen del tipo específico de la afección. Entre las más comunes se encuentran la deficiencia de hierro, que es la causa principal en muchos casos, y la deficiencia de vitamina B12, esencial para la formación de glóbulos rojos. El tratamiento de la anemia se diseña en función de su causa subyacente. Una medida preventiva clave es el consumo de una dieta rica en hierro y otros nutrientes esenciales.
Anemia de las Enfermedades Crónicas y Obesidad
Los desórdenes inflamatorios crónicos, frecuentemente asociados con patologías infecciosas y enfermedades inflamatorias, a menudo se manifiestan con hipoferremia o anemia. Esta condición se conoce como anemia de las enfermedades crónicas (AEC). En la actualidad, la obesidad destaca por su alta prevalencia y distribución poblacional, y se asocia con un aumento de la mortalidad general y un mayor riesgo de comorbilidades, incluida la AEC.
Se ha observado que la obesidad se correlaciona con bajas concentraciones de hierro sérico y un incremento en la expresión de hepcidina (Hpc) en el tejido adiposo. La elevada producción de hepcidina en individuos obesos se postula como un factor contribuyente a la hipoferremia y la anemia. La relación inversa entre los niveles de hierro y la adiposidad fue reportada inicialmente por Wenzel y colaboradores, quienes encontraron concentraciones significativamente menores de hierro sérico en adolescentes obesos en comparación con sus pares no obesos. Más recientemente, la masa grasa ha sido identificada como un predictor negativo del hierro sérico.
La etiología de la AEC asociada a la obesidad es multifactorial y aún incierta. Incluye factores como una ingesta inadecuada de hierro en la dieta y mayores requerimientos de hierro en sujetos obesos debido a un mayor volumen sanguíneo. Actualmente, la hepcidina se considera un regulador clave en los desórdenes del metabolismo del hierro observados en la patogénesis de la AEC. Su acción se manifiesta en el deterioro de la absorción intestinal de hierro, la restricción de la liberación de hierro de los depósitos corporales y la inadecuada biodisponibilidad de hierro debido a la inflamación.
La Hepcidina: Regulación y Función
La hormona hepcidina es un pequeño polipéptido catiónico, rico en cisteínas, compuesto por 25 aminoácidos y 4 puentes disulfuro. Pertenece a la familia de las defensinas, conocidas por su actividad antibacteriana y antifúngica. Descubierta en 2001, la hepcidina es el principal regulador de la absorción de hierro y su distribución en los tejidos. Un aumento patológico de sus niveles puede causar o contribuir al desarrollo de la AEC.
La expresión del gen que codifica la hepcidina se restringe casi por completo al hígado, aunque también se ha detectado en el tejido adiposo. Considerada la "hormona del hierro", la hepcidina es sintetizada inicialmente como un precursor más grande, la preprohepcidina (84 aminoácidos), a partir de un gen localizado en el cromosoma 19 humano. En los hepatocitos, la preprohepcidina es procesada a pro-hepcidina, y previo a su secreción, la prohormona convertasa media el procesamiento postraduccional para generar el compuesto bioactivo maduro.
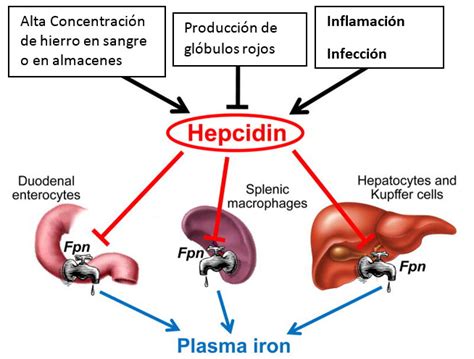
La expresión de hepcidina es inducida por las reservas de hierro y la inflamación, mientras que es suprimida por la hipoxia y la anemia. Se ha demostrado que el hierro modula la expresión de hepcidina a través de vías de señalización intracelular paralelas, como MAPK/Erk y BMP/SMAD. Se postula que BMP, SMAD y hemojuvelina (HJV) comparten una vía de regulación común para la expresión de hepcidina, ya que la región de respuesta a estos tres estímulos es idéntica. La HJV juega un papel crucial en el mantenimiento de niveles adecuados de expresión de hepcidina, mejorando la vía de señalización intracelular BMP/SMAD mediante el aumento de la sensibilidad celular a bajos niveles de BMP, actuando como cofactor en la activación de receptores de BMPs.
Por otro lado, las citoquinas proinflamatorias desempeñan un rol primordial en la inducción del gen de la hepcidina durante la inflamación, provocando un rápido aumento de la hepcidina urinaria y una disminución concomitante de los niveles de hierro sérico, lo que la clasifica como una proteína de fase aguda tipo II. La interleuquina-6 (IL-6), con su potencial actividad proinflamatoria, es un fuerte estímulo para la producción de hepcidina a través de la activación de la vía de señalización intracelular JAK/STAT. La IL-6 interviene en la inducción de la síntesis de hepcidina al aumentar la unión del factor de transcripción STAT3 al promotor de la hepcidina, lo que sugiere su papel clave en el incremento de la expresión de hepcidina en respuesta a la inflamación.
Interacción Hepcidina-Ferroportina
La actividad de la hepcidina comienza con su unión a la cara extracelular de su receptor y único exportador celular de hierro conocido: la ferroportina (Fpn). La Fpn es una proteína transmembrana presente en tejidos con alto transporte de hierro: enterocitos duodenales (absorción de hierro dietético), macrófagos del hígado, bazo y médula ósea (reciclaje de hierro de eritrocitos senescentes), hepatocitos (almacenamiento y liberación de hierro) y trofoblasto placentario (transporte de hierro materno al feto).
La unión de la hepcidina a la Fpn en las membranas de las células exportadoras de hierro induce la internalización del complejo receptor-ligando, seguida de ubiquitinización del péptido y degradación en el lisosoma. La pérdida de Fpn resulta en retención de hierro en los macrófagos, disminución de la absorción de hierro dietético en los enterocitos y, consecuentemente, una reducción del flujo de hierro hacia el plasma. Por lo tanto, la hepcidina actúa como un regulador negativo de la absorción de hierro, ajustándola a las necesidades corporales del mineral.
Se ha demostrado que la síntesis de hepcidina se correlaciona inversamente con la expresión de Fpn duodenal, afectando la absorción de hierro. El sistema hepcidina-ferroportina se considera un objetivo terapéutico en anemias y desórdenes por sobrecarga de hierro.
Obesidad y su Impacto en la Hepcidina
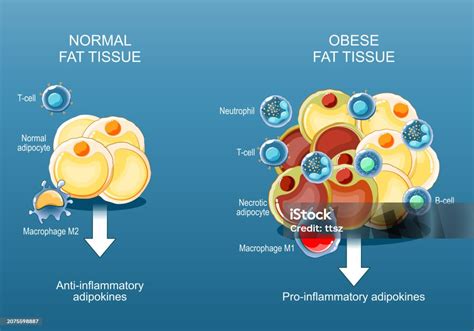
Aunque la hepcidina se produce principalmente en el hígado, se ha reportado una mayor expresión en el tejido adiposo de personas obesas. Esto sugiere una asociación más fuerte entre el hierro plasmático y la adiposidad en niños, adolescentes, adultos y mujeres posmenopáusicas. El tejido adiposo es un órgano endocrino activo, secretor de numerosas hormonas y citoquinas proinflamatorias que contribuyen a la inflamación asociada a la obesidad.
En pacientes obesos, la infiltración de macrófagos en el tejido adiposo induce la producción de adipoquinas como el factor de necrosis tumoral-α (TNF-α), IL-1β, IL-6, IL-8 e IL-10. Estos factores parecen explicar el rol de la hepcidina como mediador entre la inflamación de la obesidad y la AEC.
Adicionalmente, el tejido adiposo, especialmente el visceral, puede causar hipoxia adipocitaria. Esto resulta en inflamación crónica debido a diferencias en la tensión de oxígeno, lo que a su vez puede aumentar la expresión de hepcidina y contribuir a la asociación entre obesidad y bajos niveles de hierro. El tejido adiposo también puede influir en la homeostasis del hierro en pacientes obesos mediante la regulación de la vía de señalización BMP/HJV, ya que se ha descrito la expresión de HJV en este tejido.
La relación entre obesidad e inflamación se sustenta en la presencia de niveles elevados de proteínas de fase aguda en el plasma de personas obesas, como la ferritina sérica y la proteína C reactiva. La síntesis de ferritina está regulada por IL-6, TNF-α, insulina, factor de crecimiento insulínico (IGF-1) y hormonas tiroideas. Por lo tanto, la obesidad se asocia con un aumento de las reservas de hierro, implicando una acumulación excesiva en los tejidos, especialmente en el hígado, lo que promueve la generación de especies reactivas de oxígeno y daño tisular.
Se ha propuesto un síndrome de sobrecarga de hierro en pacientes con ferritina sérica elevada y saturación de transferrina normal. La mayoría de estos pacientes presentan sobrepeso, hiperlipidemia, hipertensión arterial o metabolismo anormal de la glucosa. Los niveles de ferritina sérica se correlacionan positivamente con la glucosa e insulina en ayunas y negativamente con la sensibilidad a la insulina. Existe evidencia de que la hiperferritinemia en la obesidad debe interpretarse en el contexto del síndrome de resistencia a la insulina (RI).
La inflamación crónica de bajo grado, característica de la obesidad, puede contribuir al desarrollo de RI, intolerancia a la glucosa y diabetes mellitus tipo 2 (DM2). La insulina estimula rápidamente la absorción de hierro en adipocitos y hepatocitos, y el hierro interfiere con la acción de la insulina en el hígado, contribuyendo a la RI. Además, la insulina podría activar el factor inducible por hipoxia 1α (HIF-1α), potenciando los efectos inflamatorios del tejido adiposo.
La acumulación de tejido adiposo intra-abdominal contribuye al desarrollo del síndrome metabólico, ya que el exceso de grasa abdominal está implicado en la fisiopatología de la RI. La circunferencia de cintura, un indicador de grasa abdominal, es uno de los criterios diagnósticos del síndrome metabólico. Existe una asociación positiva entre el síndrome metabólico y niveles elevados de ferritina sérica.
Entre las adipoquinas secretadas por el tejido adiposo, la leptina y la adiponectina tienen gran importancia metabólica. La leptina, una adipoquina proinflamatoria, puede actuar a través de un mecanismo de señalización intracelular similar a la IL-6. Estudios in vitro sugieren que la leptina regula la expresión hepática de hepcidina, lo que indica que su aumento en sangre podría contribuir a desórdenes del metabolismo del hierro. En niños obesos, se ha observado que el aumento de la producción de hepcidina está mediado por la leptina.
Por otro lado, la adiponectina es una adipoquina antiinflamatoria con efectos metabólicos opuestos a la leptina. Estudios recientes en ratones han demostrado que el tejido adiposo de ratones ob/ob (con mutación en el gen de la leptina) es más hipóxico que el de ratones delgados. Se observó una asociación entre hipoxia e incremento en la expresión de genes inflamatorios y disminución de la expresión de adiponectina en el tejido adiposo.
Hepcidina y Anemia de las Enfermedades Crónicas
La AEC, también conocida como "anemia de la inflamación", es la segunda causa más frecuente de anemia después de la anemia por deficiencia de hierro (ADF). En pacientes hospitalizados, es la anemia de mayor prevalencia. Clásicamente descrita como normocítica y normocrómica, puede volverse microcítica e hipocrómica a medida que la enfermedad progresa. Bioquímicamente, se caracteriza por bajo hierro plasmático, disminución de la capacidad total de unión del hierro, baja saturación de transferrina (Tf), disminución de sideroblastos, aumento del hierro en el sistema reticuloendotelial y valores normales de receptor de transferrina sérico (RTf).
En la práctica clínica, diferenciar la AEC de la ADF es crucial y a menudo difícil, ya que ambas cursan con disminución del hierro sérico y la saturación de Tf. Además, la inflamación dificulta la interpretación de los niveles de ferritina, cuya expresión es inducida tanto por la sobrecarga de hierro como por las citoquinas inflamatorias.
La medición de los niveles circulantes de hepcidina en plasma es de gran ayuda para el diagnóstico, aunque su disponibilidad aún es limitada. La espectroscopia de masas y el método ELISA se consideran técnicas prometedoras para la determinación de hepcidina, lo que podría facilitar la selección de terapias apropiadas.
Se ha propuesto que la relación RTf / logaritmo de ferritina sérica podría ser útil para evaluar el estado nutricional de hierro en sujetos con inflamación crónica. Una relación < 1 indicaría AEC, mientras que una relación > 2 sugeriría depósitos insuficientes de hierro, independientemente de la presencia de AEC.
El RTf es la vía convencional por la cual las células adquieren hierro. En condiciones de deficiencia de hierro, hay una mayor concentración de RTf en la superficie celular como mecanismo para captar el hierro necesario. Su medición se considera el índice óptimo para definir la deficiencia de hierro tisular. Por otro lado, la ferritina sérica sigue siendo el mejor indicador de las reservas corporales de hierro.
La primera evidencia directa que respalda la función de la hepcidina en la AEC proviene de pacientes con glucogenosis tipo Ia (GSDla). Esta enfermedad autosómica recesiva, causada por mutaciones en el gen de la glucosa-6-fosfatasa, resulta en una incapacidad para mantener la homeostasis de la glucosa. Pacientes adultos con GSDla desarrollaron grandes adenomas hepáticos y anemia con características similares a la AEC. Se han asociado niveles elevados de hepcidina con el desarrollo de AEC, una patología caracterizada por una disminución en la movilización y biodisponibilidad del hierro, lo que conduce a hipoferremia y un aumento de las reservas de hierro celular.
Relación entre Obesidad y Anemia por Deficiencia de Hierro
La obesidad y la deficiencia de hierro son problemas de salud globales que afectan a miles de millones de personas. Mientras que el sobrepeso y la obesidad son factores de riesgo clave para numerosas enfermedades crónicas, los niveles bajos de hierro en sangre constituyen la deficiencia de micronutrientes más prevalente a nivel mundial. La obesidad y la anemia pueden coexistir, siendo una combinación frecuente donde el exceso de grasa corporal promueve inflamación crónica, especialmente si la grasa se acumula en la zona abdominal. Esta inflamación eleva la hepcidina, una hormona que inhibe la absorción de hierro, provocando deficiencia incluso si el consumo es adecuado.
Un estudio observacional en 619 mujeres de 20 a 49 años reveló que la deficiencia de hierro afectó al 24% de las mujeres con peso normal, al 42% con sobrepeso y al 46% con obesidad. Una pérdida de peso inicial significativa (mínimo 5-10%) mejora la absorción y los niveles de hierro al reducir la inflamación y los niveles de hepcidina. De manera similar, la pérdida de grasa corporal seis meses después de una cirugía bariátrica reduce significativamente la inflamación (interleuquina-6) y los niveles de hepcidina, aumentando la absorción de hierro en un 28% en sujetos con deficiencia.
La obesidad genera una inflamación crónica de bajo grado que disminuye la absorción de hierro. Por lo tanto, si el paciente se suplementa inicialmente con hierro, este, al no absorberse adecuadamente, puede servir como nutriente para las bacterias del colon, alterando la microbiota intestinal.
Producción y Función de los Glóbulos Rojos
La mayor parte de la producción de glóbulos rojos ocurre en la médula ósea, el tejido blando en el centro de los huesos encargado de la formación de células sanguíneas. Los glóbulos rojos sanos tienen una vida útil de 90 a 120 días, tras lo cual las células viejas son eliminadas. Una hormona producida en los riñones, la eritropoyetina (EPO), señala a la médula ósea para que produzca más glóbulos rojos.
La hemoglobina es la proteína dentro de los glóbulos rojos que transporta oxígeno y les confiere su color característico. Las personas con anemia tienen niveles insuficientes de hemoglobina.
El cuerpo requiere ciertas vitaminas, minerales y nutrientes para producir glóbulos rojos suficientes. El hierro, la vitamina B12 y el ácido fólico son tres de los más importantes. La deficiencia de estos nutrientes puede deberse a cambios en el revestimiento del estómago o los intestinos que afectan la absorción de nutrientes (ej. celiaquía), una dieta deficiente o cirugías que extirpan parte del estómago o los intestinos.
Causas Posibles de Anemia
Las posibles causas de anemia incluyen:
- Deficiencia de hierro
- Deficiencia de vitamina B12
- Deficiencia de folato
- Ciertos medicamentos
- Destrucción prematura de glóbulos rojos (a veces por problemas del sistema inmunitario)
- Algunas formas hereditarias, como la talasemia o la anemia falciforme
- Embarazo
- Problemas de la médula ósea (linfoma, leucemia, mielodisplasia, mieloma múltiple, anemia aplásica)
- Pérdida lenta de sangre (menstruaciones abundantes, úlceras estomacales)
- Pérdida súbita de gran cantidad de sangre
Síntomas y Diagnóstico de la Anemia
Si la anemia es leve o se desarrolla lentamente, es posible que no presente síntomas evidentes. Sin embargo, algunos síntomas comunes pueden incluir:
- Fatiga y debilidad
- Palidez
- Dificultad para respirar (disnea)
- Ritmo cardíaco acelerado (taquicardia)
- Mareos
- Dolor de cabeza
- Frío en manos y pies
- Lengua adolorida o inflamada
- Úlceras bucales
- Sangrado menstrual anormal o más abundante
El proveedor de atención médica realizará un examen físico, que puede revelar:
- Soplo cardíaco
- Presión arterial baja (especialmente al ponerse de pie)
- Fiebre leve
- Piel pálida
- Frecuencia cardíaca rápida
Algunos tipos de anemia pueden manifestarse con otros hallazgos en el examen físico.
Los exámenes de sangre para diagnosticar tipos comunes de anemia pueden incluir:
- Niveles sanguíneos de hierro, vitamina B12, ácido fólico y otras vitaminas y minerales.
- Conteo sanguíneo completo (CSC).
- Conteo de reticulocitos.
Se pueden realizar pruebas adicionales para identificar problemas de salud subyacentes que causan la anemia.
Tratamiento de la Anemia
El tratamiento de la anemia debe dirigirse a su causa específica y puede incluir:
- Transfusiones de sangre.
- Corticosteroides u otros medicamentos inmunosupresores.
- Eritropoyetina, un medicamento que estimula la médula ósea a producir más células sanguíneas.
- Suplementos de hierro, vitamina B12, ácido fólico u otras vitaminas y minerales.
La anemia severa puede llevar a niveles bajos de oxígeno en órganos vitales, como el corazón, y puede resultar en insuficiencia cardíaca. Se recomienda consultar a un profesional de la salud si se presentan síntomas de anemia o sangrado inusual.