El monóxido de carbono (CO) es un gas venenoso, incoloro e inodoro, resultante de una combustión incompleta. Su formación está intrínsecamente ligada a la eficiencia del proceso de combustión y al tipo de combustible utilizado. Una combustión correcta producirá un porcentaje muy bajo de CO en los productos de la combustión.
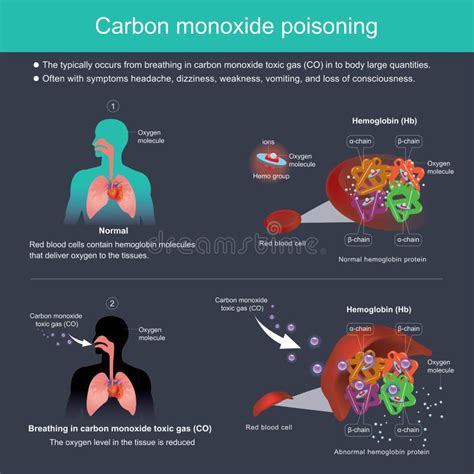
Este gas ingresa al organismo a través de los pulmones y, desde allí, pasa a la sangre, ocupando el lugar del oxígeno. Como consecuencia, reduce la capacidad de la sangre para transportar oxígeno y dificulta la utilización del mismo por parte de las células. La concentración de CO en el aire puede ser extremadamente peligrosa; por ejemplo, una concentración de 700 ppm de CO en una habitación puede ser mortal para una persona que la respire durante tres horas.
La unión del monóxido de carbono a la molécula de hemoglobina en la sangre es más fuerte que la del oxígeno, lo que impide la oxigenación adecuada de órganos y tejidos. Esta unión forma carboxihemoglobina, una molécula tóxica que puede derivar en asfixia, daños cerebrales, neurológicos, cardíacos e incluso la muerte. Los síntomas de intoxicación por CO pueden ser confundidos con gripes, intoxicaciones alimentarias o accidentes cerebrovasculares, lo que subraya la importancia de la rápida evacuación de la víctima a un centro asistencial, incluso si ha recuperado el conocimiento.
Fuentes y Formación del Monóxido de Carbono
El monóxido de carbono se origina principalmente por la combustión incompleta (por falta de oxígeno) de combustibles que contienen carbono, como la gasolina, el gas, el carbón, el aceite y la madera. Los vehículos con el motor encendido, las chimeneas, las calderas, los calentadores de agua o calefactores, y aparatos domésticos que queman combustible como estufas u hornillas de cocina, pueden producirlo si no funcionan correctamente.
Grandes cantidades de CO se forman como subproducto durante procesos oxidativos en la producción de productos químicos, lo que hace necesaria la purificación de los gases residuales. El incremento de todo tipo de combustión es un agente contaminante del ambiente, generando concentraciones de polución cada vez mayores. La formación de humos, la lluvia ácida y el aumento de alergias son consecuencias directas de este desarrollo.
Los incendios forestales también son una fuente significativa de emisión de monóxido de carbono, liberado junto a partículas finas PM2.5. Además, el CO contribuye indirectamente a intensificar estos incendios al acumularse en el aire.
Combustión Completa vs. Incompleta
Es crucial distinguir entre la combustión completa y la incompleta:
- Combustión Completa: Ocurre cuando un hidrocarburo reacciona con oxígeno en presencia de suficiente oxígeno, produciendo dióxido de carbono (CO2) y agua (H2O). Este proceso suele requerir una llama.
- Combustión Incompleta: Se produce por la falta de oxígeno y genera monóxido de carbono (CO). No se produce naturalmente en la atmósfera y sus niveles peligrosos pueden acumularse en hogares y oficinas a partir de cualquier dispositivo que queme combustible.
El dióxido de carbono (CO2), por otro lado, se forma durante la combustión completa de materiales que contienen carbono. Si bien en concentraciones normales (alrededor del 0.04% en el aire) no es tóxico, es el principal gas de efecto invernadero responsable del calentamiento global. Las plantas convierten el CO2 en oxígeno (O2) bajo la influencia de la luz solar y la clorofila, mientras que la respiración humana y animal lo revierte, creando un equilibrio que los productos gaseosos de la combustión distorsionan, acelerando el efecto invernadero.
🔥 Diferencias entre Combustión completa e incompleta | Diferencias, características [Fácil y Rápido]
Impacto y Peligros del Monóxido de Carbono
El monóxido de carbono es un gas extremadamente peligroso, a menudo denominado "asesino silencioso" debido a su naturaleza incolora, inodora e insípida, que dificulta su detección temprana. Los Centros para el Control y la Prevención de Enfermedades estiman que miles de personas son hospitalizadas anualmente por intoxicación por CO, y cientos mueren a causa de él.
La capacidad del CO para unirse a la hemoglobina reduce la función de esta para oxigenar adecuadamente el cuerpo, lo que puede llevar a asfixia y daños permanentes. En caso de percibir síntomas de intoxicación, es vital abandonar el lugar y avisar a los servicios de emergencia.
El monóxido de carbono también afecta a la biodiversidad, los hábitats y los ecosistemas de manera indirecta, alterando la composición atmosférica. Aunque no atrapa calor directamente, sus efectos amplificadores aceleran el calentamiento global. Disminuye los radicales hidroxilo (OH) en el aire, moléculas clave para descomponer contaminantes de efecto invernadero como el metano. Además, contribuye a la formación de partículas finas (PM2.5) y es precursor del ozono troposférico al reaccionar con otros contaminantes como los óxidos de nitrógeno (NOx) y los compuestos orgánicos volátiles (COV).

Medidas de Prevención y Control
La correcta evacuación de gases al exterior es fundamental para evitar la acumulación de gases tóxicos en el interior de las viviendas. Si se encienden brasas o llamas de cualquier tipo, no se debe dormir con estas encendidas.
Para reducir las emisiones de CO a la atmósfera, los vehículos que utilizan combustibles fósiles disponen de catalizadores de tres vías que convierten el CO en dióxido de carbono antes de su liberación. La monitorización de la calidad del aire es esencial para garantizar la seguridad pública, prevenir problemas de salud y proteger el medio ambiente.
Dado que el CO es un gas invisible, la instalación y el funcionamiento continuo de sistemas de monitorización de la calidad del aire son cruciales para su detección temprana. Esto permite controlar los niveles peligrosos de CO antes de que se produzcan daños. Las ciudades pueden utilizar estos datos para cumplir normativas, planificar políticas de movilidad y favorecer energías más limpias.
Normativas y Tecnologías de Detección
Muchos gobiernos y organizaciones internacionales han implementado normativas estrictas para controlar las emisiones y la exposición al CO. Los estándares de calidad del aire garantizan la vigilancia para mantener niveles seguros para la salud humana. La Administración de Seguridad y Salud Ocupacional (OSHA) en EE. UU. establece un límite permisible de exposición (PEL) de 50 ppm para el CO en promedio durante ocho horas.
Sensores especializados, como los de Kunak, calculan la concentración de CO sin necesidad de datos externos, asegurando la precisión de las mediciones. Una red interconectada permite analizar datos en plataformas digitales, facilitando la toma de decisiones ágiles y alertas ante la superación de umbrales preestablecidos. La precisión y fiabilidad de estos sensores son vitales para diversas necesidades de medición y control en instalaciones industriales, entornos naturales y ciudades.
La monitorización del monóxido de carbono es vital en entornos como la Zona de Bajas Emisiones de Bilbao para detectar el riesgo invisible y proteger la salud humana, controlar fuentes contaminantes y cumplir normativas ambientales.

Historia y Evolución del Conocimiento sobre el CO
La relación de la humanidad con el monóxido de carbono se remonta al control del fuego hace aproximadamente 800,000 años. Los primeros humanos probablemente descubrieron su toxicidad al introducir el fuego en sus viviendas. El desarrollo de la metalurgia y la fundición también expuso a la humanidad al CO.
Filósofos y médicos antiguos como Aristóteles y Galeno ya registraron la toxicidad de los humos del carbón. Investigaciones científicas modernas sobre el envenenamiento por CO comenzaron en el siglo XVIII con figuras como Georg Ernst Stahl, Friedrich Hoffmann, Joseph Priestley y Carl Wilhelm Scheele, quienes sintetizaron y aislaron el gas, aunque inicialmente con interpretaciones erróneas sobre su naturaleza.
Antoine Lavoisier y otros químicos realizaron experimentos que, aunque no concluyentes, contribuyeron al entendimiento del CO. A finales del siglo XVIII y principios del XIX, se reconoció la afinidad del CO por la sangre y su papel en la toxicidad de los humos. Claude Bernard, en el siglo XIX, describió el mecanismo del envenenamiento por monóxido de carbono, explicando cómo impide la conversión de la sangre arterial en venosa.
En el siglo XX, el CO se reconoció como un reactivo industrial valioso. Procesos como Fischer-Tropsch, hidroformilación y la producción de ácido acético a partir de metanol demostraron su utilidad en la industria química y de combustibles.

Monóxido de Carbono en la Industria y la Vida Cotidiana
La producción de monóxido de carbono es inherente a muchos procesos industriales. En la producción de productos químicos, se genera CO como subproducto y se requiere su purificación. En la industria de fertilizantes, como en la planta de LIFECO en Libia, se implementan sistemas de monitoreo ambiental para preservar la salud de trabajadores y comunidades.
En el ámbito doméstico, es crucial asegurar el correcto funcionamiento y mantenimiento de aparatos que queman combustible. La instalación de detectores de monóxido de carbono es una medida de seguridad esencial para prevenir intoxicaciones.
El tratamiento para la intoxicación por monóxido de carbono se basa en alejar a la persona de la fuente de exposición y administrar oxígeno, que actúa como antagonista específico del CO. En casos graves, cuando hasta el 75% de la hemoglobina está unida a monóxido de carbono, la única forma de sobrevivir es respirando oxígeno puro.