El calor latente es la energía que una sustancia absorbe o libera durante un cambio de fase, sin que su temperatura varíe. Este fenómeno, cuyo nombre proviene del latín latens (oculto), se refiere a la energía que no se manifiesta como un aumento o disminución de la temperatura, sino que se invierte en modificar el estado de la materia. La idea surgió en una época en la que se creía que el calor era una sustancia fluida llamada calórico.
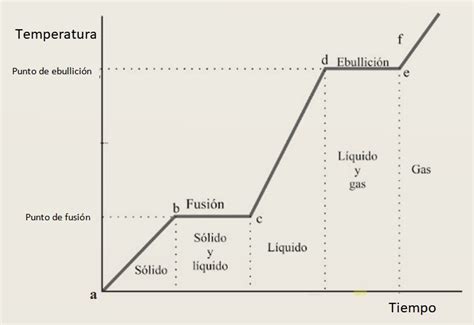
Cuando se suministra calor a una sustancia, normalmente su temperatura aumenta. Sin embargo, durante un cambio de fase, la energía absorbida o cedida se utiliza para romper o formar enlaces entre las moléculas, alterando su estado de agregación. Por ejemplo, al calentar hielo, su temperatura aumenta hasta alcanzar el punto de fusión (0 °C). A partir de este punto, aunque se siga añadiendo calor, la energía se emplea en transformar el hielo en agua líquida, manteniendo la temperatura constante hasta que todo el sólido se haya fundido.
Es fundamental especificar la temperatura a la que ocurre un cambio de fase al hablar de calor latente, ya que, aunque en menor medida, la evaporación o fusión pueden suceder a otras temperaturas. Por ejemplo, el agua posee un calor de vaporización y un calor de fusión elevados. El alto calor de vaporización del agua es una ventaja para la regulación de la temperatura corporal en organismos vivos; la evaporación del sudor, por ejemplo, absorbe calor del cuerpo, reduciendo su temperatura superficial.
La relación entre el calor suministrado (Q), la masa de la sustancia (m) y el calor latente (L) se expresa mediante la fórmula: Q = m * L. El valor de L depende del tipo de cambio de fase. Por ejemplo, para que el agua cambie de sólido a líquido a 0 °C, se requieren 334,000 J/kg (o 334 kJ/kg) de energía, lo que se conoce como calor latente de fusión del agua.
Comprendiendo los Estados de la Materia y los Cambios de Fase
En un sólido, los átomos y moléculas ocupan posiciones fijas en una red cristalina, vibrando alrededor de sus posiciones de equilibrio. A medida que la temperatura aumenta, estas vibraciones se vuelven más amplias. Cuando las vibraciones son lo suficientemente fuertes como para vencer las fuerzas de atracción intermoleculares, el sólido comienza a fundirse y se convierte en líquido.
En estado líquido, las moléculas aún están relativamente cerca, pero tienen mayor libertad de movimiento. Al seguir aumentando la temperatura y suministrar más calor, las fuerzas de atracción que mantienen unidas a las moléculas en el líquido se vencen. Las moléculas se separan, se mueven libremente y ocupan todo el recipiente que las contiene, pasando al estado de vapor o gas. Durante este proceso de cambio de estado, la temperatura permanece constante a pesar de la adición de calor.
El calor latente de evaporación del agua es significativamente mayor que el calor sensible necesario para elevar su temperatura de 0 °C a 100 °C. Esta propiedad es útil en diversas aplicaciones, como la refrigeración.
Calor Latente de Fusión y Entalpía de Fusión
El calor de fusión, también conocido como entalpía de fusión o calor latente de fusión, es la cantidad de energía necesaria para derretir o congelar una sustancia a presión constante. En química, el término "fusión" es sinónimo de "derretimiento".
Por ejemplo, el agua tiene un calor de fusión de 334 J/g a su punto de fusión de 0 °C. Esto implica que, a esta temperatura, un gramo de agua líquida debe liberar 334 julios de energía para congelarse completamente y convertirse en hielo. Si se conoce la masa molar de una sustancia, se puede calcular el calor molar de fusión. Para el agua (masa molar de 18.02 g/mol), el calor molar de fusión es aproximadamente 6020 J/mol (334 J/g * 18.02 g/mol).
El calor de fusión ha fascinado a químicos y físicos porque demuestra que una sustancia puede absorber o liberar energía sin experimentar un cambio de temperatura. Cuando un mol de hielo a 0 °C absorbe 6020 julios de calor, el agua líquida resultante también se encuentra a 0 °C.
Calor Específico vs. Calor Latente
Normalmente, cuando una sustancia absorbe o cede energía en forma de calor, su temperatura cambia. La magnitud de este cambio de temperatura está determinada por el calor específico de la sustancia, una propiedad intrínseca que indica la cantidad de energía necesaria para elevar la temperatura de un gramo de la sustancia en un grado Celsius. Por ejemplo, el calor específico del oro es 0.128 J/g°C.
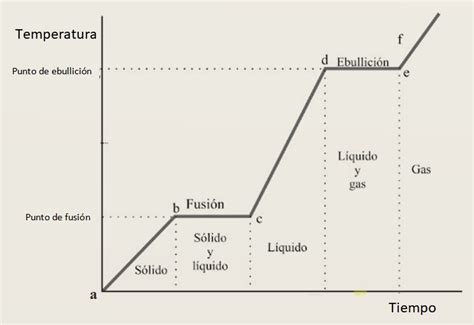
A diferencia del calor específico, que se relaciona con los cambios de temperatura dentro de una misma fase, el calor latente se asocia con la energía transferida durante las transiciones entre fases. Una gráfica de calor versus temperatura para una sustancia que no experimenta cambios de fase es lineal. Sin embargo, cuando se incluyen los cambios de fase, la gráfica presenta tramos planos que corresponden a la fusión y la vaporización.
La temperatura se define como la energía cinética media por molécula. Durante un cambio de fase, la energía térmica añadida no aumenta la velocidad de las moléculas (y por lo tanto la temperatura), sino que se utiliza para alterar su disposición y las fuerzas intermoleculares. En gases, el trabajo de expansión o compresión puede influir en la energía interna, pero en líquidos y sólidos, el cambio de volumen durante un cambio de fase es mínimo. Sin embargo, el calor de fusión implica un trabajo realizado para separar las moléculas, ya que en el estado sólido suelen estar más juntas que en el líquido.
Aplicaciones y Fenómenos Relacionados con el Calor Latente
El calor latente juega un papel crucial en diversos procesos naturales y tecnológicos:
Refrigeración y Congelación
El calor latente influye significativamente en los procesos de refrigeración y congelación industrial:
- Enfriamiento sensible: Disminución de la temperatura de un producto desde su temperatura inicial hasta su punto de congelación.
- Enfriamiento latente (calor latente): Proceso de congelación en el que se absorbe calor sin cambio de temperatura.
- Enfriamiento sensible posterior: Disminución de la temperatura del producto congelado hasta la temperatura de conservación deseada.
El calor latente de solidificación se libera cuando un líquido se enfría hasta su temperatura de fusión y comienza a solidificarse. Durante este proceso, la temperatura del producto no desciende hasta que la solidificación es completa.
Almacenamiento de Energía Térmica
El calor de cambio de estado permite almacenar el excedente de energía, por ejemplo, la obtenida de placas solares, durante períodos más largos. Los acumuladores de calor latente almacenan energía térmica mediante cambios de fase de materiales específicos (Materiales de Cambio de Fase o PCM). Estos materiales pueden ser polímeros o sales, y su transición de fase ocurre a temperaturas específicas.
La determinación del estado de carga de un acumulador de calor latente, es decir, la cantidad de energía térmica que puede almacenar o liberar, es un desafío. Se han desarrollado métodos que utilizan sensores de temperatura para medir la distribución térmica dentro del material de cambio de fases y, a partir de ahí, inferir el estado de carga. Esto permite un control más preciso y eficiente de los sistemas de almacenamiento térmico, especialmente en edificios de bajo consumo energético o en procesos industriales.
🔥 Las Leyes de la Termodinámica: una explicación sencilla
Presión y Punto de Ebullición
La presión atmosférica influye en el punto de ebullición. A mayor altitud, la presión es menor y el punto de ebullición disminuye. Por el contrario, en las ollas a presión, el aumento de la presión interior eleva la temperatura de ebullición, permitiendo cocinar los alimentos a temperaturas superiores a 100 °C y reduciendo el tiempo de cocción.
A cada presión le corresponde una temperatura de evaporación o temperatura de saturación específica.
El Hierro y su Punto de Fusión
El hierro puro se funde a una temperatura fija y precisa de 1,538 °C (2,800 °F) a presión atmosférica estándar. Este valor es una constante física fundamental en metalurgia y se utiliza como punto fijo en la Escala Internacional de Temperatura (ITS-90).
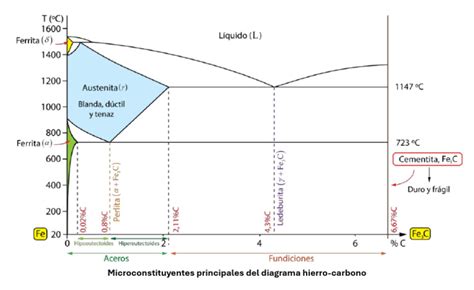
Incluso pequeñas cantidades de impurezas como carbono, azufre o fósforo pueden modificar significativamente este punto de fusión, un fenómeno conocido como depresión del punto de fusión. El carbono, en particular, tiene un efecto pronunciado: cada 0.1% de carbono reduce el punto de fusión en aproximadamente 10-15 °C. Por ello, el acero (una aleación de hierro y carbono) se funde a temperaturas inferiores, entre 1,370 °C y 1,540 °C, dependiendo de su contenido de carbono.
Antes de alcanzar su punto de fusión, el hierro puro experimenta varias transformaciones de fase en estado sólido:
- Alfa (α) a Beta (β) a 770 °C (temperatura de Curie): El hierro pierde sus propiedades ferromagnéticas. La estructura cristalina sigue siendo cúbica centrada en el cuerpo (BCC).
- Beta (β) a Gamma (γ) a 912 °C: El hierro cambia a una estructura cúbica centrada en las caras (FCC), conocida como austenita, que puede disolver más carbono.
- Gamma (γ) a Delta (δ) a 1,394 °C: El hierro vuelve a una estructura BCC (ferrita delta) antes de fundirse.
La presión también afecta drásticamente el punto de fusión del hierro. A presiones extremadamente altas, como las encontradas en el núcleo de la Tierra, el punto de fusión del hierro aumenta considerablemente, lo que explica por qué el núcleo interno permanece sólido a pesar de las temperaturas extremas.
El hierro puro es demasiado blando para aplicaciones estructurales; por ello, se alea con carbono para formar acero, que posee mayor resistencia y dureza. Las propiedades únicas del hierro puro (magnéticas, resistencia a la corrosión) lo hacen útil en aplicaciones especializadas.
El hierro líquido, con una densidad menor que el sólido, se utiliza en la fabricación de acero en hornos de oxígeno básico (BOF) y hornos de arco eléctrico (EAF), así como en procesos de fundición y en las zonas de fusión de soldadura.
tags: #calculo #calor #solidificacion