Importancia del Calor en las Reacciones Químicas
Para el campo de la química, resulta de gran interés conocer la cantidad de calor que interviene en una reacción química. En algunos casos, es necesario aportar energía en forma de calor para que la reacción se produzca, lo que se conoce como un proceso endotérmico. Esto implica un coste económico para suministrar dicha energía al sistema.
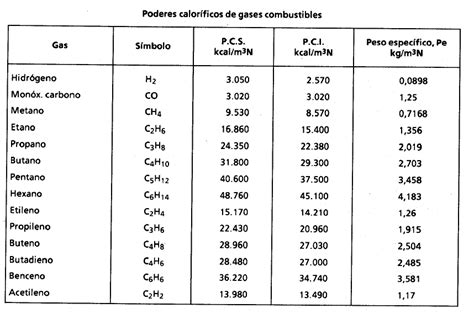
Los combustibles poseen una capacidad diferente para generar calor, dependiendo de cuánto calor desprenden al quemarse. Por esta razón, es fundamental conocer su calor de combustión.
Determinación del Calor de Combustión a partir de Energías de Enlace
Una pregunta común es qué sustancia proporciona más calor al quemarse. Por ejemplo, al comparar el propano y el butano, dos de los gases más utilizados, se busca determinar cuál es más eficiente energéticamente. Aunque existen varios procedimientos para averiguarlo, el más sencillo se basa en el cálculo a partir de las energías de enlace, también conocidas como entalpías de enlace.
Para realizar este cálculo, es necesario identificar qué enlaces químicos se rompen y cuáles se forman durante el transcurso de la reacción.
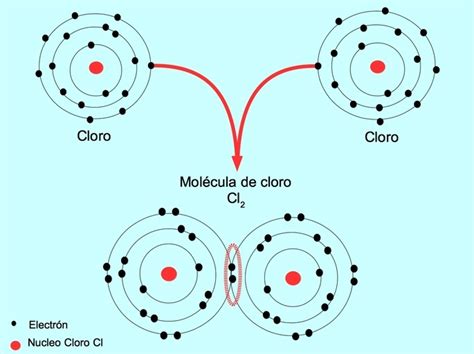
¿Qué es la Energía de Enlace?
Se denomina energía de enlace a la cantidad de energía necesaria para romper un mol de enlaces, lo que equivale a romper 6,023 x 1023 enlaces. Por analogía con las definiciones de entalpías de reacción, se suele emplear el término entalpía de enlace.
La energía química de los átomos unidos en una molécula es menor que la energía de los mismos átomos cuando están separados. Es importante destacar que estos valores son promedio. La energía de un enlace C-C, por ejemplo, no es la misma en el etano que en el butano, ya que en el primer caso los átomos de carbono enlazados solo tienen hidrógenos unidos, mientras que en el segundo caso hay grupos más complejos (metilo, etilo, etc.).
En las tablas de datos se presentan los valores medios obtenidos experimentalmente. Debido a esto, en ocasiones pueden observarse diferencias notables entre los resultados calculados utilizando energías de enlace y los datos experimentales. Por lo tanto, los resultados obtenidos por este método son únicamente aproximados.
Aplicación de las Energías de Enlace para Calcular el Calor de Reacción
Una vez que las energías de enlace están tabuladas, se utilizan para calcular los calores de reacción. El procedimiento implica detallar los enlaces que se rompen y los que se forman en la reacción. Posteriormente, se suman las energías de enlace de los enlaces rotos y se restan las energías de enlace de los enlaces formados.
En el siguiente vídeo se puede observar la resolución detallada de un ejercicio práctico sobre el cálculo del calor de reacción a partir de las energías de enlace.
Entalpía de reacción y formación EJEMPLOS
En el vídeo se utilizan los términos entalpía de reacción y entalpía de enlace. Es importante recordar que el término entalpía expresa el calor intercambiado cuando el proceso se lleva a cabo a presión constante, tal como se han definido los calores de reacción.
Para comprender mejor el proceso, se recomienda primero desplegar el apartado "Ejemplo de cálculo" para visualizar cómo se resuelve un caso específico. A continuación, utilizando los datos proporcionados en la "Tabla de valores", se puede seleccionar una reacción y calcular su calor de reacción correspondiente.
Ejemplo Práctico: Cálculo del Calor Desprendido al Quemar 10g de Combustible
Para calcular el calor desprendido al quemar una cantidad específica de combustible, como por ejemplo 10 gramos, se deben seguir una serie de pasos:
- Identificar la reacción de combustión: Escribir la ecuación química balanceada para la combustión completa del combustible en cuestión (por ejemplo, la combustión del metano: CH4 + 2O2 → CO2 + 2H2O).
- Determinar las energías de enlace involucradas: Identificar todos los enlaces químicos que se rompen en los reactivos y todos los enlaces que se forman en los productos. Consultar una tabla de energías de enlace promedio para obtener los valores correspondientes a cada tipo de enlace.
- Calcular la entalpía de reacción: Utilizar la siguiente fórmula general:
ΔHreacción = Σ (Energías de enlace de los enlaces rotos) - Σ (Energías de enlace de los enlaces formados) - Calcular el calor desprendido por mol: El valor de ΔHreacción obtenido en el paso anterior representa el calor desprendido por mol de combustible que reacciona. Si el valor es negativo, indica que la reacción es exotérmica y libera calor.
- Convertir a gramos: Calcular la masa molar del combustible.
- Calcular el calor desprendido para la cantidad dada: Utilizar la masa molar y la cantidad de combustible (en este caso, 10g) para determinar la cantidad de calor desprendido. Si se tiene el calor desprendido por mol y la masa molar, se puede calcular el calor desprendido por gramo y luego multiplicarlo por la cantidad deseada (10g).
Por ejemplo, si se desea calcular el calor desprendido al quemar 10g de metano (CH4), y se conoce la entalpía de combustión molar del metano, el cálculo sería:
Calor desprendido = (Entalpía de combustión molar del metano) x (Moles de metano en 10g)
Moles de metano = 10g / Masa molar del metano (aproximadamente 16 g/mol)