Los concentrados de hematíes (CH), también conocidos como glóbulos rojos empaquetados, son un componente sanguíneo fundamental obtenido a partir de la sangre total mediante centrifugación, separando el plasma y la capa leucoplaquetar. Su principal función es aumentar la masa eritrocitaria en pacientes con anemia, mejorando así la capacidad de transporte de oxígeno a los tejidos.
La eritropoyetina (EPO) es una glicoproteína crucial en la regulación de la eritropoyesis, el proceso de formación de glóbulos rojos. Actualmente, existen diversas moléculas de EPO recombinante humana y sus biosimilares disponibles para uso terapéutico, que pueden complementar o, en ciertos casos, reemplazar la necesidad de transfusiones.
La anemia, caracterizada por una disminución en la cantidad de glóbulos rojos o hemoglobina, resulta en un aporte insuficiente de oxígeno a los tejidos (hipoxia tisular). Esta condición puede manifestarse a través de una variedad de signos y síntomas que, en muchos casos, pueden ser aliviados mediante la transfusión de hematíes y/o el uso de EPO.
Indicaciones y Consideraciones en la Transfusión de Concentrados de Hematíes
La transfusión de CH está indicada principalmente en situaciones donde existe anemia, es necesario disminuir la hipoxemia tisular y no se dispone de un tratamiento farmacológico eficaz. Sin embargo, como con cualquier intervención terapéutica, es crucial sopesar el balance beneficio/riesgo, especialmente considerando los posibles efectos adversos asociados a la transfusión.
El beneficio obtenido de una transfusión de CH es, por naturaleza, transitorio. Por ello, es imperativo que la transfusión se acompañe de un tratamiento etiológico que aborde la causa subyacente de la anemia. La EPO, por su parte, tiene indicaciones muy precisas y su administración debe ir acompañada de suplementos de hierro, a menos que exista una sobrecarga férrica preexistente en el paciente.
Investigación sobre la Calidad y Rendimiento de los Concentrados de Hematíes
La seguridad del paciente en el contexto de las transfusiones sanguíneas es una preocupación primordial. La investigación se centra en la implementación de medidas que disminuyan los efectos adversos y mejoren el rendimiento transfusional.
Un área de interés particular es la antigüedad de los concentrados de hematíes. Algunos estudios han sugerido una posible asociación entre la transfusión de "sangre vieja" (unidades de almacenamiento prolongado) y la aparición de efectos adversos. En la práctica clínica, cada hemoderivado es proporcionado por el Banco de Sangre, especificando sus características, fecha de extracción y caducidad. Los CH comúnmente cumplen con criterios de conservación en solución salino-adenina-glucosa-manitol, un volumen de aproximadamente 250 ml, un contenido mínimo de hemoglobina, una viabilidad eritrocitaria determinada, un hematocrito entre 60-80% y una caducidad de 42 días desde la fecha de extracción.
La compatibilidad de los CH se garantiza mediante protocolos estandarizados que incluyen pruebas cruzadas entre el paciente y los hemoderivados. Si bien no siempre se cuantifican rutinariamente los niveles de potasio postransfusionales, su monitorización puede ser interesante para estudios posteriores.
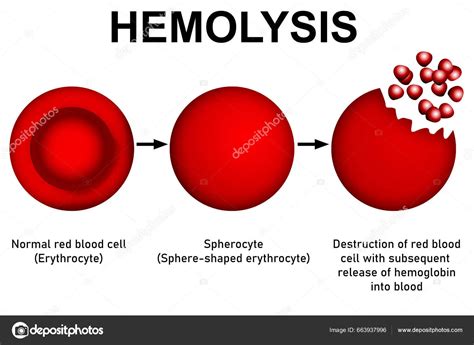
El rendimiento transfusional, que se refiere a la eficacia de la transfusión en mantener la masa eritrocitaria funcional, puede ser analizado junto con el grado de hemólisis. Estudios han observado un menor rendimiento esperado y una mayor hemólisis en concentrados de mayor antigüedad (superiores a 14 días). Estos hallazgos pueden motivar cambios en la política transfusional, como la priorización de la provisión de CH de "sangre joven" (menor de 14 días).
Aspectos Clave de la Hemoterapia y la Transfusión
La hemoterapia es una disciplina en constante evolución, requiriendo un conocimiento actualizado de los avances técnicos en la preparación y uso de la sangre y sus componentes. Este conocimiento es esencial para microbiólogos, médicos y enfermeras involucrados en la transfusión.
La sangre y los hemocomponentes son considerados tejido hematopoyético humano y deben manejarse con un criterio profesional para preservar su calidad y actividad hemoterapéutica. Los problemas inmunológicos pueden presentarse, similares a los de los trasplantes de órganos, además de otros inherentes a la sangre.
La indicación de una transfusión, así como la dosificación, velocidad de infusión y responsabilidad por las consecuencias, recae en el médico. El profesional del banco de sangre debe asegurar la calificación necesaria para despachar productos sanguíneos equivalentes. La enfermera, por su parte, debe estar atenta a los diferentes grados y tipos de reacciones transfusionales y sus procedimientos correctivos.
Selección y Análisis de Donantes de Sangre
Los donantes de sangre, ya sean voluntarios, familiares o donantes autólogos, son sometidos a un riguroso proceso de selección que incluye entrevistas y cuestionarios para evaluar su idoneidad. Se informa a los donantes sobre las enfermedades transmisibles por transfusión y los riesgos asociados, incluyendo el VIH, y se les ofrece la posibilidad de autoexclusión.
La sangre donada es analizada para detectar diversas enfermedades infecciosas transmisibles, como:
- Enfermedad de Chagas (tripanosomiasis americana).
- Malaria.
- Hepatitis B y C.
- Sífilis.
- VIH-SIDA.
La positividad para estas enfermedades puede resultar en el rechazo permanente o temporal del donante, según el caso.
Información Esencial en las Bolsas de Sangre
Cada unidad de sangre o hemocomponente debe contener información detallada, incluyendo:
- Nombre del producto e instrucciones especiales.
- Método de obtención.
- Temperatura de almacenamiento.
- Soluciones conservantes o anticoagulantes.
- Volumen y número de unidades en un pool.
- Identificación de la unidad y del centro procesador.
- Fecha y hora de vencimiento.
- Clasificación del donante.
- Grupo sanguíneo y factor Rho.
- Constancia de verificación de identidad del receptor.
- Resultados de pruebas para enfermedades infecciosas.
Fundamentos de la Transfusión Sanguínea
La decisión de transfundir a un paciente debe basarse en tres razones fundamentales y universales:
- Reposición del volumen sanguíneo.
- Reponer la capacidad de oxigenación.
- Hemostasia.
La indicación médica de una transfusión conlleva responsabilidades legales. Previamente, se requiere una evaluación médica directa, anotación de las razones en el expediente e indicación de cantidades, frecuencia, tipos y precauciones especiales.
Componentes Sanguíneos y Plasmáticos
La tabla a continuación resume los principales hemocomponentes, su composición y recomendaciones de uso:
| Hemocomponente | Composición | Recomendación |
|---|---|---|
| Sangre total | 500 ml/unidad: GR, PI, GB, Pk | Incrementar masa eritrocítica, plasmática y coagulación. |
| Glóbulos Rojos empacados | 250 ml/unidad: GR, PI, GB, Pk | Incrementar masa eritrocítica en anemias. |
| Glóbulos rojos sin leucocitos | 200 ml/unidad: GB < 5x108, Pk, PI, GR | Incrementar masa eritrocítica, evitar reacciones no hemolíticas. |
| Glóbulos rojos lavados | 180 ml/unidad: GB < 5x108, GR (sin plasma) | Incrementar masa eritrocítica, menor riesgo de reacción alérgica, febril, por proteínas plasmáticas. |
| Concentrado de plaquetas | 50 ml/unidad: Pk > 5,5x1010, GR, GB, PI | Sangrados por trombocitopenia o trombopatía. |
| Plaquetas por aféresis | 300 ml/procedimiento: Pk > 3x1011, GR, GB, PI | Igual que para plaquetas solas. |
| Plasma fresco congelado | 220 ml/unidad: Todos los factores de coagulación y de complemento | Tratamiento de trastornos de la coagulación. |
| Crioprecipitado | 5-15 ml/bolsa: Fibrinógeno, factores VIII, XIII y Von Willebrand | Hemofilia A, deficiencias de coagulación. |
Simbología: GR=Glóbulos rojos. GB: Glóbulos blancos. PI: Plasma. Pk: Plaquetas.
En pacientes trasplantados o inmunodeficientes, se pueden utilizar hemocomponentes filtrados o irradiados, prestando atención a los problemas asociados al potasio y a las transfusiones en nefrología. Los filtros para remoción de leucocitos son importantes para prevenir la reacción injerto contra huésped. Sustitutos como coloides y cristaloides, así como procedimientos de autotransfusión o hemodilución normovolémica, son alternativas consideradas.
Instrucciones Generales para la Transfusión
Al recibir un hemocomponente, el personal a cargo del paciente debe confirmar la correspondencia entre la documentación y la bolsa, así como verificar la identidad del receptor. La bolsa debe estar intacta y a la temperatura adecuada de mantenimiento (4°C para sangre, glóbulos rojos y plasma; temperatura ambiente para plaquetas y crioprecipitados).
Se debe utilizar un filtro regular de 200 µ. En casos específicos, se emplean filtros removedores de leucocitos. Toda sangre o hemocomponente debe ser agitada adecuadamente y no debe administrarse ningún medicamento o solución junto con la sangre o hemocomponente.
Transfusión de hemoderivados
Debates sobre la Transfusión de Concentrados de Hematíes y su Impacto Clínico
La transfusión de sangre es una terapia frecuente en el paciente crítico, pero su eficacia para disminuir la deuda tisular de oxígeno no ha sido consistentemente documentada. Investigaciones recientes sugieren una asociación entre la transfusión de sangre y el aumento de la morbimortalidad en estos pacientes.
Este incremento en la morbimortalidad podría estar relacionado con el efecto inmunosupresor que la sangre produce en el receptor, el cual parece estar ligado al tiempo de almacenamiento de la misma (efecto TRIM: transfusion-related immunomodulation).
Eficacia y Riesgos de la Transfusión Alogénica
Desde mediados del siglo XX, la transfusión de sangre alogénica (TSA) ha sido una práctica habitual para tratar la anemia, especialmente en pacientes críticos. Sin embargo, la creencia en la seguridad inherente de las transfusiones ha llevado a un uso liberal, a pesar de que la eficacia de la TSA en disminuir la mortalidad o morbilidad no siempre está claramente demostrada.
Si bien las técnicas de escrutinio de la sangre donada han reducido drásticamente el riesgo de transmisión de infecciones virales, la seguridad "cero" es casi imposible de alcanzar. Además, existen efectos adversos no infecciosos, inmunológicos o no, que son difíciles de controlar y se asocian a morbilidad. El envejecimiento de la población, la cirugía sofisticada y la creencia en una sangre "segura" han contribuido a un crecimiento exponencial de las TSA, mientras que la oferta de sangre disminuye.
La investigación sobre los efectos de la TSA en el paciente crítico es más reciente. Se cuestiona la eficacia de la sangre para aumentar el transporte de oxígeno con mínimos efectos indeseables, y algunos estudios sugieren que la TSA podría no ser aprobada hoy por la FDA debido a la falta de estudios que documenten su eficacia.
Aunque la transfusión puede ser eficaz en situaciones de pérdidas masivas de sangre y hemodiluciones graves, la mayor parte de los intensivistas prescriben TSA a pacientes con niveles de hemoglobina solo relativamente bajos. La evidencia de que la TSA aumente el transporte de oxígeno y, por ende, disminuya la hipoxia tisular, no es inequívoca. Tampoco hay evidencia concluyente de que transfundir aumente la supervivencia en todos los casos.
Estudios observacionales recientes han mostrado una asociación entre la TSA y un incremento de la morbimortalidad, incluso después de controlar variables de confusión. Comparar estrategias transfusionales restrictivas con otras liberales ha demostrado que una política restrictiva puede disminuir la tasa transfusional sin incrementar la morbimortalidad.
Mecanismos Potenciales de la Morbimortalidad Asociada a la Transfusión
El efecto TRIM (inmunomodulación relacionada con la transfusión) es un fenómeno por el cual la sangre alogénica modula la respuesta inmune del receptor. Si bien puede tener efectos beneficiosos en trasplantes, en el contexto transfusional se ha asociado con un incremento de la infección nosocomial y la recurrencia de neoplasias.
Se han formulado múltiples teorías para explicar el efecto deletéreo de la transfusión, incluyendo:
- La participación de leucocitos del donante.
- La presencia de sustancias bioactivas liberadas durante el almacenamiento.
- Mecanismos no inmunes que producen daño tisular y disfunción orgánica (ej. TRALI - transfusion-related acute lung injury).
Los efectos deletéreos de la TSA guardan una relación directa con el número de bolsas transfundidas y el tiempo de almacenamiento de las mismas. Los hematíes almacenados durante períodos prolongados ("hematíes viejos") presentan cambios morfológicos y funcionales que limitan su capacidad de deformarse y ceder oxígeno, pudiendo tener repercusiones fisiopatológicas significativas, como isquemia visceral.
El tiempo de almacenamiento prolongado (superior a 2-3 semanas) se asocia con un incremento de la mortalidad, la estancia hospitalaria, el fracaso multiorgánico y la neumonía nosocomial, especialmente en pacientes politraumatizados o sometidos a cirugía cardíaca.
Debates sobre la Transfusión de Hematíes y el Resultado Clínico
Existe un debate continuo sobre si la transfusión de concentrados de hematíes (TCH) incrementa la oxigenación tisular y mejora el resultado clínico. Si bien la TCH aumenta la hemoglobina y el transporte de oxígeno en la mayoría de los casos, su impacto en el consumo de oxígeno tisular es menos claro y, en muchos estudios, no se incrementa.
El objetivo primordial de la TCH es aumentar la disponibilidad tisular de oxígeno en pacientes anémicos. La eficacia de la transfusión debe evaluarse por su capacidad de mejorar el resultado clínico y los parámetros de oxigenación tisular.
Anemia y Órganos Sensibles: Corazón y Cerebro
El corazón y el cerebro son órganos particularmente sensibles a la anemia e hipoxia. En el caso del corazón, la anemia puede mal tolerarse, especialmente en pacientes con cardiopatía isquémica. Si bien la corrección de la anemia puede mejorar el resultado clínico en algunos de estos pacientes, otros estudios no han demostrado beneficios consistentes, e incluso sugieren un empeoramiento del resultado clínico con la TCH.
El cerebro, con su alta tasa metabólica, requiere un suministro de oxígeno continuo. La anemia puede afectar negativamente la función cerebral, aunque los mecanismos de adaptación como la vasodilatación selectiva pueden compensar en individuos sanos. En pacientes con disfunción cerebral severa, la anemia puede agravar la situación. La relación entre anemia, TCH y resultado clínico en pacientes neurocríticos es compleja, y mientras algunos estudios sugieren que la TCH no revierte los efectos adversos de la anemia, otros indican que puede sumar sus propios efectos deletéreos.
Transfusión de Concentrado de Hematíes y Oxigenación Tisular
La eficacia de la TCH en incrementar la oxigenación tisular está influenciada por factores dependientes del paciente (hemoglobina basal, consumo basal de oxígeno) y de la calidad de los hematíes transfundidos (tiempo de almacenamiento). La TCH es más eficaz en pacientes con déficit tisular de oxígeno más pronunciado, como aquellos con bajos niveles basales de oxigenación cerebral o perfusión tisular.

Falacias, Riesgos y Verdades a Medias en la Transfusión
Es importante distinguir la asociación de la causa-efecto. Si bien los estudios observacionales muestran una asociación entre gravedad del paciente, anemia, transfusión y pobre resultado clínico, una relación causal directa entre TCH y aumento de la morbimortalidad no siempre se ha demostrado de forma concluyente. La TCH podría ser un marcador de la gravedad subyacente del paciente.
La relación entre el tiempo de almacenamiento prolongado y un pobre resultado clínico es compleja, ya que los pacientes politransfundidos tienen mayor probabilidad de recibir unidades de hematíes con tiempo de almacenamiento prolongado, lo que dificulta el control de variables por separado.
Finalmente, el objetivo de la TCH es aumentar el consumo tisular de oxígeno, y no solo la hemoglobina. La eficacia se valora por el incremento del consumo, lo cual no siempre ocurre tras la TCH. Si bien la anemia severa empeora la morbi-mortalidad, la TCH no siempre evita sus efectos deletéreos, pudiendo sumar sus propios riesgos.
tags: #concentrados #de #hematies #metabolismo