Energía de Enlace y su Relevancia
La energía de disociación de enlaces, también conocida como energía de enlace, es la energía necesaria para romper un enlace químico. En este proceso, un electrón desapareado, denominado radical, se forma en cada átomo tras la ruptura del enlace. Al medir la entalpía de un enlace, se rompe este para que la mitad de los electrones de enlace se transfieran a cada átomo. La ruptura de un enlace es siempre un proceso endotérmico, lo que significa que la energía de enlace es siempre un valor positivo.
La energía de enlace se refiere a la energía promedio requerida para romper todos los enlaces presentes en una molécula. Por ejemplo, la energía de enlace C-H en el metano se calcula dividiendo la entalpía de atomización del metano por 4.
Aplicaciones y Predicciones Basadas en la Energía de Enlace
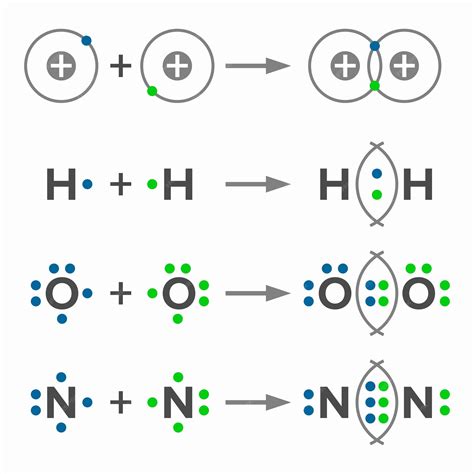
Comprender la fuerza de los enlaces químicos nos permite dilucidar las estructuras moleculares y predecir el comportamiento de las reacciones. Por ejemplo, al intentar determinar la disposición de los átomos en una estructura de Lewis, es preferible evitar la formación de enlaces débiles. Los enlaces simples como N-N y O-O son considerablemente débiles, por lo que se tiende a no incluirlos en las estructuras de Lewis, a menos que no existan otras alternativas viables.
Asimismo, el conocimiento de la fuerza de los enlaces facilita la predicción de la dirección en la que procederán las reacciones y su velocidad. La entalpía de una reacción puede calcularse comparando las energías de atomización de los reactivos y los productos. Este principio es análogo al cálculo de entalpías de reacción utilizando entalpías estándar de formación.
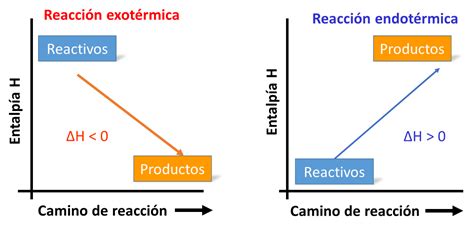
Si los productos de una reacción poseen enlaces más fuertes que los reactivos, es probable que la reacción sea exotérmica, y las reacciones exotérmicas tienden a ser espontáneas. Sin embargo, si los reactivos contienen enlaces fuertes, puede ser necesaria una cantidad significativa de energía para iniciar la reacción, incluso si esta es exotérmica. Las reacciones de combustión son un claro ejemplo: los enlaces C-C y C-H son bastante robustos, requiriendo una chispa o una llama para iniciar la combustión.
Otro caso relevante es la "fijación de nitrógeno". El nitrógeno es esencial para la síntesis de proteínas y otras moléculas vitales en nuestro organismo. No obstante, la obtención de nitrógeno a partir de N₂ es desafiante debido a la fortaleza del triple enlace. Esta dificultad subraya la necesidad de fertilizantes en la agricultura, y la producción de fertilizantes nitrogenados consume aproximadamente el 1% de la energía mundial.
El teflón, o PTFE, es un material conocido por su superficie resbaladiza y su baja reactividad, utilizado en sartenes antiadherentes y recipientes para sustancias químicas corrosivas. El PTFE está compuesto únicamente por enlaces C-C y C-F, los cuales son muy fuertes, lo que le confiere una notable resistencia a la reacción, incluso a altas temperaturas durante la cocción.
Por el contrario, la presencia de enlaces muy débiles en un reactivo puede facilitar el inicio de una reacción. El peróxido de hidrógeno (HOOH), por ejemplo, se emplea como blanqueador o desinfectante debido a la debilidad del enlace sencillo O-O, que puede romperse con facilidad, promoviendo la oxidación de sustancias cercanas.