En el vasto campo de la química, una sal se define como un compuesto químico que resulta de la combinación de cationes (iones con carga positiva) y aniones (iones con carga negativa). La proporción numérica entre estos iones es tal que el compuesto resultante es eléctricamente neutro, es decir, carece de carga neta. Las sales minerales desempeñan un papel crucial en los organismos vivos, no solo como componentes estructurales, sino también como reguladores fundamentales del pH, la presión osmótica y, de manera muy significativa, de las reacciones bioquímicas. Su participación en procesos químicos a nivel electrolítico es indispensable para la vida.
Los procesos vitales de los organismos requieren la presencia de ciertas sales en forma de iones específicos, como los cloruros, carbonatos y sulfatos. Entre los cationes más abundantes que componen los seres vivos se encuentran el sodio (Na+), el potasio (K+), el calcio (Ca2+) y el magnesio (Mg2+).
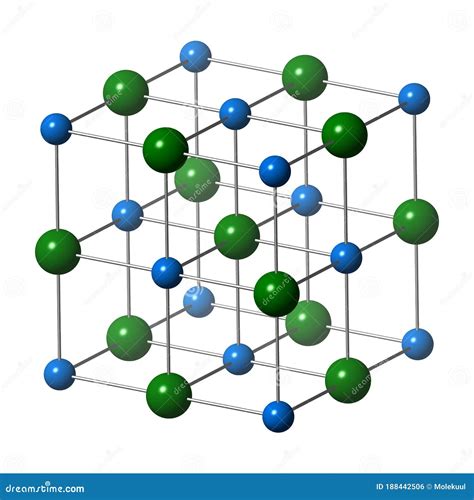
Estructura y Propiedades de las Sales Minerales
Las sales, en su estado sólido, suelen formar estructuras cristalinas, redes altamente ordenadas de aniones y cationes unidos por fuertes enlaces iónicos. Esta disposición confiere a muchas sales propiedades particulares. Generalmente, las sales sólidas son transparentes, aunque su apariencia opaca o transparente puede deberse a la diferencia en el tamaño de los cristales individuales.
Un fenómeno interesante ocurre con las sales de los metales de transición: en solución acuosa y en forma cristalina, a menudo presentan coloración. Esto se debe a las transiciones electrónicas en los orbitales 'd' de estos metales. Los electrones, dispuestos en orbitales alrededor del núcleo del átomo metálico, pueden transitar entre niveles de energía dentro de los orbitales 'd' parcialmente llenos. Cuando un electrón absorbe un fotón de luz, salta a un orbital de mayor energía, y la energía de esta excitación corresponde a la frecuencia de la luz absorbida. Si esta frecuencia se encuentra en el espectro visible, el compuesto o complejo adquiere un color determinado. La longitud de onda de la luz absorbida está influenciada por el tamaño de la brecha energética entre los orbitales 'd', la cual, a su vez, depende del tipo de ligando y la carga del ion metálico.
Conductividad Eléctrica y Solubilidad de las Sales
La conductividad, o conductancia específica, de una solución electrolítica es una medida de su capacidad para conducir la electricidad. Las sales, al ser compuestos iónicos, presentan un comportamiento particular respecto a la conducción eléctrica. En estado sólido, sus iones no son libres de moverse, lo que impide la conducción. Sin embargo, al fundirse o disolverse en un disolvente adecuado, como el agua, los iones se separan (disocian) y se vuelven móviles, permitiendo la conducción de la corriente eléctrica.
Los compuestos que se disocian completamente en agua, formando iones capaces de transportar corriente de manera eficaz, se conocen como electrolitos fuertes. Cuanto mayor sea la concentración de iones en la solución, mayor será la conductividad. Ejemplos de electrolitos fuertes incluyen el cloruro de sodio (NaCl), el sulfato de amonio, el cloruro de calcio, el fosfato de sodio y el nitrato de zinc. Estos electrolitos fuertes son típicamente compuestos inorgánicos.
La solubilidad, definida como la capacidad de disolución de una sustancia, es otra propiedad crucial de las sales minerales. Muchos compuestos iónicos muestran una solubilidad significativa en agua y otros disolventes polares. A diferencia de los compuestos moleculares, las sales se disocian en solución en sus componentes aniónicos y catiónicos. La energía reticular, las fuerzas de cohesión entre los iones en el sólido, determina en gran medida la solubilidad. La interacción de cada ion con el disolvente también es un factor determinante. La solubilidad de una sustancia es una propiedad distinta a la velocidad de disolución, que se refiere a la rapidez con la que se disuelve.
Reglas Generales de Solubilidad
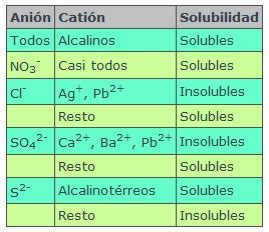
Existen reglas generales que sirven como guía para predecir la solubilidad de compuestos inorgánicos en agua, aunque siempre hay excepciones:
- Las sales que contienen elementos del Grupo I (Li+, Na+, K+, Cs+, Rb+) son generalmente solubles.
- Las sales que contienen Cl-, Br-, I- son generalmente solubles, con excepciones notables como las sales de Ag+, Pb2+ y (Hg2)2+.
- La mayoría de las sales de plata son insolubles.
- La mayoría de las sales de sulfato son solubles, aunque las de Ba2+, Sr2+, Pb2+ y Ca2+ son menos solubles.
- La mayoría de las sales de hidróxido son solo ligeramente solubles. Las sales de hidróxido de los elementos del Grupo I son solubles, mientras que las de los elementos del Grupo II (Ca, Sr, Ba) son ligeramente solubles. Las sales de hidróxido de metales de transición y Al3+ son insolubles.
- La mayoría de los sulfuros de los metales de transición son altamente insolubles (ej. CdS, FeS, ZnS, Ag2S).
- Los carbonatos son generalmente insolubles, con la excepción de los carbonatos de los metales alcalinos y del amonio.
- Los cromatos y fosfatos son generalmente insolubles, con las mismas excepciones que los carbonatos.
- Los fluoruros son generalmente insolubles, con excepciones como los fluoruros de metales alcalinos y alcalinotérreos.
La constante del producto de solubilidad (Kps) es una constante de equilibrio que describe el grado de disolución de un compuesto iónico en agua. Representa el límite de la cantidad de sal que puede disolverse en un volumen determinado de agua. Un valor de Kps bajo indica que el compuesto es menos soluble.
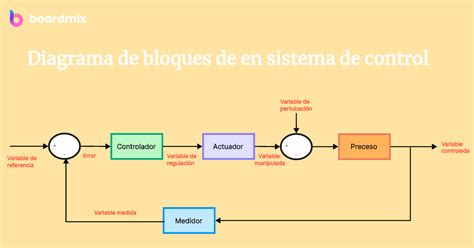
Sales Fuertes y Débiles: Impacto en el pH
Las sales pueden clasificarse según la fuerza de los ácidos y bases a partir de los cuales se forman:
- Sales fuertes (electrolitos fuertes): Compuestas por ácidos o bases fuertes, se disocian completamente en agua. Generalmente son inodoras y no volátiles. La mayoría de los metales de los grupos 1 y 2 forman sales fuertes.
- Sales débiles (electrolitos débiles): Compuestas por ácidos o bases débiles, su disociación en agua es parcial. Suelen ser más volátiles que las sales fuertes y pueden tener olores característicos de sus ácidos o bases constituyentes.
Cuando las sales se disuelven en agua, pueden reaccionar con ella en un proceso conocido como hidrólisis, alterando el pH de la solución. El resultado de esta hidrólisis depende de la fuerza relativa del ácido y la base de los que proviene la sal:
- Sales de bases fuertes y ácidos fuertes (ej. NaCl): No se hidrolizan y el pH se mantiene neutro (pH 7).
- Sales de bases fuertes y ácidos débiles (ej. acetato de sodio): El anión (acetato) proviene de un ácido débil y tenderá a aceptar protones del agua, liberando iones hidróxido (OH-). Esto resulta en un pH básico (pH > 7).
- Sales de bases débiles y ácidos fuertes (ej. cloruro de amonio): El catión (amonio) proviene de una base débil y tenderá a donar protones al agua, generando iones hidronio (H3O+). Esto resulta en un pH ácido (pH < 7).
- Sales de bases débiles y ácidos débiles: La hidrólisis es más compleja y el pH final dependerá de las constantes de acidez (Ka) y basicidad (Kb) del ácido y la base débiles correspondientes. El más fuerte de los dos determinará el carácter ácido o básico predominante.
Hidrólisis de sales I | Química | Equilibrio Iónico | V11 | Egg Educación
Funciones Biológicas de las Sales Minerales
Las sales minerales son fundamentales para la vida, desempeñando múltiples funciones esenciales en las células y en el organismo:
Función Estructural
Algunas sales minerales, como el carbonato cálcico y el fosfato cálcico, son componentes estructurales importantes. El carbonato cálcico forma caparazones y esqueletos en muchos organismos marinos, mientras que el fosfato cálcico es un constituyente esencial de los huesos y dientes de los vertebrados, proporcionando dureza y resistencia.
Regulación del pH (Función Tampón)
Las sales minerales juegan un papel vital en el mantenimiento de la homeostasis del pH en los fluidos biológicos. Las soluciones tampón o amortiguadoras, compuestas por ácidos débiles y sus bases conjugadas, son capaces de neutralizar pequeñas cantidades de ácidos o bases añadidas, evitando cambios bruscos de pH. Esto es crucial, ya que muchas reacciones bioquímicas, especialmente las catalizadas por enzimas, requieren un rango de pH muy específico para funcionar de manera óptima. Ejemplos comunes de sistemas tampón en los seres vivos incluyen el sistema bicarbonato (HCO3-/H2CO3) en el plasma sanguíneo y el sistema fosfato (H2PO4-/HPO42-) en el interior de las células.
Regulación de la Presión Osmótica y el Volumen Celular
Las sales disueltas en los fluidos corporales generan potenciales eléctricos y contribuyen a mantener el equilibrio osmótico entre el interior y el exterior de las células. La diferencia en las concentraciones de iones dentro y fuera de la célula crea un gradiente que influye en el movimiento del agua, regulando así el volumen celular y previniendo la lisis (ruptura) o la crenación (deshidratación) de las células. Iones como el sodio (Na+) y el potasio (K+) son particularmente importantes en este proceso, participando activamente en la bomba de sodio-potasio que mantiene los gradientes iónicos a través de las membranas celulares.
Participación en Reacciones Bioquímicas
Numerosos iones derivados de sales minerales actúan como cofactores o activadores de enzimas, siendo indispensables para la catálisis de una amplia gama de reacciones metabólicas. Por ejemplo, el magnesio (Mg2+) es esencial para la transferencia de grupos fosfato en reacciones que involucran ATP, y el hierro (Fe2+/Fe3+) es un componente clave de proteínas como la hemoglobina y los citocromos, involucradas en el transporte de oxígeno y en las reacciones de óxido-reducción.
Otras Funciones
Las sales minerales también participan en la transmisión del impulso nervioso, la contracción muscular, la coagulación sanguínea y son constituyentes de moléculas biológicas importantes como vitaminas y hormonas.
Aplicaciones Industriales y de Laboratorio
Las sales minerales tienen un amplio espectro de aplicaciones industriales y de laboratorio. Se utilizan en la fabricación de vidrio, papel, plásticos, textiles, tintes, cosméticos, productos farmacéuticos y fertilizantes. En el ámbito del análisis químico y farmacéutico, se emplean reactivos de alta pureza (grado p.a., ACS, farmacopea) y materias primas para procesos de fabricación, ajustes de pH y formulaciones finales de medicamentos.
