El metabolismo fosfocálcico es un proceso complejo y finamente regulado, esencial para el mantenimiento de la homeostasis en el organismo. En los mamíferos, el tejido endocrino primariamente involucrado en esta regulación se encuentra en la región de la glándula tiroides.
Regulación Endocrina del Metabolismo Fosfocálcico
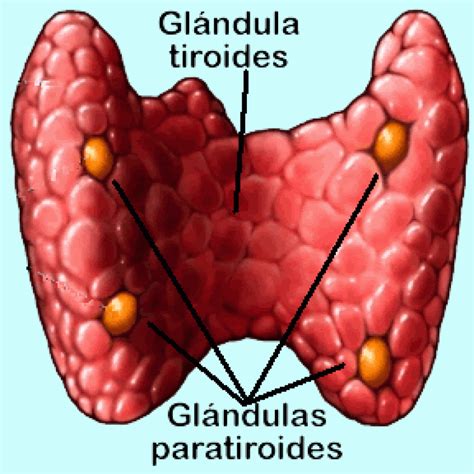
Las glándulas paratiroides, ubicadas en la cara dorsal de los lóbulos tiroideos, juegan un papel crucial al secretar la hormona paratiroidea (PTH). Paralelamente, las células C o parafoliculares del tiroides, localizadas externamente a los folículos, secretan calcitonina. Ambas hormonas, junto con la vitamina D, son fundamentales para mantener la concentración de calcio extracelular, un parámetro biológico altamente controlado cuyo valor normal se sitúa alrededor de 2.4 mmol/litro, con un rango de variación de 2.1 a 2.6 mmol/litro.
Hormona Paratiroidea (PTH)
La PTH es un polipéptido secretado por las glándulas paratiroides, que son cuatro pequeñas estructuras con un peso aproximado de 30-50 mg cada una. Estas glándulas están rodeadas por una cápsula fibrosa que se extiende formando tabiques internos, separando cordones celulares. Los tipos celulares principales son las células principales, responsables de la síntesis y secreción de la hormona, y las células oxífilas, más grandes y hormonalmente inactivas.
La síntesis de la PTH comienza como una preprohormona, que tras su secreción es convertida en la hormona activa mediante la eliminación de fragmentos en el hígado y riñón.
Acciones de la PTH
- Elevación de calcio plasmático y disminución de fosfato: La PTH actúa directamente sobre la concentración de estos minerales en la sangre.
- Sobre el hueso: Incrementa la actividad de los osteocitos y osteoclastos, promoviendo la resorción ósea (osteolisis) y disminuyendo la formación ósea (osteogénesis). Este mecanismo es vital para la regulación a largo plazo del calcio.
- Sobre el riñón: Ejerce un efecto crucial en la regulación a corto plazo. Aumenta la reabsorción tubular de calcio y, simultáneamente, disminuye la reabsorción de fosfato. Esta disminución de fosfato en plasma no solo favorece la liberación de calcio del hueso, sino que también previene el depósito de fosfato cálcico al carecer de fosfato.
- Estimulación de la Vitamina D: En el riñón, la PTH estimula la formación de la forma activa de la vitamina D.
Calcitonina
La calcitonina es un polipéptido sintetizado en las células C o parafoliculares del tiroides. Su función principal es la de disminuir la concentración de calcio plasmático, actuando de forma antagónica a la PTH.
Vitamina D
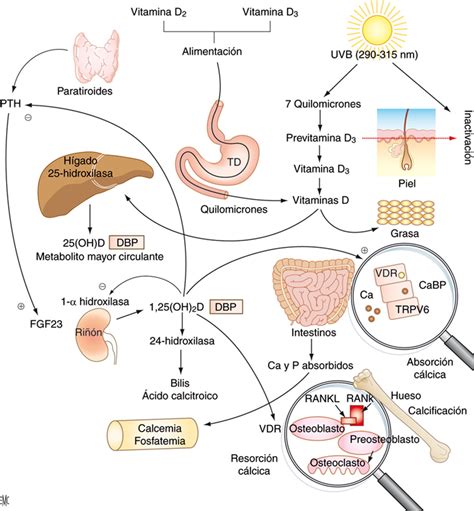
La vitamina D es un esteroide esencial para el correcto desarrollo óseo. Su carencia provoca raquitismo en niños y osteomalacia en adultos. Se obtiene de la dieta como vitamina D3 (colecalciferol) de origen animal o vitamina D2 (ergocalciferol) de origen vegetal, o se sintetiza en la piel bajo la acción de la luz solar.
La vitamina D es una prohormona que requiere dos hidroxilaciones para activarse:
- En el hígado, se convierte en 25-hidroxicolecalciferol (25-hidroxivitamina D).
- En el riñón, se transforma en 1,25-dihidroxicolecalciferol (1,25-dihidroxivitamina D o calcitriol), la forma hormonalmente activa.
La enzima renal que cataliza esta última hidroxilación es estimulada por la PTH y por estados de hipocalcemia e hipofosfatemia. El calcitriol actúa sobre el intestino delgado, favoreciendo la absorción de calcio y fosfato.
Compartimentalización del Calcio y Fósforo
El hueso es el principal reservorio de calcio y fósforo en el organismo. Aproximadamente el 99% del calcio corporal y cerca del 80% del fósforo se localizan en el esqueleto.
Células Óseas y su Función
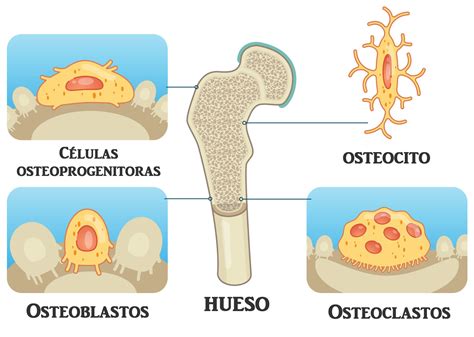
Tres tipos principales de células intervienen en la formación y resorción ósea:
- Osteoblastos: Sintetizan colágeno y promueven el depósito de sales cálcicas, participando activamente en la formación ósea.
- Osteoclastos: Son responsables de la resorción del hueso, descomponiendo la matriz ósea a través de enzimas lisosomales y fagocitosis.
- Osteocitos: Derivados de los osteoblastos, una vez rodeados por matriz calcificada, son las células más numerosas. Juegan un papel fundamental en el intercambio de calcio entre el líquido extracelular y el hueso, una función regulada hormonalmente.
Absorción Intestinal de Calcio y Fósforo
En una dieta estándar, se ingieren diariamente alrededor de 25 mmol (1g) de calcio y fósforo, en su mayoría en forma de fosfato cálcico, proveniente principalmente de productos lácteos.
La absorción intestinal neta de calcio es un proceso que depende de las necesidades nutricionales y se lleva a cabo principalmente en el duodeno mediante transporte activo. Los factores que incrementan esta absorción incluyen la presencia de vitamina D, fosfatos orgánicos y un pH ácido.
Excreción Renal de Calcio y Fósforo
El riñón es el principal órgano encargado de la excreción de calcio y fósforo, regulando el balance mineral del organismo a través de la reabsorción y filtración tubular.
Metabolismo Mineral en la Enfermedad Renal Crónica (ERC)
Las alteraciones del metabolismo mineral y óseo (MMO) son un desafío significativo en pacientes con enfermedad renal crónica (ERC). El término Alteraciones del Metabolismo Óseo y Mineral asociadas a la Enfermedad Renal Crónica (CKD-MBD) integra todas las perturbaciones bioquímicas, esqueléticas y calcificaciones extraesqueléticas que ocurren en este contexto.
Fisiopatología de CKD-MBD
La pérdida progresiva de masa y función renal afecta la homeostasis mineral. El riñón es crucial para la regulación del balance de fósforo y la producción de moléculas reguladoras como el calcitriol y la klotho.
- Retención de Fósforo: Con el deterioro renal, la capacidad de excretar fósforo disminuye, lo que puede llevar a hiperfosfatemia. El FGF-23 juega un papel clave en la fosfaturia, y su resistencia en la ERC contribuye a la retención de fósforo.
- Déficit de Calcitriol: La disminución de la función renal, la menor disponibilidad de sustrato, la acción inhibidora del FGF-23 y la pérdida de masa renal reducen la síntesis de calcitriol. Esto compromete la absorción intestinal de calcio y fósforo.
- Hiperparatiroidismo Secundario (HPTS): La retención de fósforo, el déficit de calcitriol y la hipocalcemia (a menudo transitoria) desencadenan un HPTS. El aumento de la hormona paratiroidea (PTH) se observa con filtrados glomerulares inferiores a 60 mL/min/1.73 m².
- Papel de Klotho: La proteína klotho, un correceptor del FGF-R1, es crucial para la acción del FGF-23. Su expresión disminuye en la ERC, contribuyendo a la resistencia al FGF-23 y a la menor excreción de fósforo.
ENFERMEDAD RENAL CRÓNICA ✅ fisiopatología, clínica, diagnòstico y tratamiento
Receptores y Regulación de la PTH
Las glándulas paratiroides poseen receptores que modulan la síntesis y secreción de PTH:
- Receptor de Vitamina D (RVD): La vitamina D ejerce su acción inhibitoria sobre la PTH a través de este receptor. Su disminución en la ERC genera resistencia a la acción de la vitamina D.
- Receptor-sensor de Calcio (RSCa): Detecta cambios en los niveles de calcio sérico y regula la secreción de PTH. La hiperplasia paratiroidea asociada a la ERC también disminuye la densidad de este receptor. El fósforo elevado estimula directamente la secreción de PTH, posiblemente al disminuir la actividad del RSCa.
- Receptor 1 del Factor de Crecimiento Fibroblástico (FGF-R1) y Klotho: En condiciones normales, el FGF23 ejerce una acción inhibitoria sobre la glándula paratiroides a través de FGF-R1 y klotho. En la ERC, la disminución de estos componentes conduce a resistencia a la acción inhibitoria del FGF23.
Clasificación de la Osteodistrofia Renal (ODR)
Clásicamente, la ODR se ha clasificado en dos tipos:
- Alto Remodelado (AR): Caracterizado por la Osteítis Fibrosa, con aumento de la actividad celular osteoclástica y osteoblástica.
- Bajo Remodelado (BR): Incluye la Osteomalacia (déficit de mineralización) y la Enfermedad Ósea Adinámica (mineralización normal).
Las guías KDIGO proponen una clasificación más integrada basada en tres parámetros histológicos: remodelado, mineralización y volumen óseo, buscando una armonía en los criterios diagnósticos.
Alteraciones Específicas del Metabolismo Fosfocálcico
Hipocalcemia
Se define por una concentración de calcio total < 8.5 mg/dL o calcio iónico < 4.4 mg/dL. En pediatría, puede ser transitoria en el neonato (precoz o tardía) o deberse a hipoparatiroidismo, mutaciones en el receptor sensible al calcio (CaSR) o hipomagnesemia en niños mayores. Los síntomas se relacionan con el aumento de la excitabilidad neuromuscular, como la tetania.
Hipercalcemia
Se sospecha ante una concentración de calcio total > 10.5 mg/dL o calcio iónico > 5.2 mg/dL. Las causas pediátricas incluyen el hiperparatiroidismo primario (adenoma paratiroideo, neoplasias endocrinas múltiples), hipercalcemia hipocalciúrica familiar, exceso de vitamina D, inmovilización, ciertos tóxicos y la hipercalcemia maligna asociada a tumores.
Hipofosforemia
Definida por una concentración de fósforo sérico < 2.5 mg/dL, grave si es < 1.5 mg/dL. En niños sanos es rara, pero puede asociarse a problemas neurológicos y osteomusculares en casos graves. La orientación diagnóstica se basa en la capacidad de reabsorción tubular de fósforo.
Hiperfosfatemia
Concentración de fósforo sérico > 6.5 mg/dL. Es rara, salvo en niños con insuficiencia renal crónica, donde se asocia a hiperparatiroidismo secundario y osteodistrofia renal. Si el producto Ca-P sérico supera 60, existe riesgo de hipocalcemia y calcificaciones metastásicas.

Calcificaciones Extraskeleticas
Las alteraciones del metabolismo fosfocálcico, especialmente en el contexto de la ERC, predisponen a la aparición de calcificaciones extraesqueléticas, como las cardiovasculares y de partes blandas. Estas calcificaciones son predictoras independientes de mortalidad cardiovascular y su prevalencia aumenta con el uso de suplementos de calcio y vitamina D, así como con la edad.
La calcifilaxis es una complicación grave caracterizada por necrosis isquémica dolorosa, secundaria a la calcificación de la media arterial. Afecta principalmente a muslos, abdomen y mamas, y puede presentar lesiones isquémicas en dedos o pene.
La calcificación masiva metastásica de partes blandas, a menudo periarticular, puede ser asintomática o causar compresión nerviosa y limitación del movimiento articular.
La ruptura espontánea de tendones, especialmente el de Aquiles y cuádriceps, puede ocurrir en pacientes con amiloidosis por ß2M o hiperparatiroidismo secundario severo.
Monitoreo y Manejo Terapéutico
La determinación periódica de calcio, fósforo y PTH séricos es fundamental para el manejo del paciente. Se recomienda la medición mensual de calcio y fósforo, y bimestral de PTH, para evaluar tendencias y ajustar el tratamiento.
Las guías KDIGO sugieren mantener concentraciones de fósforo normales. En pacientes en diálisis, la hiperfosfatemia se asocia a mayor mortalidad.
tags: #metabolismo #fosfocalcico #esquema