El **julio por mol** (símbolo: J·mol⁻¹ o J/mol) es una unidad de energía derivada del Sistema Internacional (SI) que se utiliza para expresar la energía molar, es decir, la energía por unidad de sustancia química medida en moles. Dado que la energía se mide en julios (J), que equivalen a newton-metro (N·m) o kilogramo por metro cuadrado por segundo al cuadrado (kg·m²·s⁻²), y la cantidad de materia se mide en moles (mol), una unidad básica del SI, la expresión del julio por mol en unidades básicas del SI sería kg·m²·s⁻²·mol⁻¹.
Esta unidad se emplea comúnmente para cuantificar la energía involucrada en las reacciones químicas o en procesos donde la energía absorbida o cedida depende de la cantidad de materia, como en las transformaciones de fase (entalpía de vaporización o de fusión de una sustancia). Ejemplos claros son las entalpías de las reacciones químicas o la energía libre de Gibbs, las cuales se expresan en julios por mol.
La división por el número de moles facilita la comparación entre procesos que involucran diferentes cantidades de material y entre procesos similares que involucran distintos tipos de materiales. El significado específico de esta cantidad siempre depende del contexto y, particularmente en reacciones químicas, está ligado a la definición del 'mol' para un proceso particular, que puede ser arbitraria.
Dado que un mol equivale a 6.02214179 × 10²³ partículas (átomos, moléculas, iones, etc.), un julio por mol es igual a 1 julio dividido por 6.02214179 × 10²³ partículas, lo que resulta en 1.66054 × 10⁻²⁴ julios por partícula. Esta cantidad de energía es extremadamente pequeña y difícil de manejar en estudios o cálculos a nivel atómico, por lo que frecuentemente se recurre a unidades del sistema atómico.
Para la energía por partícula se utiliza el electronvoltio (eV), que representa la energía cinética adquirida por un electrón al atravesar una diferencia de potencial de 1 voltio (V) en el vacío. Por conveniencia y debido al rango de magnitudes involucradas, estas cantidades casi siempre se reportan en kJ·mol⁻¹ (kilojulios por mol) en lugar de J·mol⁻¹.
Por ejemplo, los calores de fusión y vaporización suelen ser del orden de 10 kJ·mol⁻¹, las energías de enlace del orden de 100 kJ·mol⁻¹, y las energías de ionización del orden de 1000 kJ·mol⁻¹. Específicamente, 1 kJ·mol⁻¹ equivale a 0.239 kcal·mol⁻¹ o 1.04 × 10⁻² eV por partícula. A temperatura ambiente (25°C, 77°F, o 298.15 K), 1 kJ·mol⁻¹ es igual a 0.4034 kcal·mol⁻¹.
Calor Específico del Agua y su Relevancia
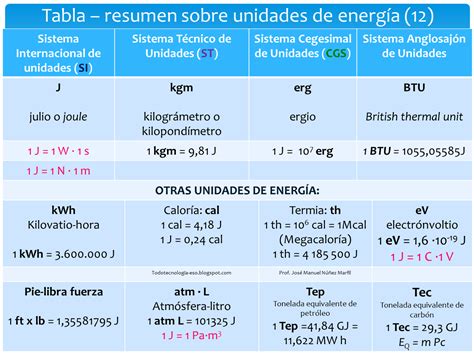
El CP del agua (calor específico del agua) es una de las propiedades más significativas de esta sustancia. Se refiere a la capacidad calorífica del agua a diferentes temperaturas, también conocida como calor específico o capacidad térmica específica. Es una propiedad de las sustancias que indica la cantidad de energía necesaria para aumentar su temperatura.
El agua posee una capacidad calorífica específica muy alta, lo que significa que requiere una considerable cantidad de calor para elevar su temperatura. Por ejemplo, para que 1 kilogramo de agua aumente su temperatura en 1°C, se necesitan 4.184 J (julios). Para comprender el CP del agua, es fundamental entender el concepto de calor específico en general, el cual se basa en la capacidad calorífica, una propiedad extensiva de la materia.
La capacidad calorífica del agua a diferentes temperaturas se mide específicamente en J/(K·kg). En condiciones normales, 1 kilogramo de agua requiere 1 kilocaloría para que su temperatura aumente 1°C, es decir, 1 kcal/°C·kg. El CP del agua es superior al de cualquier otra sustancia común.
Un ejemplo ilustrativo: si un cubo de agua se expone al sol en verano, se calentará, pero no lo suficiente como para cocinar un alimento. Este alto calor específico del agua se debe a los puentes de hidrógeno.
La elevada capacidad calorífica del agua es una propiedad crucial que contribuye significativamente a la regulación meteorológica y climática. Al variar su temperatura, el agua absorbe o libera grandes cantidades de calor. Esta propiedad es vital para los seres vivos, ya que el agua modera los cambios bruscos de la temperatura corporal al actuar como un regulador térmico. Por ejemplo, el alto calor específico del agua permite que un lago mantenga una temperatura media estable entre el día y la noche. El CP del agua es un factor meteorológico y ambiental fundamental para las zonas costeras e insulares.
Kilocalorías (kcal): Energía en la Nutrición
Las kilocalorías (kcal) son una unidad de medida energética ampliamente conocida, especialmente en el contexto de la nutrición. Los productos alimenticios envasados, frescos o no, suelen incluir información nutricional que detalla la cantidad de kilocalorías que aportan, ya sea por ración o por una cantidad específica de masa (como 100 mg).
Una kilocaloría es una unidad de medida que cuantifica la cantidad de energía que un alimento proporciona al cuerpo humano. Cuantas más kilocalorías contenga un alimento, mayor será la energía que el organismo puede almacenar. Las necesidades energéticas varían individualmente en función de la estatura, masa corporal, complexión y nivel de actividad física de cada persona.
El cuerpo humano consume calorías constantemente. Una de las funciones básicas de las kilocalorías es mantener la temperatura corporal constante, permitiendo que el cuerpo mantenga una temperatura promedio incluso en climas fríos. Además, todas las funciones vitales del cuerpo, como la respiración, el latido del corazón y el funcionamiento de los órganos, consumen la energía aportada por esta unidad calórica, la cual se obtiene exclusivamente de los alimentos. Es importante destacar que el agua, a pesar de su importancia para la vida, no contiene kilocalorías.
Necesidades Calóricas Diarias
El consumo de energía depende de cada persona. No obstante, existen patrones estándar para calcular la energía necesaria. El aporte diario recomendado de kilocalorías para un varón adulto con actividad física suave se sitúa entre 2.500 y 3.000 kcal, mientras que para mujeres con actividad física ligera oscila entre 1.800 y 2.200 kcal diarias.
Estas estimaciones se basan en el físico y el ritmo de vida de cada individuo; no es lo mismo una persona con un estilo de vida activo que una sedentaria. Existen tablas detalladas que ofrecen estimaciones precisas del aporte calórico adecuado para cada caso. Por regla general, las necesidades de kilocalorías disminuyen con la edad, mientras que aumentan durante las etapas de crecimiento, embarazo y lactancia.
No es necesario calcular obsesivamente las kilocalorías diarias. Lo fundamental es comprender qué son las kilocalorías y cómo la energía de los alimentos se distribuye en el cuerpo, así como la importancia de estas unidades calóricas para el desarrollo fisiológico.
Definición y Uso de la Kilocaloría
La kilocaloría, comúnmente abreviada como kcal, es una unidad de medida energética esencial en nutrición y medicina. Se utiliza para cuantificar la energía que los alimentos proporcionan al cuerpo humano y el gasto energético que este realiza.
Una kilocaloría equivale a la energía necesaria para aumentar en un grado Celsius la temperatura de un kilogramo de agua. Aunque en el lenguaje cotidiano se hable de "calorías", en realidad se hace referencia a kilocalorías, ya que 1 kcal equivale a 1,000 calorías (calorías termoquímicas, donde 1 cal = 4.184 J).
Las kilocalorías representan la energía que los alimentos aportan al cuerpo, siendo fundamentales para el correcto funcionamiento de los órganos, el mantenimiento del metabolismo basal y la realización de actividades diarias. El requerimiento diario de kilocalorías varía según la persona. Los alimentos ricos en grasas saludables, como el aceite de oliva, los frutos secos y el aguacate, poseen una alta densidad calórica. El consumo calórico necesario se calcula considerando el metabolismo basal, el nivel de actividad física y el gasto energético adicional por condiciones específicas.
CALORÍAS Y BALANCE ENERGÉTICO ¡¡¡NUEVO VIDEO!!! Fiteligente
tags: #significado #kcal #mol