La obesidad es una enfermedad crónica, sistémica, multiorgánica, metabólica e inflamatoria de alta prevalencia en el mundo. Se ha observado un incremento significativo en su incidencia, pasando del 7 % en 1980 al 12,5 % en 2015 en la población adulta. Diversos factores de riesgo contribuyen a esta condición, incluyendo un alto consumo energético, sedentarismo, predisposición genética, consumo frecuente de comidas fuera del hogar, ingesta de bebidas azucaradas y snacks, así como de alimentos ricos en grasas y azúcares.
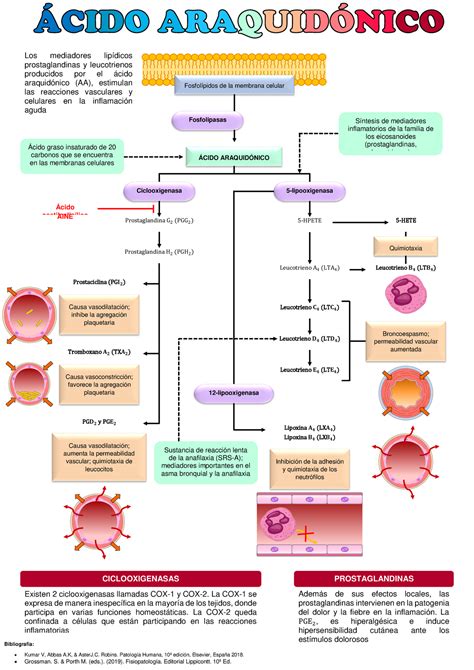
El ácido araquidónico (ARA), un ácido graso poliinsaturado de la serie omega-6, juega un papel fundamental en la biología de los mamíferos. Bioquímicamente, el ARA es sintetizado en el cuerpo a partir del ácido linoleico, un ácido graso esencial obtenido de la dieta. El ARA es un componente crítico de las membranas neuronales, formando parte de la fosfatidilcolina y otros fosfolípidos que no solo estructuran y protegen las neuronas, sino que también participan en la señalización celular y la regulación de la neurotransmisión.
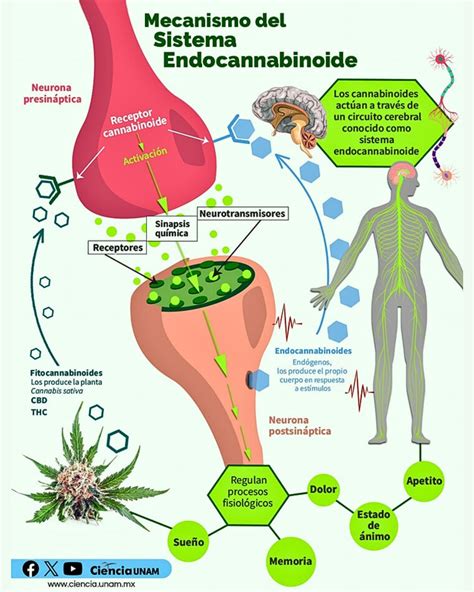
El Sistema Endocannabinoide y la Adicción a la Comida
El Omega 6 es precursor del ácido araquidónico (ARA), molécula base para la producción endógena de los endocannabinoides, que actúan como agonistas o ligandos activadores de los receptores cannabinoides tipo 1. La unión entre estos ligandos y sus receptores activa el sistema endocannabinoide (SEC), el cual se relaciona con una pérdida de memoria a corto plazo, ataxia (pérdida de coordinación motora), toma de decisiones deficientes y un efecto antinociceptivo (menor percepción del dolor), entre otros.
Cuando se activa el SEC, puede ocurrir un aumento en la síntesis de grelina a nivel gástrico, favoreciendo la liberación hipotalámica de neuropéptidos que promueven la ingesta. Adicionalmente, puede incrementarse la liberación de insulina en las células beta pancreáticas. La insulina, además de disminuir la liberación de neuropéptidos orexigénicos, puede ejercer una función a nivel del núcleo accumbens al estimular la liberación de dopamina en una respuesta indirecta.
Por otro lado, es crucial considerar el bajo consumo de alimentos fuente de ácido linolénico (ALA), cuyos derivados compiten con los derivados del ácido linoleico. Esta competencia reduce los niveles de estos ácidos grasos en el plasma sanguíneo y en los depósitos tisulares, y además, el cuerpo humano puede utilizarlos para producir cannabinoides antagonistas de los receptores CB1.
Estudio sobre la Correlación entre Ácido Araquidónico y Adicción a la Comida en Obesidad
Con el propósito de analizar la correlación entre el puntaje de adicción a la comida (evaluado mediante la escala mYFAS 2.0) y los niveles plasmáticos de ácido araquidónico en adultos con obesidad, se llevó a cabo un estudio que moduló la ingesta de alimentos fuente de ácidos grasos esenciales. El grupo de estudio se conformó por adultos que firmaron el consentimiento informado y cumplían con criterios de inclusión como presentar 2 o más criterios de adicción a la comida según la escala mYFAS 2.0, tener entre 18 y 35 años, un Índice de Masa Corporal (IMC) en rango de obesidad grado I y II, y un porcentaje de grasa corporal clasificado como obesidad.
Los participantes fueron divididos en dos grupos: A (n=8) y 1 (n=7). Cada grupo recibió dos intervenciones nutricionales: una intervención "A" (tratamiento experimental) y una intervención "B" (tratamiento estándar). La fase experimental tuvo una duración total de 9 semanas, con cada intervención y una fase de lavado de 21 días cada una, llevadas a cabo entre agosto y octubre de 2019.
Tratamiento Experimental y Restricciones Dietéticas
El tratamiento experimental se basó en principios nutricionales establecidos, con la adición de una restricción en el consumo de alimentos fuente de Omega 6. Se excluyeron aceites vegetales como girasol, soya, maíz, cártamo, canola, palma, coco y otros (con excepción del aceite de oliva, cuyo aporte de Omega 6 debía ser inferior al 10 % de su contenido). También se restringió el consumo de alimentos ultraprocesados, comidas rápidas, productos de panadería y alimentos preparados fuera de casa, debido a la dificultad para controlar el tipo de aceite utilizado en su preparación.
La intervención se realizó mediante un procedimiento estructurado, siguiendo un manual operativo diseñado para el estudio. La valoración de la composición corporal individual fue llevada a cabo por un nutricionista dietista, incluyendo mediciones de peso (kg) y talla (m) para el cálculo del IMC (kg/m²). La ingesta alimentaria se evaluó mediante el método del recordatorio global de 24 horas de pasos múltiples, aplicado en el día previo a la toma de datos y un día de fin de semana, utilizando atlas de alimentos como apoyo visual para minimizar sesgos en la estimación de porciones.
Recolección y Análisis de Muestras
Las muestras sanguíneas se obtuvieron de los participantes en ayuno. Posteriormente, fueron centrifugadas a 1000 rpm durante 10 minutos para obtener el plasma sanguíneo. Las muestras se etiquetaron y congelaron a -80°C por un período inferior a 60 días. Se realizó un manejo estadístico de variables no paramétricas, utilizando la prueba de Wilcoxon para análisis intragrupales, con un nivel de confianza del 90 %.
Resultados del Estudio
En cuanto a las características demográficas, el 60 % de los participantes de los grupos A y 1 correspondían a adultos jóvenes entre 18 y 23 años, y más del 65 % de la muestra fueron del sexo masculino.
Modulación de la Relación Omega-6/Omega-3 y Niveles de Ácido Araquidónico
Inicialmente, la relación Omega 6:3 en los participantes de ambos grupos presentó valores superiores a los recomendados (idealmente menor a 5:1). Sin embargo, tras recibir el tratamiento experimental, los participantes alcanzaron esta recomendación (evidenciado en T2 para el grupo A y T4 para el grupo 1). La línea base para las concentraciones plasmáticas de ácido araquidónico en los participantes de los grupos fue, en promedio, superior a 92 ng/dL.
Tras la exposición al tratamiento experimental, se observaron disminuciones significativas (con un nivel de confianza del 90 %) en los valores plasmáticos promedio de ácido araquidónico. Esto se evidenció en la comparación entre T1 y T2 en el grupo A (valor p de 0,012) y entre T3 y T4 para el grupo 1 (valor p de 0,091). Por el contrario, la exposición al tratamiento estándar se asoció a resultados mixtos sin diferencias significativas.
Impacto en la Adicción a la Comida y el Peso Corporal
Desde el inicio del estudio, los participantes mostraron descensos en los valores promedio del puntaje en la escala mYFAS 2.0 tras la exposición al tratamiento experimental, estándar y a la fase de lavado. Estos cambios no fueron estadísticamente significativos, a excepción de un pico de disminución en el grupo A (T2) tras el tratamiento experimental, que alcanzó significancia estadística con un intervalo de confianza del 90 %. En la fase final del estudio, los participantes obtuvieron los puntajes más bajos en la escala, con un 100 % en el grupo A y un 86 % en el grupo 1 clasificando como ausencia de adicción a la comida.
Los participantes del estudio presentaron un peso corporal promedio superior a 96 kg. Durante las 9 semanas de intervención, redujeron en promedio 4 kg, lo que corresponde aproximadamente al 3,6 % de su peso corporal inicial. Se observaron disminuciones significativas en el peso (nivel de confianza del 95 %) en la primera fase del estudio en ambos grupos. Durante la fase de lavado, ambos grupos experimentaron una disminución de peso sin diferencias significativas.
La exposición al tratamiento estándar se asoció a una disminución del peso corporal, respuesta esperada dada la naturaleza de la intervención nutricional para adultos con obesidad.
Correlación entre Ácido Araquidónico, Adicción a la Comida y Obesidad
La exposición de los grupos A y 1 al tratamiento estándar se asoció a una correlación negativa entre estas variables. Paralelamente, la asociación entre las concentraciones de ácido araquidónico y el resultado en la escala mYFAS fue directamente proporcional en los grupos tras recibir el tratamiento experimental: al disminuir una variable, la otra también presentaba este comportamiento.
Como análisis complementario, se examinó la relación entre las concentraciones de ácido araquidónico y cada criterio de adicción a la comida, cuyos resultados se detallan en la Tabla 3 (no incluida en este resumen).
El estudio de Kim et al. asocia un alto consumo de Omega 6 con un aumento en los niveles plasmáticos de ARA, mientras que el consumo de Omega 3 los disminuye. De forma simultánea, el aumento del consumo de Omega 3 en el grupo expuesto al tratamiento experimental pudo inducir un incremento en la síntesis de EPA y DHA, los cuales pueden reducir las concentraciones de ARA en plasma y membranas. Esta modulación negativa en la actividad del SEC, como resultado de la exposición al tratamiento experimental, podría estar asociada a los cambios observados en el puntaje de adicción a la comida, ya que se encontró una disminución significativa en esta escala en comparación con otras intervenciones.
Al disminuir la producción de 2-AG y AEA, se podría reducir la acción del sistema endocannabinoide sobre el núcleo accumbens, el córtex prefrontal y la amígdala, estructuras relacionadas con el circuito de recompensa, las vías dopaminérgicas mesolímbica y mesocortical, y alteraciones en la conducta alimentaria. Esto significa que se limitaría la hiperactividad dopaminérgica mediada por el SEC.
La correlación identificada entre el puntaje de la escala mYFAS 2.0 y las concentraciones plasmáticas de ARA fue mayor en los participantes de este estudio cuando su IMC era más elevado. Esto coincide con el estudio de Little et al., quienes encontraron un incremento en los niveles plasmáticos de AEA y 2-AG en personas con obesidad en comparación con personas con sobrepeso o peso adecuado, sugiriendo que la hiperactividad del SEC podría estar directamente relacionada con el exceso de peso.
La asociación entre la activación del SEC y la adicción a la comida está fuertemente ligada a la percepción placentera de los alimentos palatables y la actividad del SEC en el núcleo accumbens. Este efecto a largo plazo puede generar cambios neurobiológicos, incluyendo alteraciones en la transmisión dopaminérgica que afectan negativamente la densidad de receptores dopaminérgicos tipo 2 en el circuito de recompensa, modificando así la conducta alimentaria y manifestando los primeros signos de comportamientos adictivos.
🧁El CEREBRO induce HAMBRE o SACIEDAD, aprende CÓMO
Metabolismo de Ácidos Grasos y Pérdida de Peso
Cuando los participantes fueron expuestos a las intervenciones, el déficit energético promovido por los tratamientos nutricionales pudo estimular la movilización y el uso de ácidos grasos, disminuyendo sus reservas. Simultáneamente, el incremento en las concentraciones de DHEA y EPEA (derivados del Omega 3) promovido por el consumo de Omega 3 en el tratamiento experimental podría explicar la disminución del peso corporal. Esto se debería a la acción de estos cannabinoides a nivel hepático sobre el metabolismo de las grasas, incluyendo la reducción de la producción de enzimas lipogénicas como la ácido graso sintasa, lo cual coincide con los picos de pérdida de peso observados en los participantes que recibieron el tratamiento experimental.
Conclusiones Preliminares
La disminución del consumo de Omega 6 y el aumento del consumo de Omega 3 se asociaron a una reducción en el puntaje de la escala de adicción a la comida y en las concentraciones plasmáticas de ácido araquidónico en los participantes expuestos al tratamiento experimental. Se encontró una correlación directamente proporcional entre estas variables, que podría relacionarse con la producción de endocannabinoides a partir del ARA. Estas moléculas pueden interactuar con estructuras del sistema nervioso central vinculadas al circuito de recompensa y las vías dopaminérgicas mesolímbica y mesocortical.
El tratamiento estándar también se asoció a una disminución del peso corporal, una respuesta esperada, ya que corresponde a una intervención nutricional diseñada para adultos con obesidad.
Fuentes de Ácidos Grasos y sus Implicaciones
El ácido araquidónico (ARA) es un ácido graso poliinsaturado omega-6 crucial en la biología de los mamíferos. Es un componente de los fosfolípidos de las membranas neuronales y participa en la señalización celular. El ARA también influye en procesos reproductivos como la ovulación y la implantación, y está implicado en condiciones patológicas inflamatorias y autoinmunes.
Recientemente, se ha investigado el potencial de la suplementación con ARA para mejorar la respuesta anabólica al entrenamiento de fuerza. Un estudio (Mitchell et al., 2018) hipotetizó que el ARA podría aumentar la síntesis de proteínas musculares (MPS) vía activación de mTOR y potenciar la respuesta anabólica tardía mediante la modulación de la biogénesis ribosomal y la expansión de células satélite. Los resultados indicaron que, si bien la MPS y la activación de mTOR no difirieron entre el grupo ARA y placebo en las primeras 4 horas de recuperación, la biogénesis ribosomal aumentó a las 48 horas post-ejercicio solo en el grupo ARA. Las células satélite por fibra muscular también aumentaron a las 48 horas post-ejercicio sin diferencias entre grupos. En resumen, la suplementación con ARA no alteró la respuesta anabólica aguda al ejercicio de fuerza en hombres entrenados, pero estimuló la biogénesis ribosómica a las 48 horas post-ejercicio.
Es importante distinguir el ácido araquidónico del ácido araquídico, un ácido graso saturado de cadena muy larga (AGCCML). El ácido araquídico, presente en frutos secos y aceites, se ha asociado a un menor riesgo de enfermedades cardiovasculares (parada cardiaca súbita, insuficiencia cardiaca, enfermedad coronaria) y diabetes tipo 2. También se ha relacionado con la salud neurológica, siendo un componente del fosfatidilglucósido (PtdGlc), implicado en la señalización del sistema nervioso central y el desarrollo cerebral.
La dieta y otros factores del estilo de vida, como la ingesta total de grasas, el consumo de frutos secos y la actividad física, pueden influir positivamente en los niveles circulantes de AGCML, incluido el ácido araquídico, mejorando la salud cardiometabólica.
En cuanto al consumo de ácido araquidónico en la dieta, se señala que no es perjudicial si se mantiene una dieta reducida en Omega 6 de origen vegetal. El ARA se metaboliza en dos moléculas, una pro-inflamatoria y otra anti-inflamatoria, y estudios indican que la ingesta de 840 mg a 2.000 mg diarios durante 50 días no ha mostrado aumento de inflamación. El DHA (ácido graso omega-3) y el ácido araquidónico son componentes esenciales del cerebro y la retina. Altos niveles de Omega 6 y ARA se han relacionado con una menor pérdida ósea en mujeres, pero solo cuando consumían altos niveles de Omega 3. La carne y el huevo, que contienen ácido araquidónico, son fuentes esenciales de nutrientes.
tags: #acido #araquidonico #paleo