El ácido sulfúrico, cuya fórmula química es H2SO4, es una molécula esencial compuesta por átomos de hidrógeno, azufre y oxígeno. Específicamente, se forma por la unión de dos átomos de hidrógeno, uno de azufre y cuatro de oxígeno, resultando en un compuesto altamente ácido y corrosivo. Su importancia es tal que el nivel de desarrollo industrial de un país a menudo se mide por su consumo de ácido sulfúrico, siendo uno de los compuestos químicos más producidos a nivel mundial.
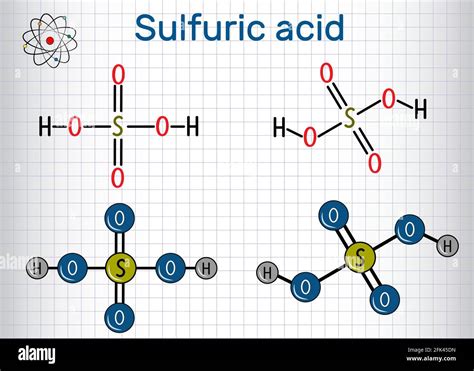
¿Qué es el Ácido Sulfúrico?
El ácido sulfúrico se presenta como un líquido aceitoso, viscoso, incoloro y sin olor. Históricamente, se le conocía como aceite de vitriolo, debido a que se obtenía a partir de minerales que contenían azufre, conocidos como vitriolos. En la actualidad, el ácido sulfúrico se produce industrialmente en diversos grados de pureza, que van desde casi puro (98%) hasta soluciones muy diluidas. Su manipulación, especialmente en concentraciones altas, requiere precauciones significativas debido a su naturaleza corrosiva y al potencial de reacciones violentas, como salpicaduras y emisión de vapores, al mezclarse incorrectamente con agua.
La molécula de ácido sulfúrico presenta una estructura piramidal, con el átomo de azufre en el centro y los átomos de oxígeno en los vértices. Los átomos de hidrógeno se enlazan a los átomos de oxígeno que no forman enlaces dobles con el azufre. Dependiendo de la disolución, estos hidrógenos pueden disociarse, lo que confiere al ácido sus propiedades ácidas.
Usos Industriales del Ácido Sulfúrico
El ácido sulfúrico es un componente fundamental en una amplia gama de procesos industriales y reacciones químicas, siendo indispensable para la producción de numerosos productos. Sus aplicaciones más destacadas incluyen:
- Fertilizantes: Es un componente clave en la fabricación de fertilizantes, especialmente en la producción de ácido fosfórico y superfosfatos de cal, que facilitan la absorción de fosfato por las plantas. También se utiliza en la producción de sulfato de amonio.
- Industria Química: Sirve como materia prima para la síntesis de otros ácidos importantes, como el ácido nítrico y el ácido clorhídrico, y participa en la producción de una gran variedad de productos químicos industriales.
- Minería y Metalurgia: Se emplea en la extracción de metales y en el tratamiento de superficies metálicas.
- Industria Petroquímica: Actúa como catalizador en el refinado del petróleo crudo y en otros procesos de la industria petroquímica.
- Baterías: Las baterías de plomo-ácido, comunes en vehículos, contienen soluciones diluidas de ácido sulfúrico que permiten la conducción eléctrica entre los electrodos.
- Detergentes y Cosméticos: Es un ingrediente fundamental en la producción de detergentes (especialmente aquellos que contienen "sulfato" en su nombre) y en la manufactura de pigmentos y otras moléculas utilizadas en cosméticos.
- Industria Farmacéutica: Interviene en la producción de diversos medicamentos.
- Industria Textil y Papelera: Se utiliza en la fabricación de textiles y papel.
Propiedades y Peligros del Ácido Sulfúrico
El ácido sulfúrico es conocido por su alta reactividad y sus peligrosas propiedades corrosivas. Su afinidad por el agua lo convierte en un potente agente deshidratante, capaz de extraer agua de materiales orgánicos, incluyendo los tejidos humanos. Esta reacción con el agua libera una cantidad considerable de calor, lo que puede generar incendios y quemaduras si no se maneja con control.
Las reacciones del ácido sulfúrico con las moléculas orgánicas de nuestro organismo son irreversibles y alteran su función normal. Por ejemplo, las proteínas pueden desnaturalizarse (cambiar su estructura tridimensional) y las grasas pueden saponificarse (convertirse en jabón). El resultado es una transformación profunda de los tejidos afectados.
Los efectos del ácido sulfúrico en los tejidos humanos dependen de su concentración, la zona expuesta y el tiempo de contacto. Las formas diluidas pueden causar irritación y lesiones leves si no se retiran rápidamente, mientras que las formas concentradas pueden provocar úlceras y daño permanente. La inhalación de sus vapores puede causar irritación en las vías respiratorias, erosión dental y estomatitis. El contacto con los ojos puede resultar en daño permanente y ceguera.
¿Qué son las proteínas? | Biología Desde Cero
Precauciones al Manipular Ácido Sulfúrico
Debido a su peligrosidad, la manipulación del ácido sulfúrico requiere extremas precauciones:
- Dilución: Siempre se debe añadir el ácido concentrado al agua lentamente, y nunca al revés. La adición de agua al ácido puede generar una reacción exotérmica violenta, provocando ebullición y salpicaduras peligrosas.
- Protección Personal: Es indispensable el uso de equipo de protección adecuado, incluyendo guantes resistentes a químicos, gafas de seguridad o pantalla facial, y ropa protectora.
- Primeros Auxilios: En caso de contacto con la piel, no se debe lavar inmediatamente con agua. Primero, se debe neutralizar el ácido con jabón o una solución de agua de cal, y luego enjuagar abundantemente con agua. La ropa contaminada debe retirarse de inmediato.
- Inhalación: Se debe evitar respirar los vapores. Si ocurre, trasladarse a un área con aire fresco y buscar atención médica.
- Ingestión: La ingestión es extremadamente peligrosa y requiere atención médica inmediata.
Investigación y Descubrimientos Relacionados con el Ácido Sulfúrico
La historia del ácido sulfúrico se remonta a la antigüedad, con su estudio atribuido a alquimistas como Jabir ibn Hayyan en el siglo VII y Ibn Zakariya al-Razi en el siglo IX. Los alquimistas europeos lo conocían como "aceite de vitriolo" y lo consideraban una sustancia de gran importancia, incluso buscando su uso como piedra filosofal.
Johann Rudolph Glauber, en el siglo XVII, mejoró su producción. Posteriormente, John Roebuck, en 1746, introdujo el uso de cámaras de plomo para su fabricación a gran escala, aunque con concentraciones más bajas. Mejoras posteriores por Louis Joseph Gay-Lussac y John Glover permitieron obtener concentraciones más altas. El desarrollo del proceso de contacto en 1831 por Peregrine Phillips revolucionó la producción, permitiendo obtener ácido sulfúrico concentrado de manera más económica.
El ácido sulfúrico concentrado comercialmente suele tener una pureza del 98%, siendo esta forma más estable para el almacenamiento. Existen diversas concentraciones y grados de pureza (técnico, USP) para satisfacer distintas aplicaciones industriales y farmacéuticas.
Investigaciones recientes han revelado la existencia de microorganismos capaces de sobrevivir en ambientes extremadamente ácidos, como el Ferroplasma acidiphilum. Descubierto por investigadores del CSIC, este microorganismo extrae energía del hierro y su hábitat en vetas de pirita (compuesto de hierro y azufre) sugiere que estos elementos pudieron haber sido catalizadores para el origen de la vida en la Tierra. El estudio de estos organismos extremófilos abre nuevas vías para comprender la evolución de la vida y la bioquímica en condiciones extremas.

El Ácido Sulfúrico en el Contexto Humano y Ecológico
Aunque el ácido sulfúrico tiene usos domésticos limitados debido a su peligrosidad, sus propiedades reactivas lo hacen útil en algunos productos de limpieza, como limpiadores de desagües. Sin embargo, su manipulación y almacenamiento requieren un cuidado extremo.
La producción y uso de ácido sulfúrico tienen implicaciones ambientales, particularmente en la formación de lluvia ácida. El dióxido de azufre (SO2), liberado por la quema de combustibles fósiles y procesos industriales, puede oxidarse en la atmósfera para formar trióxido de azufre (SO3), que luego reacciona con el agua para producir ácido sulfúrico. Este ácido se disuelve en las gotas de lluvia, disminuyendo el pH de la precipitación y afectando ecosistemas acuáticos y terrestres, así como edificaciones.
En el ámbito de la salud, la exposición ocupacional a vapores de ácidos inorgánicos fuertes, incluido el ácido sulfúrico, ha sido asociada con un aumento en la tasa de cáncer de laringe en estudios limitados, especialmente en individuos fumadores y expuestos a múltiples químicos. Sin embargo, no hay evidencia concluyente que vincule la exposición exclusiva al ácido sulfúrico con la carcinogenicidad en humanos.
Los niños pueden estar expuestos al ácido sulfúrico a través del contacto con productos de limpieza domésticos o baterías de automóviles. La curiosidad infantil y el almacenamiento inadecuado de estos productos aumentan el riesgo de ingestión accidental o contacto con la piel y los ojos. Estudios sugieren que los niños podrían ser más susceptibles a los efectos de la inhalación de ácido sulfúrico debido a sus vías respiratorias más estrechas y una mayor tasa de inhalación de aire por kilogramo de peso corporal.
El ácido sulfúrico no se absorbe ni se distribuye por el cuerpo, y no atraviesa la placenta ni pasa a la leche materna. Sus efectos son primariamente locales, causando daño directo en los tejidos con los que entra en contacto.
tags: #acido #sulfurico #metabolismo