Un equipo de científicos argentinos ha logrado un avance significativo en la investigación neurológica del país al crear por primera vez en laboratorio neuronas humanas a partir de células de la piel de un paciente con la enfermedad de Alzheimer familiar o hereditaria. Este modelo celular innovador permite estudiar los mecanismos de la neurodegeneración con una precisión sin precedentes y abre la puerta a la evaluación de futuras terapias personalizadas.
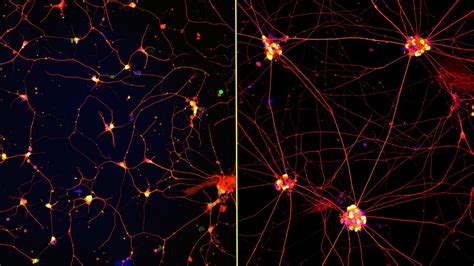
Un Nuevo Modelo para la Investigación del Alzheimer
El estudio, fruto de la colaboración entre el Centro de Investigación en Medicina Traslacional Severo R. Amuchástegui (CIMETSA) de Córdoba-CONICET, la Fundación Instituto Leloir y la Facultad de Medicina de la UBA, fue publicado en la prestigiosa revista científica Scientific Reports. El objetivo principal fue profundizar en las bases moleculares de la enfermedad utilizando un modelo propio, derivado de un paciente argentino portador de una mutación genética específica.
Luis Ignacio Brusco, decano de la Facultad de Ciencias Médicas de la UBA y uno de los participantes clave en el estudio, subrayó el impacto de este avance: "Poder trabajar con neuronas obtenidas a partir de células de un paciente con Alzheimer hereditario permite observar en detalle cómo se desencadenan los daños en el cerebro y, a futuro, pensar en tratamientos hechos a medida para cada persona". Brusco destacó que este logro redefine el paradigma de la investigación local sobre esta enfermedad neurodegenerativa.
Reprogramación Celular y Observación Directa del Daño
Para el desarrollo de este modelo, los investigadores emplearon una técnica avanzada de reprogramación celular. Mediante este método, las células de la piel del paciente fueron transformadas en células madre pluripotentes inducidas (iPSC). Estas células madre tienen la notable capacidad de diferenciarse en cualquier tipo de célula del cuerpo, y en este caso particular, fueron guiadas para convertirse en neuronas corticales humanas. Este proceso permitió al equipo observar directamente los mecanismos de daño celular en un modelo auténtico y personalizado.
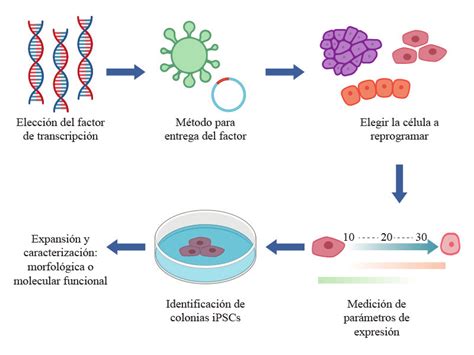
Disfunción Celular y el Papel del Calcio
La investigación se centró específicamente en un paciente portador de la mutación M146L en el gen Presenilina-1, una alteración genética fuertemente vinculada al Alzheimer familiar. Al analizar las neuronas generadas en el laboratorio, los científicos observaron de manera concluyente la existencia de alteraciones significativas en la regulación del calcio intracelular y una notable disfunción en las mitocondrias, las organelas celulares responsables de la producción de energía.
Estos hallazgos sugieren una conexión crucial entre el daño neuronal característico del Alzheimer y la disfunción en la homeostasis del calcio y el metabolismo mitocondrial, y plantean que estos procesos podrían ser tan o más importantes que la acumulación de la proteína beta amiloide, la hipótesis tradicionalmente aceptada. Laura Morelli, investigadora de la Fundación Instituto Leloir, explicó que el nuevo modelo proporciona una perspectiva más fiel de la patología: "Estas neuronas creadas en el laboratorio reflejan mejor la fisiología del cerebro y las alteraciones específicas del paciente, lo que facilita el estudio de la patología y el eventual desarrollo de terapias más precisas".
El análisis detallado reveló que las neuronas portadoras de la mutación exhiben una dinámica anómala del calcio, un funcionamiento mitocondrial deficiente y una producción incrementada de especies reactivas de oxígeno (ROS). Esta sobreproducción de ROS genera procesos inflamatorios crónicos en el tejido neuronal. Carlos Wilson, primer autor del artículo, señaló que el "estado de alto metabolismo" de estas neuronas podría acelerar significativamente la muerte celular, incluso antes de que las células agoten sus reservas de energía.
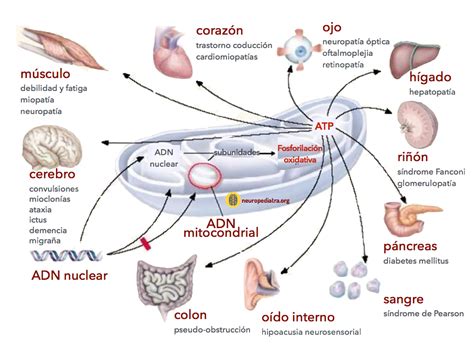
Hacia la Medicina de Precisión en el Tratamiento del Alzheimer
Aunque la forma familiar del Alzheimer representa una minoría (menos del 1%) de los casos totales, el estudio de sus mecanismos subyacentes es de vital importancia. La relación causa-efecto en esta variante hereditaria es considerablemente más directa, lo que simplifica el análisis de los procesos patológicos y la identificación de posibles dianas terapéuticas. Además, la disfunción mitocondrial y el déficit energético cerebral son características compartidas con el Alzheimer esporádico, la forma más común de la enfermedad, lo que amplía la relevancia clínica de estos hallazgos.
La relevancia clínica de este avance radica en la apertura de una nueva vía para la medicina de precisión. El modelo celular desarrollado permite analizar los procesos patológicos directamente en el tejido afectado, una estrategia que hasta ahora no era factible para este tipo de enfermedades neurodegenerativas en Argentina. El equipo de investigación, bajo la coordinación de Alfredo Cáceres, Laura Morelli y Luis Ignacio Brusco, continuará profundizando en la caracterización de las rutas moleculares alteradas. Asimismo, planean evaluar la eficacia de diversos fármacos sobre las disfunciones detectadas y expandir el sistema para incluir a más pacientes y analizar otras mutaciones genéticas asociadas al Alzheimer.
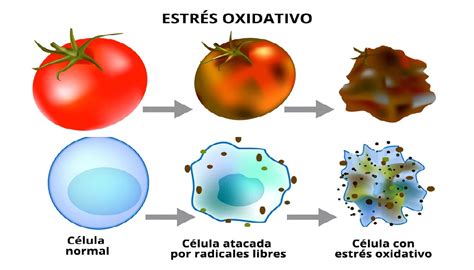
Estrés Oxidativo: Un Actor Clave en Diversos Procesos Celulares
Las células vivas realizan una serie de funciones esenciales para el mantenimiento fisiológico y metabólico del organismo humano. Durante las diversas reacciones metabólicas, se generan subproductos, entre los cuales se encuentran las especies reactivas de oxígeno (ROS). Estas son moléculas pequeñas y altamente reactivas, producidas como subproductos del metabolismo celular en organismos aeróbicos, y se encuentran en distintas partes de la célula, como las mitocondrias, el retículo endoplasmático y el citosol.
El "desequilibrio" electrónico de las ROS las hace reaccionar fácilmente con otras moléculas celulares. Afortunadamente, el cuerpo posee sistemas de defensa celular compuestos por moléculas antioxidantes que neutralizan estas ROS. El estrés oxidativo ocurre cuando hay un exceso de ROS en el cuerpo y una cantidad insuficiente de antioxidantes para eliminarlas. El estrés oxidativo prolongado se ha asociado con diversos síntomas, como dolor muscular, problemas de memoria, fatiga y cansancio.
Relación del Estrés Oxidativo con Enfermedades
El estrés oxidativo está vinculado a una amplia gama de enfermedades y trastornos. Es importante destacar que los síntomas específicos varían según la persona y la condición médica subyacente. Además, muchos de los signos clínicos asociados son inespecíficos y pueden solaparse con los de otras condiciones, por lo que se recomienda consultar a un médico ante cualquier síntoma preocupante.
- Cáncer: La presencia excesiva de ROS puede causar daño en el ADN, lo que favorece la aparición de mutaciones, cambios en la transcripción y problemas en la división celular, mecanismos asociados al desarrollo del cáncer.
- Enfermedades cardiovasculares: El estrés oxidativo promueve la formación de placas en las arterias, un proceso conocido como aterosclerosis.
- Enfermedades neurodegenerativas: Se ha observado que los niveles de ROS y el estrés oxidativo aumentan con la edad, contribuyendo a la degeneración neuronal en enfermedades como el Alzheimer.
Diagnóstico y Manejo del Estrés Oxidativo
El diagnóstico directo del estrés oxidativo en humanos puede ser complejo debido a la falta de un marcador específico y estandarizado. La medición de ROS en muestras de sangre es un método emergente que puede ser útil. Otros estudios, como la evaluación de niveles de antioxidantes, pruebas de estrés oxidativo inducido y marcadores de inflamación, también pueden ayudar a dilucidar este estado fisiológico alterado.
Dado que las ROS son parte del metabolismo normal, es prácticamente imposible evitar su exposición. Sin embargo, se pueden adoptar estrategias para mantener un equilibrio saludable:
- Dieta rica en antioxidantes: Consumir una variedad de frutas y verduras (5 porciones diarias), frutos secos (almendras, nueces), ajo, jengibre, cúrcuma y té verde.
- Granos enteros: Incluir en la dieta quinoa, arroz integral, cebada y avena, que son fuentes de antioxidantes como la vitamina E, selenio y polifenoles.
El estrés oxidativo es un estado alterado que requiere atención médica, ya que su asociación con diversas enfermedades a largo plazo subraya la importancia de su manejo y prevención.
El Rol del Eritrocito en el Metabolismo del Oxígeno y la Fisiología del Ejercicio
Un estudio reciente cuestiona el dogma clásico de la fisiología del ejercicio que considera al eritrocito (glóbulo rojo) como un mero transportador pasivo de oxígeno. Tradicionalmente, la capacidad de transporte de oxígeno se ha asociado casi exclusivamente a variables cuantitativas como el número de eritrocitos o la concentración de hemoglobina. Sin embargo, este artículo propone un cambio conceptual relevante: los eritrocitos poseen un metabolismo glucolítico y redox activo que podría modular dinámicamente la cinética del oxígeno, influyendo directamente en la fisiología del ejercicio.
Metabolismo Activo del Eritrocito
Desde un punto de vista bioquímico, los eritrocitos dependen exclusivamente de la glucólisis para la producción de ATP, lo que los convierte en un modelo único para estudiar la relación entre metabolismo energético y función celular. Este metabolismo no solo mantiene la viabilidad celular, sino que regula propiedades clave como la afinidad de la hemoglobina por el oxígeno, principalmente a través de metabolitos como el 2,3-bisfosfoglicerato (2,3-BPG). Además, el estado redox del eritrocito, mediado por sistemas como el glutatión y la vía de las pentosas fosfato, es esencial para preservar tanto la estructura celular como la funcionalidad de la hemoglobina.
El estrés oxidativo, frecuente durante el ejercicio, puede alterar profundamente estos sistemas. La oxidación de proteínas y lípidos, así como la depleción de antioxidantes, no solo compromete la eficiencia metabólica del eritrocito, sino también su deformabilidad, un factor crítico para atravesar los capilares musculares. A pesar de esta base teórica, existe una laguna en la investigación: la falta de estudios integradores que analicen de forma directa el papel funcional del metabolismo eritrocitario en la oxigenación muscular durante el ejercicio.
Adaptación Metabólica y Estrés Oxidativo
Uno de los hallazgos más relevantes del estudio es que el flujo glucolítico eritrocitario aumenta de forma marcada durante el ejercicio agudo. Este incremento representa una adaptación metabólica destinada a satisfacer las demandas energéticas y redox del entorno fisiológico, demostrando que el eritrocito es una célula capaz de ajustar su metabolismo en respuesta al estrés fisiológico. Esto implica que la capacidad de transporte de oxígeno no depende únicamente de la cantidad de hemoglobina, sino también de la capacidad metabólica del eritrocito para modular su función.
El estrés oxidativo, sin embargo, altera este comportamiento dinámico. Bajo condiciones de estrés oxidativo inducido, el aumento del flujo glucolítico es significativamente menor. Los autores interpretan esto como una pérdida de control metabólico, posiblemente mediada por daño oxidativo en enzimas, transportadores de glucosa o sistemas reguladores. Los datos sugieren una reprogramación metabólica hacia la vía de las pentosas fosfato, priorizando la producción de NADPH para defensa antioxidante a expensas de la producción de ATP y 2,3-BPG. Este cambio, si bien protege frente al daño oxidativo, reduce la eficiencia energética y la capacidad de modular la afinidad de la hemoglobina por el oxígeno.
Influencia en la Oxigenación Muscular y el Rendimiento
El estudio establece una conexión funcional entre el metabolismo eritrocitario y el rendimiento deportivo. Se demuestra que el estrés oxidativo eritrocitario se asocia con una reducción de la oxigenación muscular y del VO₂peak (consumo máximo de oxígeno), incluso en músculos no directamente afectados por el estrés. Los mecanismos propuestos incluyen la disminución de la deformabilidad eritrocitaria, lo que dificulta el flujo capilar y la entrega de oxígeno; alteraciones en el 2,3-BPG y la curva de disociación de la hemoglobina, modificando la liberación de oxígeno; y un déficit energético intracelular que compromete procesos mecánicos y de transporte.
El análisis computacional refuerza esta idea al mostrar que, en condiciones de estrés oxidativo, el eritrocito opera por debajo de su capacidad bioenergética teórica. Sin embargo, los autores reconocen limitaciones, como el efecto relativamente pequeño observado sobre el rendimiento (~4% en VO₂peak) y la posible influencia de otros factores no medidos.
Valoración Crítica y Conclusiones
Este trabajo posee un elevado valor conceptual al desplazar el foco de una visión cuantitativa del transporte de oxígeno a una visión cualitativa y metabólica del eritrocito. Introduce al eritrocito como un posible modulador activo de la fatiga, abriendo nuevas líneas de investigación. No obstante, se deben considerar varias limitaciones, como el tamaño muestral reducido (n=20) y una población homogénea (hombres jóvenes), lo que limita la generalización de los resultados. El diseño experimental es indirecto, infiriendo el efecto del eritrocito sobre el músculo, y hay una falta de medición de variables clave como la deformabilidad eritrocitaria o el flujo microvascular real.
En conjunto, el estudio aporta evidencia convincente de que el eritrocito debe ser considerado un actor metabólico activo en la fisiología del ejercicio, con implicaciones significativas para la comprensión del rendimiento y la fatiga.
Biología: El oxígeno y la respiración
tags: #alteraciones #celulares #metabolismo #oxigeno