La cirugía y el trauma desencadenan respuestas fisiológicas complejas en el organismo, caracterizadas por una acelerada pérdida de proteína muscular, un incremento en la oxidación de aminoácidos y una disminución de la síntesis proteica general. Estas manifestaciones, conocidas globalmente como respuestas de fase aguda, son variables y dependen del estado nutricional del paciente, la naturaleza del proceso subyacente y el tipo de anestesia empleada.
Los Dres. Franco Carli y Thomas Schricker, del Departamento de Anestesia de la Universidad McGill, han destacado en su editorial la modulación de la respuesta catabólica frente al acto quirúrgico. Tradicionalmente, se atribuía esta respuesta a un estímulo de hormonas catabólicas como las catecolaminas, el cortisol y el glucagón, junto con una reducción de hormonas anabólicas como la insulina. Sin embargo, investigaciones más recientes han identificado el papel de sistemas en cascada, como la vía del ácido araquidónico, el sistema del complemento y las citoquinas, que actúan como elementos inmunosupresores y catabólicos posquirúrgicos.
Las pérdidas de nitrógeno pueden ser significativas, oscilando entre 40 g en cirugías abdominales electivas y hasta 300 g en pacientes con quemaduras graves. Para ilustrar, la pérdida de 50 g durante una colecistectomía convencional puede equivaler a una merma de 1500 g de tejido magro. En situaciones donde la oxidación y la degradación proteica ocurren simultáneamente, el balance nitrogenado deja de ser un marcador adecuado de las alteraciones del metabolismo proteico.
Aunque las respuestas de fase aguda son un fenómeno adaptativo del organismo a diversas agresiones, su perpetuación en el posoperatorio puede prolongar la convalecencia, retrasar la cicatrización de heridas y aumentar la predisposición a infecciones. Para atenuar estas alteraciones metabólicas, se han explorado diversas estrategias, incluyendo técnicas específicas de analgesia.
Estrategias Analgésicas y su Impacto Metabólico
El uso de analgésicos como la morfina o el fentanilo ha demostrado su capacidad para suprimir la mayoría de las respuestas endocrinas y metabólicas asociadas a la cirugía, lo que indirectamente contribuye a reducir las pérdidas de nitrógeno.
La clonidina, utilizada como premedicación por sus efectos sedativos, ansiolíticos y analgésicos, reduce la actividad simpaticoadrenal, los niveles de cortisol plasmático y la excreción de nitrógeno. No obstante, su efecto sobre las células β pancreáticas, dependiente de la dosis, puede inhibir la secreción de insulina y causar hiperglucemia.
La analgesia epidural ha demostrado ser eficaz en prevenir la degradación de proteínas y la oxidación de aminoácidos en el posoperatorio, siempre que el paciente reciba un adecuado soporte nutricional. Más allá de sus efectos metabólicos directos, al facilitar una movilización más rápida del paciente, la analgesia epidural previene la atrofia muscular, ejerciendo así una acción anticatabólica.
En cuanto a las técnicas quirúrgicas, la cirugía laparoscópica genera una respuesta de fase aguda menos pronunciada en comparación con los procedimientos convencionales.
Nutrición Perioperatoria y Controversias
Los ayunos preoperatorios prolongados, necesarios en intervenciones intestinales, así como la infusión de glucosa y aminoácidos, continúan siendo temas de debate. Por otro lado, el apoyo nutricional perioperatorio, de tipo hipercalórico e hiperproteico, es objeto de análisis por sus posibles efectos adversos, como la hiperglucemia, que puede prolongar la necesidad de asistencia respiratoria, afectar la capacidad fagocítica de los leucocitos polimorfonucleares y disfuncionar el sistema del complemento. Además, el uso de accesos venosos centrales para la nutrición parenteral incrementa el riesgo de infecciones.
Es crucial determinar si el candidato a recibir apoyo nutricional hipercalórico e hiperproteico se encuentra en estado eutrófico o desnutrido, ya que solo en estos casos los beneficios potenciales superan los riesgos asociados a la alimentación artificial. La glutamina se destaca como un nutriente específico con resultados prometedores en la reversión de las consecuencias del catabolismo.
Agentes Anabólicos y Futuras Direcciones
Ante los resultados a menudo limitados del aporte de nutrientes y calorías, se recurre a agentes anabólicos. La insulina, administrada en infusión continua con glucosa, ha mostrado reducir la pérdida proteica, aunque el uso de altas cantidades de carbohidratos puede derivar en infiltración hepática y estimular la formación de dióxido de carbono.
La hormona del crecimiento recombinante humana se presenta como un agente prometedor, a pesar de que su administración en presencia de sepsis puede incrementar la tasa de mortalidad.
En síntesis, la complejidad de los factores que intervienen en la respuesta catabólica a la injuria limita la consecución de éxitos deseables, incluso con un enfoque multidisciplinario en el manejo del paciente.
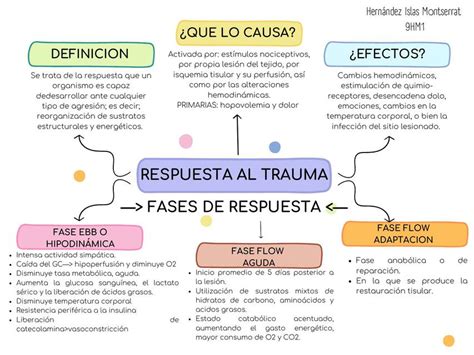
Errores Innatos del Metabolismo (EIM) y el Desafío Anestésico
La historia de las enfermedades de almacenamiento de glucógeno (EAG) se remonta a los años veinte, con descripciones anatómicas de individuos que presentaban hipertrofia orgánica y severos trastornos metabólicos durante la lactancia. Observaciones iniciales de Van Creveld, Von Gieke y Pompe sentaron las bases para comprender un grupo de enfermedades infantiles caracterizadas por la incapacidad de lograr una "combustión completa del glucógeno". La falta de acceso a la energía liberada por la degradación del glucógeno conduce a su acumulación en los tejidos, afectando órganos como el hígado, los riñones, el corazón y los músculos.
A pesar de la limitada información disponible en aquel entonces, estos investigadores reconocieron la naturaleza heterogénea de estas anomalías y su compleja etiología, sin tratamientos predecibles. Sus brillantes conclusiones se corroboraron posteriormente con el descubrimiento de los pasos necesarios para la síntesis y degradación del glucógeno.
Actualmente, se conoce la deficiencia enzimática específica en todas las EAG y sus consecuencias metabólicas. Sin embargo, el diagnóstico preciso de las EAG aún presenta desafíos, requiriendo un examen detallado de signos y síntomas, junto con la selección de pruebas bioquímicas y genéticas idóneas. Esto puede ser particularmente complejo en neonatos y lactantes con presentaciones insidiosas.
En la práctica clínica, es habitual evaluar a los neonatos antes de una cirugía cuando se sospecha una anomalía metabólica, especialmente si se combinan hallazgos neurológicos vagos o una función miocárdica anormal. Ante un diagnóstico confirmado de EAG en un neonato que requiere cirugía de urgencia, el anestesiólogo debe plantearse cómo prevenir las complicaciones inducidas por los anestésicos y el estrés metabólico de la cirugía. La literatura y la experiencia clínica en anestesia para la mayoría de las EAG son limitadas, a menudo basadas en reportes aislados de complicaciones severas o evoluciones sin incidentes.
Glucogenosis Tipo I (Enfermedad de Von Gierke)
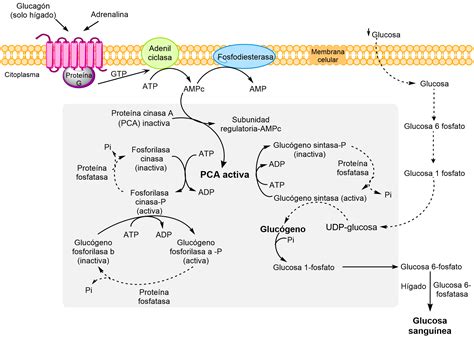
La EAGI, o enfermedad de Von Gierke, es la forma más común de estas patologías, con una incidencia anual de 1/50.000-100.000 nacimientos. Se manifiesta entre los 3 y 4 meses de edad con síntomas de hipoglucemia, temblores, convulsiones y apnea. Normalmente, la glucosa-6-fosfatasa es un sistema multienzimático clave en la gluconeogénesis y la glucogenólisis. En la EAGI, se han descrito múltiples defectos en esta cascada enzimática, afectando la glucosa-6-fosfato hidrolasa, la glucosa-6-fosfato translocasa, la translocasa por fosfato inorgánico y la translocasa por glucosa inorgánica. Genéticamente, los pacientes con EAG presentan mutaciones en el gen de la glucosa-6-fosfato hidrolasa, o en el gen de la glucosa-6-translocasa para otras variantes de la EAGI. Estas complejas interacciones bioquímicas y genéticas dificultan la predicción certera de la respuesta individual de las variantes de la EAGI a los anestésicos.
Glucogenosis Tipo II (Enfermedad de Pompe)
La enfermedad de Pompe (EAGII) se ha asociado consistentemente en la literatura con la presencia de arritmias ventriculares tras la inducción de anestesia general con ciertos agentes. Estudios han sugerido que las técnicas anestésicas usuales con propofol o sevoflurano podrían estar relacionadas con arritmias malignas y fallecimientos. Se recomienda una estratificación de riesgo preoperatorio que incluya una evaluación detallada de la masa ventricular izquierda, ya que los pacientes que fallecieron presentaban los índices más elevados. Sin embargo, el pequeño tamaño de las muestras y la falta de datos fisiológicos cardíacos detallados impiden calcular el riesgo específico de mortalidad para cada agente anestésico.
Glucogenosis Tipo III
Un estudio retrospectivo de Valencia et al. analizó una serie de 19 pacientes con EAGIII expuestos a anestésicos usuales. Este trabajo no reportó eventos fatales, y solo dos pacientes presentaron complicaciones aparentemente vinculadas a la anestesia. Curiosamente, cuatro de estos pacientes con EAGIII también presentaban cierto grado de cardiomiopatía hipertrófica, sin reportarse arritmias ventriculares durante la anestesia. La mayoría recibió inducción anestésica con sevoflurano o propofol sin efectos adversos. Se concluyó que la baja incidencia de complicaciones se debió en parte al bajo riesgo de los procedimientos quirúrgicos en pacientes clínicamente estables.
El avance en el campo de las patologías complejas como las EAG es notable. La terapia dirigida con reemplazo de enzimas humanas recombinantes ha sido un avance significativo, pero también aumenta la exigencia para los equipos multidisciplinarios. A medida que más pacientes con raras deficiencias enzimáticas sobreviven por más tiempo, la expectativa de sobrevida tras la cirugía aumenta. Sin embargo, persisten interrogantes sobre los mecanismos de las complicaciones anestésicas en este grupo de pacientes, como la diferencia en la aparición de arritmias ventriculares entre la EAGII y la EAGIII, a pesar de la exposición a agentes y procedimientos similares.
No está claro si la fibrilación ventricular en pacientes con EAGII bajo anestesia se debe a hipoperfusión coronaria, hipoxia, vasoconstricción o infiltración de glucógeno en el sistema de conducción eléctrica del corazón. Tampoco se conoce si los pacientes con EAGIII están protegidos de estos efectos, ni cómo se comparan los pacientes con EAG y cardiomiopatía con aquellos con cardiomiopatías aisladas en su respuesta cardiovascular a la depresión miocárdica o a los agentes vasodilatadores. Se anticipa la necesidad de desarrollar centros médicos dedicados, con atención centralizada y capacidad de investigación, para establecer guías de seguridad ampliamente aceptadas para el cuidado anestésico de pacientes con EAG.
Mientras tanto, en todo paciente diagnosticado con EAG, la evaluación preoperatoria y la planificación deben incluir un conocimiento detallado de la anatomía y función cardíaca, un análisis cuidadoso de los agentes anestésicos, monitorización intraoperatoria y manejo posoperatorio. Estas consideraciones deben aplicarse a cualquier paciente pediátrico enfermo con alta morbimortalidad esperada.
Síndrome Metabólico y Complicaciones Perioperatorias
El síndrome metabólico (SM) es un conjunto de alteraciones asociadas a un alto riesgo de enfermedades cardiovasculares. A pesar de ser un problema de salud pública, su impacto en el ámbito anestésico-quirúrgico es poco conocido.
Un estudio de casos y controles con 300 pacientes (150 casos y 150 controles) en Cartagena, Colombia, analizó la correlación entre el SM y las complicaciones perioperatorias en pacientes de cirugía programada con anestesia general. Se registraron variables sociodemográficas, hemodinámicas, respiratorias y complicaciones perioperatorias (hipotensión, hipertensión, hipoxemia, sangrado, dolor moderado-severo y náuseas o vómitos postoperatorios).
Los resultados indicaron que las complicaciones perioperatorias fueron significativamente más frecuentes en el grupo de casos con SM (p<0,001). Se observaron diferencias significativas en edad y estado físico según la Asociación Americana de Anestesiólogos (ASA) (p<0,05). El síndrome metabólico se correlacionó con un mayor riesgo de complicaciones perioperatorias (odds ratio [OR] = 3,31). El estado físico ASA III también fue un factor de riesgo de complicaciones postoperatorias (OR = 4,01).
Las conclusiones del estudio resaltan que el síndrome metabólico es un factor de riesgo de complicaciones perioperatorias. Se enfatiza la necesidad de implementar estrategias de intervención sanitaria para la prevención y el manejo del SM en el ámbito quirúrgico, con el objetivo de reducir las complicaciones asociadas.
SÍNDROME METABÓLICO. Síntomas, tratamiento y prevención
Errores Innatos del Metabolismo en Pacientes Pediátricos
Los errores innatos del metabolismo (EIM) son desórdenes bioquímicos causados por el defecto de una proteína en alguna vía metabólica, asociándose a complicaciones multisistémicas y afectando significativamente la calidad de vida de los pacientes pediátricos. La incidencia reportada de EIM varía de 1:800 a 1:5.000 nacimientos, y a menudo son subdiagnosticados debido a sintomatología inespecífica, bajo índice de sospecha o manifestaciones intermitentes. La terapia de reemplazo enzimático y una mejor comprensión fisiopatológica han prolongado la esperanza de vida de estos pacientes, incrementando la frecuencia con la que son sometidos a cirugías no cardíacas.
La literatura sobre el manejo anestésico en EIM es escasa, con predominio de reportes de casos específicos. Un estudio observacional descriptivo retrospectivo en el Hospital Pablo Tobón Uribe (HPTU) analizó el manejo anestésico en pacientes pediátricos con EIM sometidos a cirugía no cardíaca entre 2008 y 2011. Se incluyeron 19 pacientes, con un total de 34 eventos anestésicos.
El EIM más frecuente fue la glucogenosis tipo III (7 pacientes, 37%), seguido de la hiperglicinemia no cetósica (4 pacientes, 21%). En general, se presentaron pocas complicaciones anestésicas, lo cual se atribuye a la naturaleza de bajo riesgo de los procedimientos electivos y a la optimización preoperatoria.
Se observaron dos complicaciones anestésicas en el posoperatorio inmediato de pacientes con hiperglicinemia no cetósica: convulsiones en un caso y la necesidad de ventilación mecánica en otro. Estos hallazgos sugieren que las convulsiones y la insuficiencia respiratoria son posibles complicaciones perioperatorias en la hiperglicinemia no cetósica.
La evaluación preanestésica debe considerar el compromiso cardiorrespiratorio y las alteraciones de la vía aérea, especialmente en patologías como la mucopolisacaridosis, que puede cursar con inestabilidad de la columna cervical. Los paraclínicos preoperatorios deben individualizarse según el compromiso del paciente. Es destacable que en la glucogenosis tipo III, cuatro de los siete pacientes presentaron cardiomiopatía hipertrófica, hallazgo no tan común como el compromiso hepático y muscular.
En el posoperatorio, estos pacientes requieren vigilancia estrecha debido al riesgo de descompensación metabólica y deterioro clínico. Es fundamental reiniciar el manejo farmacológico y dietario tempranamente, evitar largos períodos de ayuno, prescribir líquidos con dextrosa y mantener una adecuada hidratación. Las cirugías programadas deben realizarse en centros con equipos multidisciplinarios y disponibilidad de UCI.
Las limitaciones del estudio incluyen el subregistro, la clasificación diagnóstica y datos incompletos en algunas historias clínicas. Se destaca la necesidad de protocolos claros en cuanto a la optimización preanestésica y el plan de manejo perioperatorio para garantizar la mejor atención a estos pacientes, dada la limitada familiaridad con ellos en Colombia.

tags: #anestesia #alteraciones #metabolicas