La resonancia magnética (RM) se ha consolidado como una herramienta fundamental en el diagnóstico y pronóstico de diversas condiciones neurológicas, especialmente en la población neonatal. A pesar de su creciente uso, la heterogeneidad en los protocolos entre centros médicos persiste, lo que subraya la necesidad de estandarización. Este documento, desarrollado por el Grupo Cerebro Neonatal en colaboración con neurorradiólogos pediátricos, establece recomendaciones basadas en evidencia científica y experiencia clínica para optimizar su aplicación.
Logística y Preparación para la Resonancia Magnética Neonatal
La logística de la RM neonatal abarca desde la preparación del paciente hasta la adquisición de imágenes y la aplicación de protocolos específicos para cada patología. La preparación del paciente, detallada en la Tabla S1 del Apéndice B, es crucial para garantizar la seguridad y calidad del estudio. Se enfatiza la importancia de la comunicación directa con el equipo radiológico, proporcionando información clínica detallada como la edad gestacional, edad posmenstrual y cronológica, antecedentes relevantes y hallazgos neurológicos.
Para obtener imágenes de alta calidad, se recomienda el uso de equipos de al menos 1.5 T y bobinas específicas para cabeza neonatal o multicanal. El protocolo de secuencias y parámetros debe ser optimizado para el cerebro neonatal, adaptándose al historial clínico específico del paciente. Si bien existe un protocolo básico (Tabla 1), se deben añadir secuencias individualizadas según la necesidad (Tabla 2).
Papel de la Resonancia Magnética en Enfermedades Neurológicas Neonatales
La RM juega un papel diagnóstico y pronóstico clave en diversas enfermedades neurológicas neonatales. Se destacan las siguientes:
Encefalopatía Neonatal Aguda y Convulsiones
La encefalopatía neonatal aguda es un síndrome clínico caracterizado por una alteración del nivel de alerta o neuroconducta, que puede acompañarse de disfunción neurológica de origen hipóxico-isquémico, infeccioso, genético o metabólico. En neonatos donde no se sospecha origen hipóxico-isquémico, la RM se realiza lo antes posible para orientar el diagnóstico y, en ocasiones, el tratamiento.
Encefalopatía Hipóxico-Isquémica (EHI)
La RM es el estudio de elección para diagnosticar la naturaleza y gravedad de la lesión cerebral en la EHI, así como para proporcionar información pronóstica. La EHI asocia patrones de lesión característicos con fuerte correlación con el pronóstico neurológico (Tabla 3). Es fundamental describir con precisión la afectación de estructuras individuales, incluyendo la corteza, ganglios basales, sustancia blanca, troncoencefálico y cuerpos mamilares. La lesión aguda de los cuerpos mamilares, correlacionada con problemas de aprendizaje y memoria, requiere cortes axiales o coronales en T2 de 2mm para su visualización (Tablas 2 y 3).
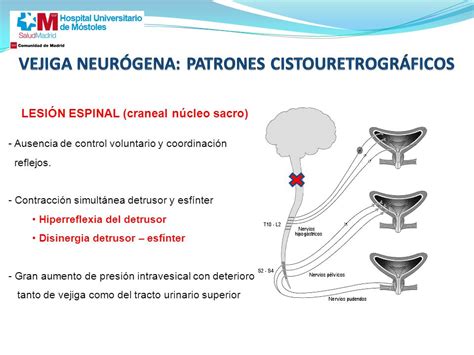
Aunque la ecografía cerebral (EC) se realiza de forma rutinaria en niños con EHI, su sensibilidad y valor pronóstico son más limitados, especialmente para lesiones corticales, cerebelosas y del troncoencefálico. Sin embargo, la EC es un estudio complementario que permite seguimientos seriados y monitorización de la evolución del daño.
Infarto Cerebral Arterial Neonatal (ICAN)
La RM cerebral es la técnica de elección para el diagnóstico y pronóstico del ICAN, determinando el territorio arterial afectado, la extensión y las estructuras involucradas (Tabla 4). La EC puede identificar el ICAN, especialmente en la arteria cerebral media, a partir de las 24 horas de vida en manos expertas. Una RM con tractografía a los 3 meses de edad puede ser útil para afinar el pronóstico (Tabla 4).
Trombosis del Seno Venoso (TSV) e Infarto Venoso Cerebral
La RM combinada con venografía alcanza alta sensibilidad para la TSV, facilitando la caracterización de lesiones asociadas. La EC también ha demostrado alta especificidad en el diagnóstico de TSV. El infarto venoso cerebral, a menudo hemorrágico y localizado en territorios de drenaje venoso, se diagnostica con estudios de RM, especialmente con secuencias de susceptibilidad magnética (SSM). El pronóstico depende de la localización y las estructuras afectadas.
Neonatos con Cardiopatías Congénitas
En neonatos con cardiopatías congénitas, la dismaduración cerebral, la lesión por isquemia-reperfusión y el daño cerebral adquirido son mecanismos patogénicos relevantes. La EC es obligatoria al nacimiento, tras procedimientos, ante clínica neurológica o deterioro hemodinámico agudo. Si la EC muestra alteraciones o es no concluyente, se completa el estudio con RM.
Infección Congénita por Citomegalovirus (CMV)
La EC y la RM son complementarias en el estudio de la infección congénita del SNC por CMV. La EC es superior para diagnosticar calcificaciones y vasculopatía arterial. En RN con infección congénita sintomática o alteraciones en la EC, se realiza RM para evaluar la lesión de sustancia blanca y descartar malformaciones corticales o cerebelosas (Tabla 5).
Metabolismo Magnético Anderson y Envejecimiento
En un contexto diferente, la investigación sobre el envejecimiento ha explorado el uso de la resonancia magnética para evaluar el ritmo de envejecimiento biológico. Estudios previos desarrollaron una métrica llamada "Velocidad del Envejecimiento" (Pace of Aging) basada en análisis de sangre y seguimiento de la salud a lo largo del tiempo. Investigaciones más recientes combinaron esta métrica con escáneres de resonancia magnética cerebral para desarrollar una nueva medida, el "Dunedin-PACNI", basada exclusivamente en datos cerebrales. Esta herramienta ha demostrado predecir la disminución de la capacidad cognitiva, el riesgo de enfermedades y la mortalidad futura.
Examen del cerebro por resonancia magnética
El Dr. Ahmad Hariri de la Universidad de Duke destaca que esta metodología permite predecir el debilitamiento de las habilidades cognitivas y el riesgo de demencia en personas mayores, basándose en información recopilada a mitad de la vida.
Estudio Dipcan: Digitalización y Medicina Personalizada en Cáncer
El estudio Dipcan es una iniciativa que busca transformar la medicina personalizada en oncología mediante la digitalización y el análisis de datos integrados. Este proyecto, financiado por la Unión Europea, reclutará a 2.000 pacientes con tumores sólidos metastásicos para ofrecerles de forma gratuita un test genómico, historia clínica estructurada, resonancia magnética e imágenes digitalizadas de su tumor.
El objetivo es generar un algoritmo de inteligencia artificial para comprender mejor los tumores. El Dr. Enrique Grande, director científico del proyecto, explica que se integrarán datos clínicos, metabólicos, genómicos, patológicos digitales y radiómicos para obtener una visión de 360º de los tumores. La transformación digital permitirá codificar los datos de los pacientes desde múltiples perspectivas.
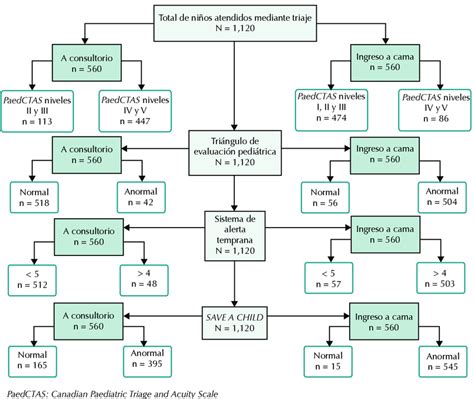
El estudio se llevará a cabo en la Unidad de Ensayos Clínicos Fase I del MD Anderson Cancer Center Madrid. Los participantes recibirán una analítica de sangre, una resonancia magnética y se les tomará una muestra tumoral. Cualquier paciente con un tumor sólido metastásico que cumpla los criterios de inclusión podrá participar de forma gratuita. El estudio Dipcan ofrece a los pacientes un mejor conocimiento de su enfermedad y la posibilidad de acceder a tratamientos dirigidos basados en alteraciones moleculares específicas.
La innovación en anatomía patológica, biología molecular y el análisis de datos genómicos, incluyendo la biopsia líquida, son pilares fundamentales del estudio. La integración de ingenieros en el ámbito de la salud es crucial para la gestión y análisis de grandes volúmenes de datos (big data), lo que permitirá tomar decisiones más informadas y atraer investigación farmacéutica.
Se espera que el estudio Dipcan cambie la práctica clínica en oncología mediante un mejor conocimiento de la enfermedad, las características clínicas y moleculares de los pacientes, y la optimización de recursos. El reclutamiento se extenderá por aproximadamente dos años, seguido de un año de análisis de datos, con una duración total de tres años. Se espera abrir los primeros centros de participación a finales de marzo o principios de abril.
Métodos de Valoración del Estado Nutricional
La desnutrición, tanto por defecto como por exceso (obesidad), sigue siendo una patología de gran impacto en la morbi-mortalidad, afectando a un porcentaje significativo de pacientes hospitalizados. La evaluación nutricional es una herramienta fundamental que debe realizarse de forma temprana y regular. El término "malnutrición" abarca un espectro de alteraciones nutricionales, incluyendo déficits y excesos de nutrientes.
Los métodos de evaluación del estado nutricional se dividen en:
Evaluación Global Subjetiva (VGS)
Integra parámetros clínicos como cambios en el peso corporal, ingesta alimentaria, síntomas gastrointestinales y capacidad funcional. Es útil para identificar pacientes en riesgo de desnutrición, con alta sensibilidad y especificidad, aunque no es útil en casos de malnutrición por exceso.
Evaluación Objetiva
Indicada en pacientes desnutridos o en riesgo, se basa en indicadores clínicos, antropométricos, dietéticos y socioeconómicos para realizar indicaciones nutricionales precisas. Se clasifica la desnutrición cualitativamente (Marasmo, Kwashiorkor, Mixta, Estados Carenciales, Desnutrición Oculta) y cuantitativamente (según el porcentaje de Peso de Referencia).
Indicadores Objetivos de Diagnóstico del Estado Nutricional
1. Evaluación Antropométrica: Medición de dimensiones y composición corporal. Incluye indicadores de masa corporal total (Índice de Peso para la Talla, % Peso de Referencia), masa grasa (Índice de Masa Corporal, % Grasa Corporal, circunferencias, pliegues cutáneos) y masa muscular o magra (estimada mediante diversas ecuaciones y modelos). El Índice de Masa Corporal (IMC) es un indicador clave, con umbrales de alerta para el riesgo individual y poblacional.
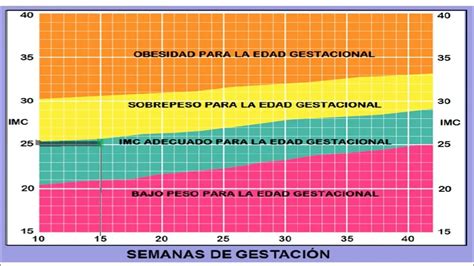
- En el neonato: Se utilizan peso corporal, longitud, circunferencias (brazo, tórax, muslo) y pliegues cutáneos.
- En el niño y adolescente: Se emplean peso, talla, circunferencia cefálica, circunferencia media del brazo izquierdo, pliegues tricipital y subescapular, y áreas grasa y muscular.
2. Indicadores Bioquímicos: Análisis de marcadores en sangre u otros fluidos corporales que reflejan el estado nutricional.
3. Indicadores Dietéticos: Evaluación de la ingesta de alimentos y nutrientes a través de encuestas alimentarias, registros o recordatorios de 24 horas.
4. Indicadores Clínicos: Examen físico en busca de signos y síntomas asociados a deficiencias o excesos nutricionales.
5. Indicadores Funcionales: Evaluación de la función inmunológica, muscular o de otros sistemas corporales que puedan verse afectados por el estado nutricional.
La evaluación nutricional debe ser parte integral de la atención médica, permitiendo identificar individuos en riesgo, diagnosticar malnutrición y monitorizar la eficacia de las intervenciones nutricionales.
tags: #estudio #del #metabolismo #magnetico #anderson