El síndrome metabólico (SM) es una condición clínica definida por la agrupación de múltiples factores de riesgo cardiovascular de origen metabólico. Estos factores, actuando de manera sinérgica, incrementan significativamente el riesgo de desarrollar enfermedades cardíacas, diabetes mellitus tipo 2 (DM2) y otras patologías. Aunque una persona puede presentar un solo factor de riesgo, la presencia de al menos tres de ellos define el síndrome metabólico.
La prevalencia del SM es considerable en la población general, y su aparición está estrechamente ligada a la resistencia a la insulina, la obesidad, el sedentarismo y, en algunos casos, a la susceptibilidad familiar. La DM2 y otros componentes del SM se han convertido en enfermedades epidémicas, asociadas a una alta morbimortalidad.
Definición y Criterios Diagnósticos del Síndrome Metabólico
La definición del SM ha variado a lo largo del tiempo y entre diferentes consensos internacionales. Cuatro grupos principales han establecido criterios diagnósticos: la Organización Mundial de la Salud (OMS), el Grupo de Estudio para la Resistencia a la Insulina (EGIR), el consenso del National Cholesterol Education Program Adult Treatment Panel III (NCEP ATP III) y la Federación Internacional de Diabetes (IDF).
Los consensos más utilizados son los de la IDF y el NCEP ATP III. El NCEP ATP III requiere la presencia de al menos 3 de los siguientes 5 criterios: obesidad central, elevación de triglicéridos, bajo colesterol HDL (HDLc), hipertensión arterial y alteración de la glicemia de ayunas. La American Heart Association/National Heart, Lung and Blood Institute (AHA/NHLBI) sugirió un punto de corte de 100 mg/dL para la glicemia de ayunas.
La Federación Internacional de Diabetes (IDF) establece como requisito básico la presencia de obesidad central y la medición de la circunferencia abdominal. En 2009, se realizó un consenso internacional que propuso la siguiente definición, requiriendo el cumplimiento de al menos tres de cinco criterios:
- Perímetro abdominal: De acuerdo al grupo étnico (≥80 cm para mujeres y ≥90 cm para hombres).
- Triglicéridos: ≥150 mg/dL o en tratamiento farmacológico para hipertrigliceridemia.
- Colesterol HDL (HDLc): <40 mg/dL en hombres y <50 mg/dL en mujeres, o en tratamiento farmacológico para aumentarlo.
- Presión arterial: ≥130/85 mmHg o en tratamiento farmacológico para hipertensión.
- Glicemia en ayunas: ≥100 mg/dL o en tratamiento con hipoglucemiantes.
La prevalencia del SM varía considerablemente según los criterios empleados, la edad, el género y la raza. Generalmente, aumenta con la edad y es más alta en varones en ciertos grupos etarios.
Fisiopatología del Síndrome Metabólico
Si bien no existe un único mecanismo patogénico universalmente aceptado para el SM, se han propuesto varias explicaciones fisiopatológicas, siendo la resistencia a la insulina (RI) considerada el principal factor asociado.
Resistencia a la Insulina y Obesidad
La resistencia a la insulina es una afección en la cual el cuerpo no utiliza eficazmente la insulina, una hormona crucial para el transporte de glucosa a las células. Esta resistencia, a menudo asociada con la obesidad, especialmente la obesidad abdominal (cuerpo con "forma de manzana"), es un eje central en la patogenia del SM.
El tejido adiposo, particularmente la grasa visceral abdominal, juega un papel fundamental. Los adipocitos viscerales son metabólicamente más activos, liberando una mayor cantidad de ácidos grasos libres (AGL) y citoquinas inflamatorias que drenan directamente al hígado. Los AGL elevados en plasma tienen un efecto directo sobre órganos diana de la insulina como el hígado y el músculo, bloqueando la señalización intracelular del receptor de insulina, un fenómeno conocido como lipotoxicidad.
La lipotoxicidad contribuye a la RI en estos órganos y a la falta de regulación pancreática ante la glucemia elevada. Además, los AGL pueden aumentar el estrés oxidativo, el ambiente proinflamatorio sistémico y disminuir la reactividad vascular.
El Adipocito como Célula Inflamatoria
El estado proinflamatorio asociado a la obesidad y al SM se explica por la presencia de células inflamatorias entre los adipocitos y por la actividad inflamatoria inherente de los propios adipocitos. Se observa un aumento de moléculas proinflamatorias como el factor de necrosis tumoral α (FNT-α), el inhibidor del activador del plasminógeno 1 (PAI-1), la interleuquina 6 (IL-6) y la leptina, junto con una disminución de la adiponectina, una citoquina antiinflamatoria.
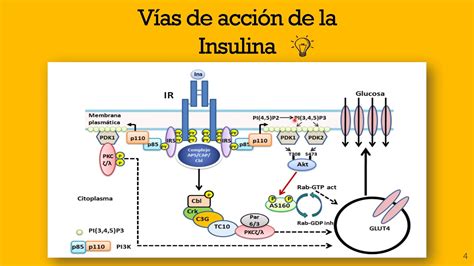
El FNT-α puede producir una fosforilación anormal del sustrato del receptor de la insulina (IRS), alterando su transducción. La adiponectina, por otro lado, mejora el control de la glucemia, tiene funciones hipolipemiantes, antiinflamatorias y antiaterogénicas, y su disminución se asocia con SM y progresión de enfermedad cardiovascular.
Efectos No Clásicos de la Insulina
La insulina ejerce efectos vasodilatadores, antitrombóticos, antiinflamatorios, antioxidantes y natriuréticos que se ven alterados en presencia de RI. Estos efectos no clásicos son importantes para comprender las alteraciones observadas en el SM, especialmente el aumento del riesgo aterotrombótico.
La RI puede determinar un aumento de las especies reactivas de oxígeno y una disminución de la actividad de la óxido nítrico sintetasa endotelial (eNOS). Esto se acompaña de aumentos locales y sistémicos de endotelina y angiotensina, potentes vasoconstrictores e inflamatorios. El resultado es un estado inflamatorio crónico en la pared vascular y disfunción endotelial, que contribuyen a la ateromatosis.
Factores Genéticos y Otros Mecanismos
Los factores genéticos pueden explicar la RI en individuos no obesos, ciertas poblaciones y parientes directos de personas diabéticas. Se han identificado polimorfismos en genes como el de la "Fatty Acid Binding Protein 2" (FABP2) asociados con RI y obesidad.
El rol de los PPAR (Receptores del proliferador peroxisomal activado), particularmente los tipos α y γ, es crucial. Son esenciales para la diferenciación y proliferación de los adipocitos, el almacenamiento de ácidos grasos, el aumento de la síntesis de adiponectina y la prevención de la salida de AGL a la circulación. La modulación de estos receptores mediante agonistas puede mejorar la RI y el SM.
Otras alteraciones fisiopatológicas incluyen el aumento de la expresión de angiotensinógeno en la grasa visceral, que puede contribuir a la hipertensión, y el incremento de los niveles de PAI-1, relacionado con complicaciones cardiovasculares. El estrés oxidativo también se ha relacionado directamente con el SM, evidenciado por el aumento de enzimas antioxidantes y productos de peroxidación lipídica.
Síndrome Metabólico y Diabetes Mellitus Tipo 2
Existe una fuerte asociación entre el SM y el desarrollo de Diabetes Mellitus tipo 2 (DM2). En pacientes que cumplen los criterios de SM pero no tienen DM, el riesgo de desarrollar esta enfermedad aumenta significativamente. Por otro lado, en individuos diabéticos, la presencia de SM se ha identificado como un factor de riesgo cardiovascular independiente.
La obesidad central, la resistencia a la insulina y la disfunción del tejido adiposo son factores clave que predisponen tanto al SM como a la DM2. La hiperinsulinemia compensatoria inicial puede mantener los niveles de glucemia, pero con el tiempo, si la secreción de insulina es insuficiente, puede aparecer intolerancia a la glucosa y, finalmente, DM2.
Enfoque Terapéutico
El objetivo principal del tratamiento del SM es la prevención del desarrollo de enfermedad cardiovascular. La terapia de primera línea se centra en la pérdida de peso y el control de los factores de riesgo mayores, como el C-LDL, la hipertensión arterial y la alteración del metabolismo de los hidratos de carbono.
La modificación del estilo de vida, incluyendo una dieta equilibrada (rica en frutas, verduras, granos enteros, nueces y semillas) y la actividad física regular, ha demostrado ser eficaz. Sin embargo, estas estrategias solo tienen un impacto significativo si se mantienen a largo plazo. La participación de un equipo multidisciplinario es fundamental para integrar los elementos clave del tratamiento, que incluyen cambios de estilo de vida, dieta adecuada, actividad física y apoyo social.
En casos donde los cambios en el estilo de vida no son suficientes, puede ser necesario el uso de medicamentos. Los fármacos con efectos pleiotrópicos, que actúan sobre el eje renina-angiotensina-aldosterona o sobre los receptores PPAR, parecen prometedores.
Enfermedades metabólicas y la importancia del ejercicio en Falando de Saúde.
tags: #fisiopatologia #del #sindrome #metabolico