El tejido adiposo, lejos de ser un simple reservorio de energía, es actualmente reconocido como un órgano dinámico con complejas funciones neuroinmunoendocrinas que participa activamente en la homeostasis del organismo. Su notable plasticidad le permite adaptarse a diversas condiciones, como la ingesta de nutrientes o las fluctuaciones en su volumen tisular, modificando tanto la función como el número de sus células constituyentes. La liberación anómala de moléculas por parte de estas células, incluyendo citoquinas y adipocinas, puede desencadenar procesos inflamatorios locales y sistémicos, especialmente cuando provienen del tejido adiposo visceral, afectando a órganos como el hígado y el sistema cardiovascular.
La obesidad, caracterizada por un incremento excesivo de grasa corporal, representa un desafío de salud pública global. Mientras que tradicionalmente se le consideraba un anexo para protección, calor y energía, la investigación ha revelado su papel multifacético como un órgano con funciones neuroinmuno-endocrinas. A través de la producción de hormonas, antimicrobianos, citoquinas y adipocinas, el tejido adiposo interactúa con diversas células y órganos, contribuyendo a la defensa y al equilibrio del organismo.
La plasticidad del tejido adiposo se manifiesta en su capacidad de regeneración tras cirugías y en su variabilidad de tamaño, influenciada por factores como la edad, la actividad física, la ingesta alimentaria, la función endocrina, la genética y la programación neonatal. En cuanto al balance energético, el adipocito blanco se especializa en el almacenamiento de energía, mientras que el tejido adiposo pardo (BAT) la disipa en forma de calor.
Origen de los Adipocitos
Diversos linajes celulares, originados de la célula madre mesenquimatosa, dan lugar a los distintos tipos de adipocitos, cada uno caracterizado por la expresión de genes y factores de transcripción específicos. El adipocito blanco, por ejemplo, se desarrolla a partir de la célula madre mesenquimatosa, pasando por etapas intermedias como los adipoblastos y preadipocitos, los cuales expresan el factor de transcripción 21.
Se han identificado progenitores PDGFRα (receptor del factor de crecimiento derivado de plaquetas α) como bipotenciales, capaces de originar tanto adipocitos blancos como beige. Aunque los adipocitos blancos generalmente no expresan MyF5, estudios recientes han detectado este marcador en algunos de sus progenitores. El adipocito rosa, por su parte, tiene su origen en la glándula mamaria de los roedores. Durante la gestación, los adipocitos blancos se transforman en células epiteliales productoras de leche, y los adipocitos pardos en células mioepiteliales, ambos considerados reservorios grasos y expresando marcadores como S-100b y leptina.
Tipos de Tejido Adiposo: Blanco y Pardo
El ser humano posee dos tipos principales de tejido adiposo: el tejido adiposo blanco (WAT) y el tejido adiposo pardo (BAT), cada uno con características fisiológicas y funcionales distintas. El WAT es el más predominante.
Tejido Adiposo Blanco (WAT)
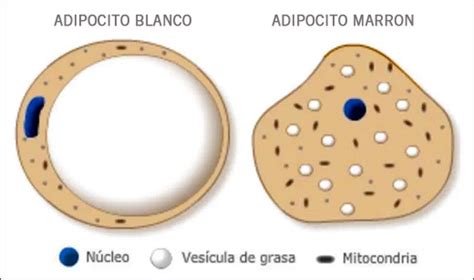
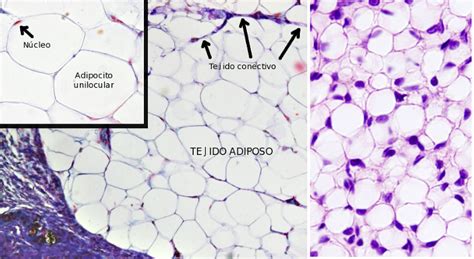
Los adipocitos blancos son células de tamaño variable, principalmente determinado por su contenido lipídico. De forma esférica cuando están aislados, adoptan una forma ovalada al agruparse en el tejido. Su característica distintiva es la presencia de una única gota unilocular de triglicéridos que ocupa más del 90% de su volumen. El núcleo se aplana y se desplaza hacia la periferia, con el citoplasma formando un delgado borde alrededor de la masa lipídica. La masa lipídica no está rodeada por una membrana.
El WAT constituye al menos el 10% del peso corporal total en un individuo sano. Se localiza en diversas áreas del cuerpo, incluyendo la hipodermis (panículo adiposo, actuando como aislante térmico), la glándula mamaria (fuente de lípidos y energía), el omento mayor, los mesenterios, el espacio retroperitoneal (rodeando los riñones), el pericardio visceral y el globo ocular (como almohadilla protectora), además de la médula ósea.
El WAT secreta una serie de péptidos, conocidos colectivamente como adipocinas (hormonas, factores de crecimiento y citoquinas), que ejercen acciones autocrinas y endocrinas. Estas moléculas permiten la comunicación sistémica con otros tejidos y órganos como el cerebro, el músculo y el hígado, contribuyendo a la regulación del equilibrio energético global.
Tejido Adiposo Pardo (BAT)
El tejido adiposo pardo es un tejido termogénico esencial, presente en grandes cantidades en los neonatos y cuya cantidad se reduce drásticamente con la edad en los adultos. En neonatos, el BAT representa casi el 5% de la masa corporal total y se localiza en regiones como la cervical, axilar, paravertebral, mediastínica, esternal y abdominal. Su función principal es generar calor para proteger al recién nacido contra la hipotermia durante la exposición al frío (termogénesis adaptativa).
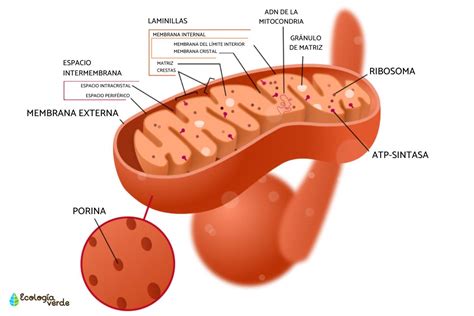
Las células del tejido adiposo pardo (multiloculares) son más pequeñas que las del WAT. Su citoplasma contiene numerosas gotas de lípidos pequeñas, de ahí su denominación multilocular. El núcleo es excéntrico pero no aplanado. Los adipocitos pardos son generalmente poligonales, con un diámetro que varía entre 15 y 50 μm. Presentan diferencias clave respecto al WAT: una alta cantidad de mitocondrias esféricas y grandes, un elevado grado de vascularización e inervación simpática, y la expresión de la proteína específica proteína de desacoplamiento (UCP1 o termogénica).
La UCP1, localizada en la membrana mitocondrial interna, actúa como un conducto de protones, disipando la energía generada por la cadena de transporte de electrones en forma de calor, en lugar de ser utilizada para la síntesis de ATP. Este proceso, conocido como desacoplamiento de la oxidación de ácidos grasos, es crucial para la generación de calor y la protección contra la hipotermia.
El Fenómeno de Browning y las Células Beige
La epidemia de obesidad y el aumento de enfermedades metabólicas asociadas han impulsado la búsqueda de estrategias terapéuticas. En el tejido adiposo blanco, existen adipocitos UCP+ que pueden experimentar un proceso de transdiferenciación, adquiriendo un fenotipo similar al del tejido adiposo pardo. Estas células se conocen como adipocitos brite o beige, y su origen se denomina "browning" del tejido blanco.
La irisina, una adipoquina y mioquina inducida por el ejercicio, secretada principalmente por el músculo esquelético y también por el tejido adiposo, ha demostrado potencial para inducir el "browning" en ratones. Estudios en humanos sugieren que los niveles de irisina en plasma aumentan con el entrenamiento y tras el ejercicio, indicando su rol en la demanda energética y su posible aplicación terapéutica contra la obesidad y la mejora de la diabetes.
El factor de crecimiento fibroblástico 21 (FGF-21), una hormona hipoglucemiante producida principalmente en el hígado, también juega un papel en la termogénesis y la expresión de UCP1 en el tejido adiposo pardo, promoviendo la lipólisis en el WAT y la generación de calor.
La familia de las proteínas morfogénicas óseas (BMP), miembros de la superfamilia del factor de crecimiento transformante-β (TGF-β), participan en la adipogénesis del BAT y en el "browning" de las células beige. Específicamente, el BMP-7 induce la expresión de UCP-1 y activa reguladores transcripcionales clave como PPARγ y PGC-1α, promoviendo el gasto energético y protegiendo contra el aumento de peso.
Las hormonas tiroideas son reguladores fundamentales del metabolismo y la temperatura corporal. La orexina también influye en la termogénesis, especialmente durante el envejecimiento.
Situaciones que Inducen la Transdiferenciación y Aumento de Tejido Adiposo Pardo
Diversas situaciones fisiológicas y patológicas pueden estimular la expansión del tejido adiposo pardo o la aparición de adipocitos beige:
- Estimulación adrenérgica: Situaciones de estrés físico severo o condiciones como el feocromocitoma (un tumor productor de catecolaminas) pueden inducir un aumento significativo de la masa de BAT.
- Estrés metabólico y termorregulador: Pacientes con quemaduras severas exhiben un estado hipermetabólico, con conversión de adipocitos blancos a BAT. Estudios de inmunohistoquímica han mostrado una mayor expresión de UCP1 y marcadores de grasa parda y beige en estos pacientes, sugiriendo una modificación fenotípica del WAT en respuesta al estrés.
- Hibernomas: Estos tumores benignos derivados de la grasa parda, aunque de etiología incierta, se asocian con una pérdida de peso debido a un aumento de la termogénesis del BAT.
- Exposición a bajas temperaturas y ejercicio: Estas condiciones fisiológicas promueven la actividad y expansión del tejido adiposo pardo y la transdiferenciación a células beige.
El trasplante de grasa, inicialmente una herramienta de investigación, ha demostrado beneficios terapéuticos potenciales en la modulación del peso corporal. En ratones, el trasplante de grasa subcutánea en la cavidad visceral ha resultado en descenso de peso, reducción de masa grasa, mejora de la sensibilidad a la insulina, aumento del consumo de oxígeno y disminución de la grasa corporal total.
Tejido Adiposo y Cáncer de Mama
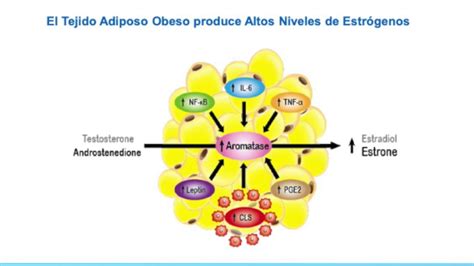
El tejido adiposo juega un papel crucial en el desarrollo de ciertos tipos de cáncer, como el cáncer de mama en mujeres posmenopáusicas. El tejido adiposo es una fuente importante de estrógenos, los cuales están implicados en el desarrollo de tumores hormonodependientes.
Estudios han investigado la relación entre el porcentaje de adiposidad y el índice de inmunorreactividad de los receptores a estrógenos (RE) y progesterona (RP) en mujeres mexicanas con cáncer de mama. Se ha observado una asociación entre el porcentaje de adiposidad y la expresión de RE y RP. La obesidad se ha identificado como un factor de riesgo importante para el desarrollo de cáncer de mama positivo a receptores hormonales.
El tejido adiposo, al ser un órgano endocrino, almacena y metaboliza hormonas esteroideas. Los estrógenos, a su vez, regulan el metabolismo y la localización del tejido adiposo blanco, influyendo en la adipogénesis, lipogénesis y lipólisis. En mujeres posmenopáusicas, la disminución de estrógenos se asocia con un aumento de la grasa central, donde ocurre la aromatización de esteroides sexuales. Los receptores de estrógeno (ER) y progesterona (PR) se expresan en el tejido adiposo humano, siendo la isoforma ERα la de mayor expresión en adipocitos maduros.
Los mecanismos por los cuales los estrógenos y sus receptores modulan el desarrollo tumoral son complejos. Se postula que la unión de estrógenos a sus receptores estimula la proliferación del epitelio mamario, aumentando el número de células susceptibles a errores de replicación y mutaciones. Alternativamente, el metabolismo de los estrógenos puede generar sustancias genotóxicas que dañan directamente el ADN.
La obesidad, al generar un exceso de tejido adiposo blanco, contribuye a la producción de estrógenos, especialmente en mujeres posmenopáusicas. Esto, sumado a la expresión de ER y PR en el tejido adiposo, subraya la importancia de un estilo de vida saludable y el control de la obesidad como estrategias de prevención para el cáncer de mama hormonodependiente.
El Papel de las Adipocinas y la Inmunología del Tejido Adiposo
El tejido adiposo libera una variedad de adipocinas que modulan diversas funciones fisiológicas y patológicas. Algunas de ellas incluyen:
- Leptina: Regula el apetito y el gasto energético, y su desregulación está implicada en la obesidad y la resistencia a la insulina.
- Adiponectina: Posee efectos antiinflamatorios y mejora la sensibilidad a la insulina. Niveles reducidos de adiponectina se asocian con enfermedades cardiovasculares y obesidad.
- Resistina: Se ha relacionado con la inflamación y la resistencia a la insulina.
- Visfatina: Implicada en la regulación de la glucosa y la inflamación.
- Apelina: Desempeña roles en la homeostasis energética, la inflamación y la función cardiovascular.
- Zinc-α2-glicoproteína (ZAG): Modula la masa grasa corporal y puede ser un biomarcador en ciertas enfermedades.
- Proteínas de unión a ácidos grasos (FABPs): Involucradas en el metabolismo de los lípidos.
- Factor de crecimiento de fibroblastos 21 (FGF-21): Regula el metabolismo y la termogénesis.
- ANGPTL8: Identificada como una de las responsables de la inhibición de la lipoproteína lipasa (LPL).
La inmunología del tejido adiposo es un campo de creciente interés. El tejido adiposo alberga una compleja red de células inmunitarias, incluyendo macrófagos, linfocitos T, linfocitos B, células NKT y mastocitos. En condiciones de obesidad, se observa una infiltración de células inmunitarias y un estado de inflamación crónica de bajo grado, que contribuye a la disfunción del tejido adiposo y al desarrollo de comorbilidades metabólicas.
Las células inmunitarias en el tejido adiposo interactúan con los adipocitos y otras células del estroma, liberando citoquinas y factores que modulan la homeostasis energética, la sensibilidad a la insulina y la inflamación sistémica. Por ejemplo, los macrófagos asociados al tejido adiposo (ATM) juegan un papel crucial en la inflamación observada en la obesidad, y su fenotipo puede ser modulado por diversas células inmunitarias, como los eosinófilos y las células del tipo 2 de inmunidad innata (ILC2).
Los linfocitos T reguladores (Tregs) y las células NKT también participan en la regulación de la homeostasis del tejido adiposo y la inflamación. La desregulación de estas poblaciones celulares puede exacerbar la inflamación y la disfunción metabólica en la obesidad.
Avances Tecnológicos y Perspectivas Futuras
El diagnóstico de la obesidad se basa tradicionalmente en el índice de masa corporal (IMC), la medición de la cintura y el porcentaje de grasa corporal. Sin embargo, estas medidas son indirectas y no siempre reflejan fielmente la distribución o el porcentaje total de grasa corporal. La valoración morfofuncional, que incorpora técnicas como la dinamometría, la bioimpedancia y la ecografía, ofrece una visión más completa de la composición corporal.
La biopsia del tejido adiposo subcutáneo (TAS) se perfila como una herramienta valiosa para la medicina personalizada. El estudio de cambios genéticos, morfológicos y funcionales en biopsias de TAS permite un mejor diagnóstico y manejo de pacientes con sobrepeso u obesidad, identificando cambios genéticos y epigenéticos implicados en la enfermedad.
Además, el estudio del tejido adiposo que rodea a los tumores puede arrojar luz sobre los mecanismos moleculares que vinculan la obesidad con el desarrollo y la progresión de ciertos tipos de cáncer. La evaluación de la distribución de la grasa corporal (visceral vs. glúteo-femoral) y el grado de actividad del tejido adiposo son esenciales para comprender las diferencias individuales en el riesgo metabólico y cardiovascular.
La investigación continúa explorando las vías moleculares que modifican el tejido adiposo en respuesta a tratamientos como la cirugía bariátrica. Los cambios en el perfil secretor del tejido adiposo y la expresión de genes implicados en el metabolismo, la inflamación y la organización de la matriz extracelular son áreas de intenso estudio. La caracterización de nuevos componentes del citoesqueleto de los adipocitos, como las septinas, también abre nuevas vías para comprender la plasticidad y disfunción del tejido adiposo.
Obesidad - Adipocitos
tags: #inmunohistoquimica #tejido #adiposo #obeso