Introducción a la Hepatotoxicidad por Psicofármacos
Los pacientes que atraviesan procesos de deshabituación del alcoholismo crónico a menudo reciben tratamientos con psicofármacos que, en su mayoría, presentan un riesgo de hepatotoxicidad. Según el Formulario Nacional de Medicamentos, estos psicofármacos se clasifican en varios grupos: benzodiacepinas, antidepresivos tricíclicos, fármacos de deshabituación, anticonvulsivantes y antipsicóticos.
Se ha observado que los grupos de anticonvulsivantes y antipsicóticos muestran una correlación con las enzimas hepáticas, específicamente con la transaminasa glutámico oxalacética en el caso de los antipsicóticos.
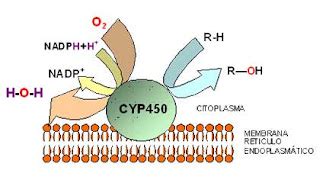
En términos generales, se concluye que la mayoría de los psicofármacos pueden causar daño hepático debido a su metabolismo en el hígado y a los efectos que ejercen sobre las citocromo oxidasas.
Hepatotoxicidad como Reacción Adversa de Psicofármacos
La hepatotoxicidad, aunque conocida, es una reacción adversa infrecuente asociada al uso de inhibidores de la recaptación de serotonina (ISRS) y benzodiacepinas. Dada la alta prevalencia de trastornos psiquiátricos y el consecuente elevado consumo de estos medicamentos, es relevante la publicación de casos que evidencien este riesgo.
Caso Clínico de Fibrosis Hepática Asociada a Psicofármacos
Se estudió el caso de una mujer de 32 años con antecedentes de alergia al polen y trastorno bipolar. Desde febrero de 2001, consumía una infusión diaria de Aquilea tranquilizante. El 7 de diciembre de ese mismo año, inició tratamiento con sertralina, alprazolam y cloracepato. La paciente no presentaba antecedentes de hepatitis, cirugías hepáticas, transfusiones sanguíneas, tatuajes, uso de drogas intravenosas o consumo de alcohol. Tampoco había realizado viajes recientes al extranjero y sus análisis hepáticos previos siempre habían sido normales.
En enero de 2002, la paciente desarrolló un cuadro sintomático caracterizado por diarrea, anorexia y una pérdida de peso de 10 kg. En febrero de 2002, aparecieron ictericia, astenia y prurito. El 15 de febrero, se suspendió la administración de sertralina. La exploración física reveló una paciente con leve ictericia y sin otros hallazgos de relevancia clínica (peso: 50 kg, altura: 154 cm). Los análisis de laboratorio mostraron:
- Bilirrubina total: 3,8 mg/dl
- Bilirrubina directa: 2,8 mg/dl
- ASAT (AST): 108 IU/l
- ALAT (ALT): 281 IU/l
- GGT: 444 IU/l
- FA (Fosfatasa Alcalina): 1200 IU/l
Los resultados del hemograma y la coagulación se encontraban dentro de la normalidad.
El 25 de mayo de 2002, la paciente fue remitida al centro, presentándose asintomática y con una exploración física normal. Las serologías para los virus de la hepatitis A, B, C, citomegalovirus, herpes simple, Salmonella, Brucella, Epstein-Barr, VIH y Coxiella burnetti, así como el ARN del VHC, resultaron negativas. Los autoanticuerpos (ANA, ANCA, AMA, SMA, SLA, LKM), inmunoglobulinas, ceruloplasmina, cobre, sideremia, ferritina, alfa-1-antitripsina, hormonas tiroideas, anticuerpos antigliadina y antiendomisio se encontraban dentro de los rangos de normalidad.
La ecografía abdominal y la colangiografía por resonancia magnética no mostraron alteraciones en el hígado, páncreas, vesícula biliar y vías biliares. Las alteraciones analíticas hepáticas mostraron una mejoría progresiva, normalizándose primero la bilirrubina y posteriormente la fosfatasa alcalina. Sin embargo, persistió una elevación de la GGT (241 IU/l) y de la ALAT (66 IU/l). Por este motivo, el 7 de julio se suspendieron el alprazolam y el clorazepato, y se realizó una biopsia hepática.
La biopsia hepática reveló un cilindro hepático con citoarquitectura alterada, manifestada por fibrosis portal. Los espacios porta estaban ligeramente ensanchados, con la formación de finos puentes porto-portales y escasa actividad inflamatoria. El índice de Knodell fue de cinco puntos (1 punto por necrosis erosiva leve focal; 0 puntos por citolisis parenquimatosa; 1 punto por inflamación portal leve y 3 puntos por fibrosis en puentes interportales).
La paciente continuó asintomática. En el último control analítico, en noviembre de 2002, los valores de GGT y ALAT eran de 75 y 51 IU/l, respectivamente.
Análisis de la Causalidad y la Bibliografía
En el caso descrito, se observa una estrecha relación entre la ingesta de los medicamentos y el desarrollo de la lesión hepática. Según los criterios de causalidad de la escala del Council for International Organizations of Medical Sciences (CIOMS) para trastornos hepáticos provocados por fármacos, la puntuación obtenida fue de 6 puntos, lo que clasifica la sospecha de hepatotoxicidad como "probable".
Aunque inicialmente se atribuyó la lesión hepática a la sertralina, la evolución posterior y los hallazgos de la biopsia hepática impiden afirmar con certeza cuál de los psicofármacos fue el agente causal. Se han documentado alteraciones hepáticas asociadas a la sertralina en 1,28 casos por cada 100.000 pacientes-año. Una revisión bibliográfica exhaustiva (utilizando descriptores como sertraline, alprazolam, clorazepate, serotonin uptake inhibitors, benzodiazepines, hepatitis, liver fibrosis, liver cirrhosis en Medline) reveló 4 casos de hepatotoxicidad por alprazolam y uno por cloracepato. En la mayoría de estos pacientes, al igual que en el caso presentado, se administraban concomitantemente otros psicofármacos.
Además, es bien conocida la capacidad de la sertralina para interactuar con múltiples fármacos, incluido el alprazolam, a través de la inhibición del citocromo P450 3A. Por lo tanto, no se descarta la posibilidad de hepatotoxicidad inducida simultáneamente por ambos fármacos.
Es poco probable que los componentes del preparado de plantas medicinales fueran la causa principal del cuadro clínico, dado que se consumían desde casi un año antes. No obstante, podrían haber potenciado los efectos de los fármacos. En la bibliografía revisada, solo se encontraron dos casos de fibrosis hepática relacionados con la administración de fluoxetina y bentazepam, respectivamente.
En conclusión, dada la alta incidencia de los trastornos depresivos y el uso frecuente de ISRS y benzodiacepinas, se subraya la necesidad de la retirada total de estos fármacos ante la sospecha de hepatotoxicidad.
Metabolismo Hepático y Farmacocinética de Psicofármacos
La insuficiencia hepática tiene un impacto significativo en la farmacocinética de los psicofármacos, afectando su absorción, metabolismo, distribución y eliminación. Esto, a su vez, modifica la concentración plasmática, el tiempo de acción y la efectividad de los medicamentos.
Una proporción considerable de la sangre proveniente de las venas hepáticas accede directamente a la circulación sistémica debido a la presencia de shunts porto-sistémicos. Este fenómeno altera el metabolismo de primer paso hepático, resultando en un aumento de la concentración sanguínea del fármaco.
Más del 80% de los psicofármacos se unen a proteínas plasmáticas. En casos de insuficiencia hepática, la síntesis de estas proteínas se ve reducida, lo que incrementa la fracción libre del fármaco en sangre. Fármacos como la venlafaxina, el litio, el topiramato, la gabapentina, la pregabalina, el metilfenidato y la memantina presentan una menor unión a proteínas.
Fases del Metabolismo Hepático de Fármacos
- Fase I: Las enzimas del citocromo P450 (monooxigenasas) son responsables de la hidrólisis, oxidación, desalquilación o reducción de las moléculas de fármacos. Generalmente, este proceso disminuye la actividad farmacológica.
- Fase II: Esta fase implica la conjugación del fármaco con moléculas endógenas, como el ácido glucurónico, sulfato, aminoácidos o acetato. La conjugación aumenta la hidrofilicidad de la molécula y, en la mayoría de los casos, elimina su actividad farmacológica.
Los pacientes con insuficiencia hepática experimentan variaciones significativas en el equilibrio de fluidos, lo que puede afectar a psicofármacos hidrosolubles, como el litio.
Tipos de Lesión Hepática Inducida por Fármacos
Las lesiones hepáticas inducidas por fármacos pueden clasificarse según el patrón predominante de daño:
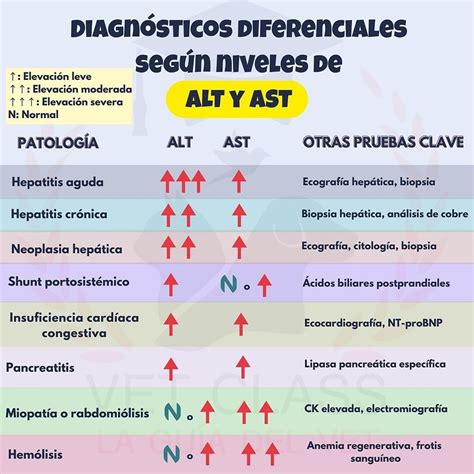
- Lesión Hepatocelular: Caracterizada por un aumento significativo de las concentraciones de aminotransferasas (ALT y AST). Los síntomas pueden incluir malestar general y dolor en el cuadrante superior derecho del abdomen. En casos graves, puede acompañarse de hiperbilirrubinemia (ictericia hepatocelular), lo que se asocia con una mayor mortalidad. Fármacos como el paracetamol y la isoniazida son ejemplos de causantes de este tipo de lesión.
- Lesión Colestásica: Se manifiesta con prurito e ictericia, asociados a un aumento significativo de la fosfatasa alcalina sérica. Generalmente, es menos grave que la lesión hepatocelular, pero la recuperación puede ser prolongada. La amoxicilina/clavulánico y la clorpromazina son ejemplos de fármacos que pueden inducir este tipo de daño. En casos raros, puede derivar en hepatopatía crónica con síndrome de conductos biliares evanescentes.
- Lesión Mixta: En estos casos, no predomina claramente el aumento de aminotransferasas ni de fosfatasa alcalina. Los síntomas también pueden ser una combinación de los anteriores. Fármacos como la fenitoína pueden causar este tipo de lesión.
La lesión hepática inducida por fármacos puede ser predecible (ocurre poco después de la exposición y está relacionada con la dosis, como en la intoxicación por paracetamol) o impredecible (se desarrolla tras un período de latencia y no guarda relación con la dosis). Las lesiones predecibles son una causa frecuente de ictericia e insuficiencia hepática aguda en Estados Unidos, mientras que las impredecibles son una causa rara de enfermedad hepática grave.
Factores de Riesgo y Patrones de Lesión Hepática
Los factores de riesgo para desarrollar lesiones hepáticas inducidas por fármacos no se conocen completamente, pero algunos se asocian a un mayor riesgo para medicamentos específicos:
- Edad ≥ 18 años: puede aumentar el riesgo con amoxicilina-clavulanato, isoniazida.
- Obesidad y diabetes: pueden incrementar la gravedad y la incidencia de lesiones hepáticas inducidas por fármacos con ciertos medicamentos.
- Enfermedad hepática preexistente: puede aumentar el riesgo en pacientes que reciben metotrexato o tratamiento antituberculoso.
- Consumo concomitante de alcohol y tabaco: el riesgo de lesiones hepáticas inducidas por fármacos no está claramente establecido.
- Polimorfismos genéticos: el gen PTPN22, un polimorfismo común, se asocia con lesiones hepáticas inducidas por muchos fármacos.
Antidepresivos y Riesgo de Hepatotoxicidad
La depresión es una de las enfermedades más prevalentes a nivel mundial. Los antidepresivos, cuyo mecanismo de acción se basa en la modulación de neurotransmisores como la serotonina, pueden causar lesión hepática inducida por fármacos (LHID).
Aunque los inhibidores selectivos de la recaptación de serotonina (ISRS) son ampliamente prescritos por su perfil de seguridad en sobredosis y menores efectos secundarios en comparación con los antidepresivos tricíclicos, es crucial ser consciente de que algunos efectos adversos, aunque raros, pueden ser graves.
Se calcula que entre el 0,5% y el 3% de los pacientes tratados con antidepresivos pueden experimentar una leve elevación asintomática de los niveles de aminotransferasas séricas. Todos los antidepresivos tienen el potencial de inducir hepatotoxicidad, especialmente en pacientes de edad avanzada y polimedicados. Se han reportado casos de LHID que ponen en riesgo la vida, incluyendo insuficiencia hepática aguda grave o muerte.
Las lesiones subyacentes suelen ser de tipo hepatocelular, con menor frecuencia colestásica o mixta. Los antidepresivos asociados con un mayor riesgo de hepatotoxicidad incluyen iproniazida, nefazodona, fenelzina, imipramina, amitriptilina, duloxetina, bupropión, trazodona, tianeptina y agomelatina. Por otro lado, el citalopram, escitalopram, paroxetina y fluvoxamina parecen tener un menor potencial hepatotóxico.
La incidencia de daño hepático por antidepresivos "clásicos" (ej. clomipramina, imipramina) es de 1,42-4,0 casos por 100.000 habitantes/año, mientras que para los "nuevos antidepresivos" (ej. fluoxetina, sertralina) es similar (1,28-3,62 casos por 100.000 habitantes/año), con la excepción de la nefazodona, que fue retirada del mercado por este motivo. Por lo tanto, en términos de hepatotoxicidad, ambos grupos de fármacos se consideran igualmente seguros.
Caso de Hepatotoxicidad Aguda por Sertralina
Se describe el caso de un varón de 47 años que acudió a consulta por astenia y molestias abdominales inespecíficas. Tomaba hidroclorotiazida y bisoprolol para la hipertensión arterial y sertralina 50 mg/día desde hacía un mes por disuria. La exploración física reveló ictericia mucocutánea. Los análisis mostraron elevación de GPT (500 UI/l), GOT (191 UI/l), fosfatasa alcalina (377 UI/l), GGT (508 UI/l) y bilirrubina total (2,66 mg/dl), con bilirrubina directa (1,39 mg/dl).
Los marcadores de hepatitis viral y autoinmune fueron negativos, y la ecografía abdominal evidenció signos de colesterolisis vesicular. Con la sospecha de hepatotoxicidad aguda por sertralina, se suspendió su administración, mientras el paciente continuó con bisoprolol e hidroclorotiazida. Tras la retirada de la sertralina, los parámetros hepáticos se normalizaron a los 3 meses. Esta reacción adversa fue comunicada al Sistema Español de Farmacovigilancia.
En este caso, los síntomas de hepatotoxicidad aparecieron un mes después de iniciar el tratamiento con sertralina. Aplicando un algoritmo diagnóstico, todos los datos sugieren toxicidad inducida por este fármaco: las pruebas descartaron hepatitis autoinmune o viral, la elevación de enzimas hepáticas coincidió con el inicio del tratamiento, y aunque el bisoprolol también puede causar elevación de transaminasas, su incidencia es muy baja y el paciente lo tomaba sin problemas previos. La recuperación espontánea tras la retirada de sertralina, a pesar de mantener el bisoprolol, refuerza la hipótesis.
La hepatotoxicidad por sertralina suele manifestarse entre 3 y 8 semanas tras el inicio del tratamiento, con un daño hepatocelular de tipo mixto. El mecanismo exacto no está claro; la sertralina es un inhibidor del citocromo P-450 2D6, lo que podría aumentar la concentración de otros fármacos hepatotóxicos. Asimismo, la incidencia de hepatotoxicidad por sertralina aumenta con dosis superiores a 100 mg, lo que podría sugerir un efecto de auto-inhibición del metabolismo.
Una breve historia de antidepresivos - Neil R. Jeyasingam
Diagnóstico y Tratamiento de la Lesión Hepática Inducida por Fármacos
El diagnóstico de la lesión hepática inducida por fármacos (LHID) se basa en la identificación de patrones característicos en las pruebas de laboratorio, la exclusión de otras causas de hepatopatía y la temporalidad de la aparición de la lesión en relación con la exposición al fármaco.
Las manifestaciones clínicas varían desde síntomas inespecíficos hasta ictericia, compromiso de la síntesis hepática y encefalopatía. La detección temprana mejora el pronóstico.
La clave diagnóstica reside en identificar una hepatotoxina potencial, un patrón de anomalías hepáticas característico de la sustancia y una coincidencia temporal entre la lesión y el perfil del hepatotóxico. La mejora de las pruebas hepáticas tras la suspensión del agente causal es un signo diagnóstico adicional importante.
Dado que no existe una prueba única confirmatoria, es fundamental excluir otras causas de hepatopatía, como las virales, biliares, alcohólicas, autoinmunes y metabólicas.
Criterios para la Lesión Hepática Inducida por Fármacos Significativa
Las lesiones hepáticas inducidas por fármacos clínicamente significativas se definen comúnmente por al menos uno de los siguientes criterios:
- AST o ALT > 5 veces el límite superior normal, o Fosfatasa Alcalina > 2 veces el límite superior normal, en dos ocasiones con al menos 24 horas de diferencia.
- Bilirrubina total > 2,5 mg/dL junto con elevación de transaminasas o fosfatasa alcalina.
- Índice Internacional Normalizado (IIN) > 1,5 con elevación de transaminasas o fosfatasa alcalina.
Se debe evitar la readministración del fármaco sospechoso. Los casos de posible LHID deben ser notificados a los programas de farmacovigilancia.
Manejo Terapéutico
El tratamiento principal de la lesión hepática inducida por fármacos consiste en la suspensión inmediata del fármaco responsable. Si se realiza de forma temprana, suele conducir a la reversión del cuadro.
En casos graves, especialmente si el paciente desarrolla ictericia hepatocelular y compromiso de la función hepática, se debe solicitar interconsulta con un especialista, ya que podría considerarse el trasplante hepático.
Existen antídotos para algunas hepatotoxinas específicas, como la N-acetilcisteína para la intoxicación por paracetamol y la silimarina o penicilina para el envenenamiento por Amanita phalloides. En ciertos casos, los corticosteroides pueden ser útiles en lesiones hepáticas inducidas por fármacos con síndrome DRESS o en lesiones de tipo autoinmune.
Prevención de la Lesión Hepática Inducida por Fármacos
Los esfuerzos para prevenir la LHID comienzan durante el desarrollo de los fármacos. Aunque la seguridad aparente en ensayos preclínicos no garantiza la seguridad en su uso generalizado, la información disponible en bases de datos como LiverTox, mantenida por los National Institutes of Health, puede identificar fármacos potencialmente hepatotóxicos.
No se ha demostrado que el control sistemático de las concentraciones de enzimas hepáticas reduzca la incidencia de hepatotoxicidad.

Consideraciones sobre Estatinas y Enfermedad Hepática
Muchos fármacos, como las estatinas, pueden causar una elevación asintomática de las enzimas hepáticas (ALT, AST, fosfatasa alcalina). Sin embargo, en raras ocasiones, se desarrolla una lesión hepática clínicamente significativa o con compromiso de la función hepática.
No se recomienda suspender el tratamiento con estatinas en pacientes con enfermedad hepática crónica. El uso de estatinas en estos pacientes no difiere de su uso en individuos sin enfermedad hepática basal. De hecho, las estatinas pueden tener propiedades antifibróticas y ser beneficiosas en pacientes con esteatohepatitis asociada a disfunción metabólica (MASH) y enfermedad hepática asociada a disfunción metabólica (MASLD).
Las guías de la American Association for the Study of Liver Disease (AASLD) indican que los pacientes con MASLD tienen un mayor riesgo cardiovascular, pero no un mayor riesgo de lesión hepática grave por estatinas. Estas guías confirman que las estatinas pueden utilizarse para tratar la dislipidemia en pacientes con MASLD, MASH y cirrosis relacionada con MASH.
Las estatinas pueden usarse con precaución en dosis bajas en pacientes con cirrosis descompensada, tras una cuidadosa evaluación del balance riesgo-beneficio.
tags: #isoenzima #implicada #metabolismo #hepatico #antidepresivos