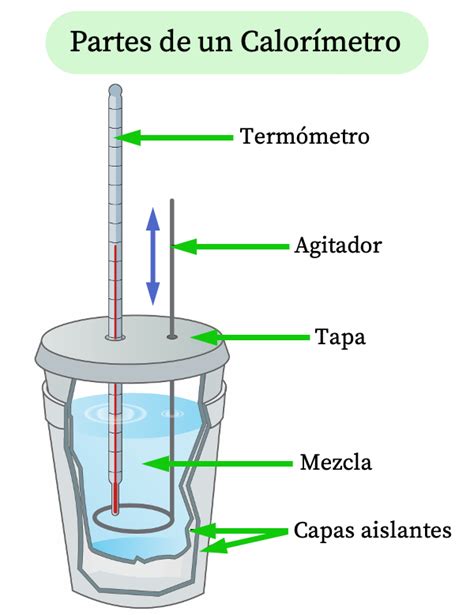
La calorimetría es la rama de la física dedicada a la medición del calor generado en una reacción química o un cambio de estado, utilizando un instrumento conocido como calorímetro. El término "calorímetro" fue acuñado por Antoine Lavoisier, quien en 1780 empleó un conejillo de indias con este dispositivo para cuantificar la producción de calor (Kenny, et al., 2017; De Waele, et al., 2018).
Aplicación de la Calorimetría en Nutrición
En el ámbito de la nutrición, la calorimetría se aplica para determinar el gasto energético total diario (GET). Este valor representa la cantidad de energía, expresada en kilocalorías por día (kcal/día), que un individuo necesita para mantener sus funciones vitales y actividades normales (Delsoglio, et al., 2019).
El GET comprende varios componentes:
- Gasto energético basal (GEB): La energía necesaria para el mantenimiento de las funciones vitales en reposo.
- Termogénesis: El coste energético asociado a la producción de calor por el cuerpo.
- Actividad física: La energía gastada durante el movimiento y el ejercicio.
- Crecimiento: La energía requerida para el desarrollo y la reparación de tejidos.
La actividad física es el componente más variable del GET y el único que puede ser controlado voluntariamente. Su contribución al GET puede oscilar entre el 10% y el 50%, dependiendo del tipo, duración e intensidad del ejercicio (Hernández-Ortega et al., 2019).
A nivel práctico, la determinación del gasto energético basal de un individuo puede ser más precisa que la estimación de su ingesta energética (Nates & Tajchman, 2016). La cuantificación del GEB es fundamental tanto en la clínica como en la epidemiología nutricional, sirviendo como pilar para la correcta estimación de los requerimientos energéticos.
Metodología de Estudio
Se llevó a cabo un estudio descriptivo documental, seleccionando artículos científicos que abordan el tema de la calorimetría. La recopilación de información se realizó a través del buscador Google Académico. Se excluyeron aquellos trabajos que no cumplían con los criterios de inclusión o cuyo contenido temático ya estaba representado en otros documentos considerados.
Google Académico es una herramienta valiosa para localizar documentos académicos como artículos, tesis, libros, patentes y resúmenes de congresos.
El Organismo Humano como Sistema Termodinámico
El cuerpo humano funciona como un sistema termodinámico que requiere energía para mantener sus funciones y la actividad física habitual. El equilibrio entre la energía ingerida (a través de la alimentación) y la energía gastada (en el mantenimiento de la vida y la actividad) es crucial para la estabilidad de las reservas corporales y, por ende, para el mantenimiento del peso corporal (De Waele, et al., 2018). Lograr este equilibrio energético es un objetivo prioritario en las políticas de salud pública, especialmente en las sociedades occidentales.
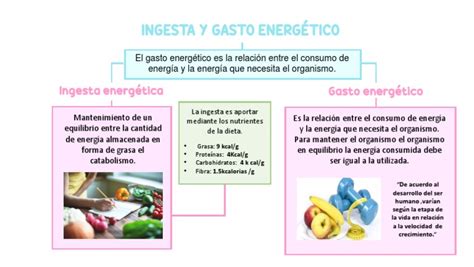
El gasto energético total (GET) en adultos se compone del gasto energético basal (GEB), la termogénesis y la actividad física. Una determinación precisa del GEB es esencial para una estimación adecuada del GET (Muñoz, et al., 2018).
Tipos de Calorimetría
Calorimetría Directa
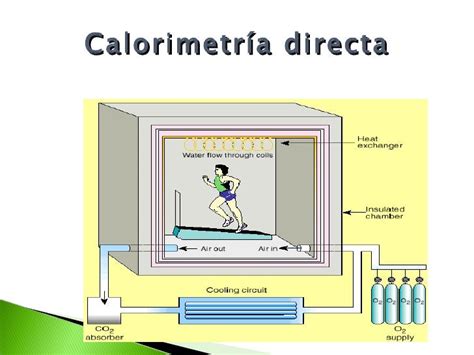
La calorimetría directa mide la producción de calor corporal y es considerada el método más preciso para cuantificar el gasto calórico (Kenny, et al., 2017). Este método se basa en principios termodinámicos y consiste en medir la cantidad de calor liberada por el cuerpo dentro de un calorímetro aislado.
El procedimiento implica introducir a una persona en una cámara aislada con condiciones de temperatura controladas. El calor generado por el individuo es transferido al aire circundante y, posteriormente, a un sistema de agua que rodea la cámara. Midiendo el cambio de temperatura del agua y conociendo su masa, se puede calcular el número de calorías generadas por la persona dentro del calorímetro (Hernández et al., 2019).
Calorimetría Indirecta
La calorimetría indirecta se fundamenta en la teoría de que la energía obtenida de la oxidación de sustratos (nutrientes) es proporcional al consumo de oxígeno (VO2) y a la liberación de dióxido de carbono (VCO2) (Kenny, et al., 2017).
La oxidación de los macronutrientes produce dióxido de carbono, agua y energía, requiriendo un volumen determinado de oxígeno. Aunque la oxidación de proteínas también produce nitrógeno ureico, su contribución calórica es menor, por lo que a menudo se omite en los cálculos para simplificar. El metabolismo energético está intrínsecamente ligado al VO2, ya que la tasa de utilización de ATP (la molécula de energía celular) determina la oxidación de sustratos.
En la mayoría de los procesos metabólicos (excepto la glucólisis anaerobia), la síntesis de ATP está acoplada a la oxidación de sustratos energéticos, liberando una cantidad constante de calor por mol de ATP generado (aproximadamente 75 kJ/mol ATP) (Almajwal & Abulmeaty, 2019).
Dado que las reservas de oxígeno del organismo son limitadas y el consumo de oxígeno medido en la espiración refleja el utilizado por los tejidos, es posible calcular el gasto energético multiplicando el oxígeno consumido por su equivalente calórico, asumiendo la oxidación de un único tipo de macronutriente.
Calorimetría en Circuito Abierto
La calorimetría en circuito abierto requiere la medición precisa del volumen y flujo del aire respiratorio, así como de las fracciones de O2 y CO2 en el aire inspirado y espirado. Estos calorímetros miden las concentraciones de O2 y CO2 en el aire espirado y el flujo de aire, registrando también la temperatura ambiente, la presión atmosférica, la humedad y el tiempo (Becerril, et al., 2015).
Este sistema es adaptable tanto a la ventilación mecánica como a la respiración espontánea (Hernández-Ortega, et al., 2019).
Condiciones para la Determinación del Gasto Energético en Reposo (GER) por Calorimetría Indirecta
Para obtener mediciones precisas del GER mediante calorimetría indirecta, se deben cumplir las siguientes condiciones:
- Reposo físico: El individuo debe estar en posición supina, sin movimientos musculares, durante 30-60 minutos antes de la exploración. No debe estar dormido.
- Reposo mental: Evitar emociones fuertes o estrés psíquico.
- Temperatura ambiente: Mantener una temperatura de entre 20-25°C.
- Ayuno: El sujeto debe haber ayunado durante 6-12 horas antes de la determinación.
Cociente Respiratorio (CR)
El cociente respiratorio (CR) se calcula dividiendo el VCO2 producido entre el VO2 consumido. Un CR de 1 indica la oxidación exclusiva de carbohidratos, mientras que un valor de 0,707 sugiere la oxidación de lípidos. Los valores intermedios reflejan la oxidación de proteínas (Delsoglio, et al., 2019).
El CR es útil para evaluar la adecuación de la pauta nutricional y su efecto respiratorio, permitiendo una aproximación a la oxidación de sustratos.
La oxidación de proteínas puede estimarse a través de la eliminación de nitrógeno ureico, utilizando la relación: proteínas (g) = 6,25 x No. Para minimizar errores, es crucial una correcta recolección de orina de 24 horas. En casos de insuficiencia renal, se deben considerar los cambios en el pool de nitrógeno ureico.
A pesar de su utilidad, la calorimetría indirecta puede presentar limitaciones en cuanto a exactitud, ya que las constantes de consumo de oxígeno varían según factores individuales como género, edad y masa corporal. Además, puede resultar incómoda para el paciente y el equipo médico (Kenny, et al., 2017; Ramírez, et al., 2020).

Evolución y Aplicaciones de la Calorimetría
El estudio de la calorimetría ha experimentado una evolución significativa a lo largo del tiempo. Los principios básicos de la calorimetría, que implican medir el calor transferido hacia o desde una sustancia mediante el intercambio de calor con un objeto calibrado (el calorímetro), siguen siendo fundamentales.
Un calorímetro está diseñado para minimizar la transferencia de calor entre el sistema en estudio y su entorno, permitiendo así mediciones precisas del calor involucrado en procesos químicos, el contenido energético de los alimentos, y otros fenómenos (Figura 5.11).
Históricamente, la calorimetría ha tenido aplicaciones notables. Por ejemplo, la química Reatha Clark King realizó experimentos calorimétricos que fueron de gran importancia para la NASA en su búsqueda de mejores combustibles para cohetes.
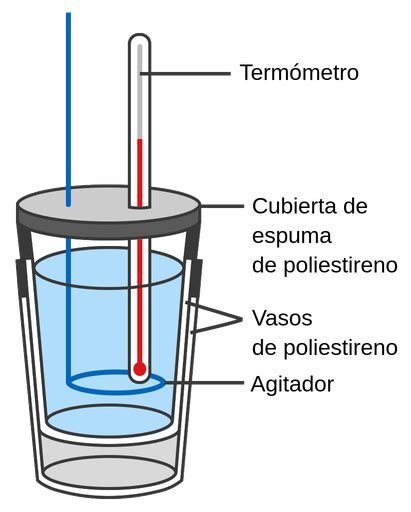
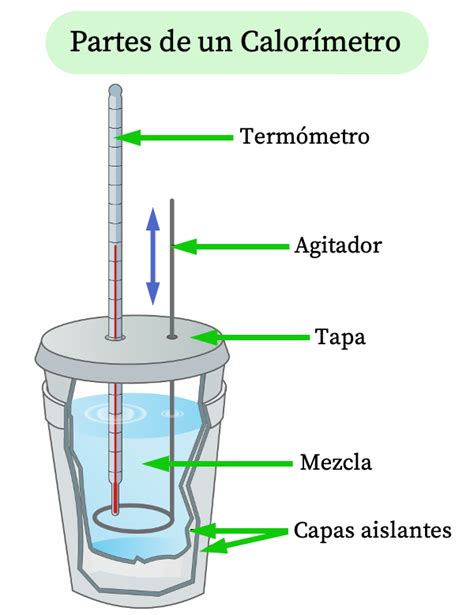
Los calorímetros utilizados en la investigación a menudo son altamente aislados para prevenir la transferencia de calor no deseada. Los estudiantes de química general suelen emplear calorímetros sencillos, como los construidos con vasos de poliestireno (Figura 5.12), mientras que existen también calorímetros de solución comerciales.
Calorimetría en Reacciones Químicas
Los mismos principios de la calorimetría se aplican al estudio de las reacciones químicas. Cuando una reacción exotérmica ocurre en una solución dentro de un calorímetro, el calor liberado es absorbido por la solución, aumentando su temperatura. Por el contrario, en una reacción endotérmica, el calor necesario es absorbido de la energía térmica de la solución, provocando una disminución de la temperatura (Figura 5.11).
Ejemplos de Aplicación
Se han presentado diversos ejemplos de cálculo calorimétrico:
- Transferencia de calor entre sustancias a diferentes temperaturas: Se describe el proceso de equilibrio térmico cuando un objeto caliente se coloca en contacto con uno más frío. Se presentan problemas de cálculo de temperaturas iniciales o calores específicos, involucrando barras de acero, cobre y otros metales, y su interacción con agua.
- Calorimetría en reacciones químicas: Se aborda la neutralización de ácidos y bases fuertes (HCl y NaOH) en un calorímetro de taza de café, calculando el calor liberado por la reacción.
- Reacciones de precipitación: Se calcula el calor producido en la formación de AgCl sólido al mezclar soluciones de NaCl y AgNO3.
- Calentadores de manos: Se explica el principio exotérmico detrás de los calentadores de manos que utilizan la precipitación de acetato de sodio.
- Bolsas de hielo instantáneo: Se describe el proceso endotérmico de disolución de nitrato de amonio en agua, que causa enfriamiento.
- Disolución de sales: Se calcula el calor involucrado en la disolución de KCl en agua, observando una disminución de temperatura.

Calorimetría de Bomba
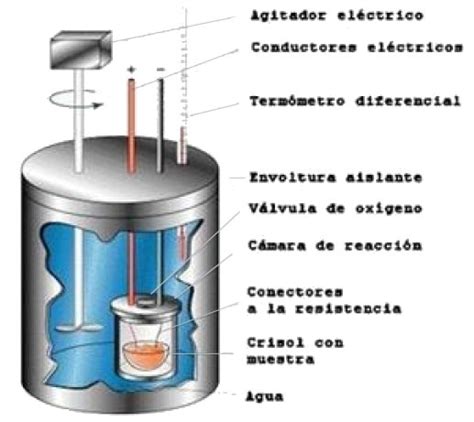
Los calorímetros de bomba operan a volumen constante y se utilizan para medir la energía liberada en reacciones que generan calor significativo y productos gaseosos, como las reacciones de combustión. Estos calorímetros consisten en un robusto recipiente de acero (la "bomba") que contiene los reactivos y está sumergido en agua (Figura 5.17).
La muestra se coloca dentro de la bomba, que se llena de oxígeno a alta presión. Una chispa eléctrica inicia la reacción, y el calor producido es absorbido por la bomba y el agua circundante. El aumento de temperatura se mide para calcular la energía liberada.
Los calorímetros de bomba requieren calibración, que se realiza utilizando una reacción con un calor conocido, como la combustión de ácido benzoico. Se presentan ejemplos de cálculo de la capacidad calorífica del calorímetro y la energía producida en la combustión de glucosa y benceno.
Calorimetría en el Cuerpo Humano
Desde la construcción del primer calorímetro de cuerpo entero en 1899, se han desarrollado diversas tecnologías para medir el calor producido por un ser humano vivo. Los calorímetros de habitación completa permiten realizar actividades cotidianas, generando datos más realistas sobre el gasto energético.
Estos calorímetros se emplean para estudiar el metabolismo de individuos en diferentes condiciones ambientales, dietas y estados de salud (como la diabetes). Por ejemplo, se han utilizado para determinar el gasto energético de mujeres en el posparto, contribuyendo a la elaboración de recomendaciones nutricionales y de ejercicio más precisas.
Calorías y Macronutrientes
En la vida cotidiana, la energía se expresa comúnmente en Calorías (con mayúscula), o kilocalorías (kcal), que son unidades de energía nutricional. Una caloría (cal) equivale a 4,184 julios, mientras que una Caloría (Cal o kcal) equivale a 1.000 cal.
Los macronutrientes de los alimentos, que son las proteínas, los carbohidratos y las grasas, aportan diferentes cantidades de energía:
- Proteínas: Aproximadamente 4 Calorías por gramo.
- Carbohidratos: Aproximadamente 4 Calorías por gramo.
- Grasas y aceites: Aproximadamente 9 Calorías por gramo.
Las etiquetas nutricionales de los alimentos proporcionan información sobre su contenido calórico. Estos valores se obtienen actualmente mediante el sistema Atwater, que utiliza el contenido calórico promedio de los macronutrientes, ajustado por la fibra dietética (un carbohidrato no digerible).
El contenido calórico de los alimentos puede determinarse experimentalmente mediante calorimetría de bomba, quemando una muestra del alimento y midiendo la energía liberada.

Definiciones Históricas y Científicas de Caloría
La definición de caloría ha evolucionado a lo largo del tiempo:
- Caloría (cal): Cantidad de calor necesaria para elevar la temperatura de 1 gramo de agua de 14,5°C a 15,5°C a presión normal.
- Caloría Nutricional (Cal o kcal): Utilizada por Wilbur O. Atwater, es la cantidad de calor necesaria para elevar la temperatura de 1 kilogramo de agua de 0°C a 1°C. Esta unidad se adoptó por conveniencia para la población general.
Antoine Lavoisier, en el siglo XVIII, demostró experimentalmente que el calor producido por los animales era resultado de la combustión de alimentos, similar a una vela encendida, utilizando un calorímetro para medir la producción de calor del conejillo de indias.
Marcelino Berthelot, en la década de 1870, diferenció entre la "caloría pequeña" (g-caloría) y la "Caloría" (kilocaloría).
El trabajo de Atwater en la década de 1880 sentó las bases para la ciencia de la nutrición moderna, investigando el contenido calórico de los alimentos y promoviendo la "alimentación científica" para un equilibrio entre la ingesta y el gasto energético.
Cálculo del Gasto Energético Diario
Para determinar las necesidades calóricas diarias de un individuo, se deben considerar varios factores:
- Gasto energético basal (GEB): La energía mínima requerida para mantener las funciones vitales en reposo.
- Gasto energético por actividad física: La energía consumida durante el ejercicio y las actividades diarias.
- Termogénesis inducida por la alimentación: La energía necesaria para digerir, absorber y metabolizar los nutrientes.
Las ecuaciones predictivas, que consideran género, estatura y edad, son métodos rápidos y sencillos para estimar el GEB, aunque deben aplicarse en condiciones de ayuno y reposo.
El objetivo de la pérdida de peso requiere un déficit calórico, mientras que el aumento de masa muscular implica un aumento de la ingesta calórica, combinado con entrenamiento adecuado. El desequilibrio entre la ingesta y el gasto energético puede llevar al síndrome de "deficiencia energética relativa en el deporte".
El contenido calórico de los alimentos se puede estimar utilizando el sistema Atwater, multiplicando las proporciones de grasa, proteínas y carbohidratos por sus respectivos factores calóricos (9 kcal/g para grasas, 4 kcal/g para proteínas y carbohidratos).
tags: #kilocalorias #totales #metodo #calorimetria