Introducción a las Reacciones de Aminoácidos
Los aminoácidos son los bloques de construcción de las proteínas y desempeñan un papel crucial en numerosos procesos metabólicos dentro del organismo. Su metabolismo es complejo e interconectado, involucrando una serie de reacciones químicas que permiten la síntesis, degradación y transformación de estos compuestos. Dos de las reacciones más importantes en el metabolismo de los aminoácidos son la transaminación y la desaminación.
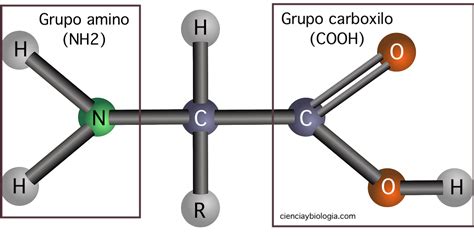
Transaminación: El Intercambio de Grupos Amino
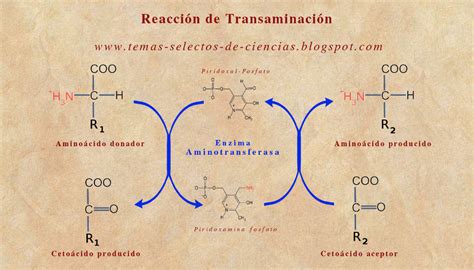
La transaminación, también conocida como aminación, es una reacción bioquímica fundamental en la que un grupo amino (-NH2) se transfiere de un α-aminoácido a un α-cetoácido. Esta reacción es catalizada por enzimas llamadas transaminasas o aminotransferasas, que requieren piridoxal fosfato (PLP), la forma activa de la vitamina B6, como coenzima. El PLP actúa como un transportador temporal del grupo amino.
La reacción general de transaminación se puede representar de la siguiente manera:
α-aminoácido + α-cetoácido ⇌ α-cetoácido + α-aminoácido
En este proceso, el grupo amino del aminoácido original se transfiere al α-cetoácido, convirtiéndolo en un nuevo α-aminoácido. Simultáneamente, el aminoácido original se convierte en su correspondiente α-cetoácido. Las transaminaciones son reacciones reversibles y son esenciales para la síntesis de aminoácidos no esenciales y para la interconversión de aminoácidos en el metabolismo.
Importancia de la Transaminación
- Síntesis de Aminoácidos: Permite la formación de aminoácidos necesarios para la síntesis de proteínas y otras biomoléculas.
- Catabolismo de Aminoácidos: Facilita la eliminación del grupo amino de los aminoácidos antes de que sus esqueletos carbonados sean utilizados para la producción de energía o la síntesis de otros compuestos.
- Interconexión Metabólica: Vincula el metabolismo de los aminoácidos con el ciclo de Krebs y la gluconeogénesis, permitiendo que los esqueletos carbonados de los aminoácidos se utilicen en estas vías.
Desaminación: La Eliminación del Grupo Amino
La desaminación es el proceso mediante el cual se elimina el grupo amino de un aminoácido. Esta reacción es crucial para la eliminación del nitrógeno del cuerpo, principalmente en forma de amoníaco (NH3) o urea. Existen varias vías de desaminación, siendo las más importantes la desaminación oxidativa y la desaminación no oxidativa.
Desaminación Oxidativa
La desaminación oxidativa es la principal vía por la cual se eliminan los grupos amino en muchos aminoácidos. Esta reacción ocurre principalmente en el hígado y es catalizada por la enzima glutamato deshidrogenasa. En esta vía, el grupo amino del glutamato se elimina para formar amoníaco y un α-cetoácido (el α-cetoglutarato). La reacción es reversible y requiere NAD+ o NADP+ como aceptores de electrones.
Glutamato + NAD(P)+ + H2O ⇌ α-cetoglutarato + NH3 + NAD(P)H + H+
El amoníaco producido es tóxico para el organismo y, por lo tanto, se convierte rápidamente en urea en el ciclo de la urea, también en el hígado. La urea es menos tóxica y se excreta a través de los riñones.
Desaminación No Oxidativa
Algunos aminoácidos sufren desaminación no oxidativa, que implica la eliminación directa del grupo amino sin la participación de un aceptor de electrones como NAD+ o NADP+. Estas reacciones son específicas para ciertos aminoácidos y son catalizadas por enzimas diferentes a la glutamato deshidrogenasa. Ejemplos incluyen la deshidratación de la serina, treonina y cisteína, que produce acrilato o α,β-insaturados derivados, y la eliminación de amoníaco de la histidina, que genera urocanato.
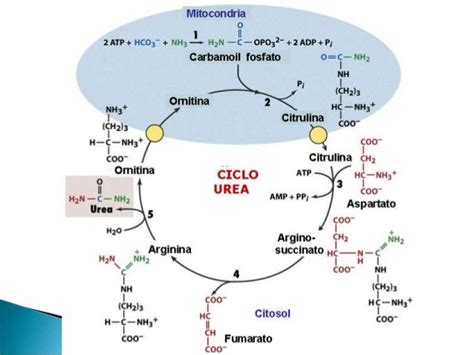
El Ciclo de la Urea: Eliminación del Exceso de Nitrógeno
El ciclo de la urea es una vía metabólica central en el hígado de los animales ureotélicos (como los mamíferos) que convierte el amoníaco tóxico en urea, la cual es luego transportada a los riñones para su excreción. Este ciclo consta de cinco reacciones enzimáticas que incorporan el amoníaco y el dióxido de carbono en compuestos orgánicos, culminando en la formación de urea.
Las etapas clave del ciclo de la urea incluyen:
- Formación de carbamoil fosfato a partir de amoníaco, CO2 y ATP.
- Condensación de carbamoil fosfato con ornitina para formar citrulina.
- Condensación de citrulina con aspartato para formar argininosuccinato.
- Escisión del argininosuccinato para producir arginina y fumarato.
- Hidrólisis de la arginina para liberar urea y ornitina, completando el ciclo.
BIOQUÍMICA ESENCIAL: El Viaje del Amoníaco | Ciclo de la Urea Explicado para Exámenes y Clínica.
Relación entre Transaminación y Desaminación
Las reacciones de transaminación y desaminación están íntimamente relacionadas en el metabolismo de los aminoácidos. La transaminación actúa como un primer paso para recolectar el nitrógeno de varios aminoácidos en forma de glutamato. Posteriormente, la desaminación oxidativa del glutamato por la glutamato deshidrogenasa libera el amoníaco, que luego entra en el ciclo de la urea para su eliminación.
Esta interconexión permite que los restos carbonados de los aminoácidos puedan ser catabolizados para obtener energía o ser convertidos en glucosa o cuerpos cetónicos, mientras que el nitrógeno se maneja de manera segura a través de la formación y excreción de urea.
tags: #mapa #metabolico #trasaminacion #y #desaminacion