El proyecto NeuroCobre se enfoca en desentrañar los complejos mecanismos celulares y moleculares que subyacen a la disfunción del metabolismo del cobre y las mitocondrias en diversas patologías. Entre ellas se incluyen la enfermedad de Menkes (MD), asociada al gen ATP7A; la enfermedad de Wilson (WD), ligada al gen ATP7B; y la enfermedad de Parkinson familiar PARK1, relacionada con el gen SCNA.
Modelos Celulares para el Estudio del Metabolismo del Cobre
Se han empleado diversas líneas celulares para investigar el comportamiento de las proteínas transportadoras de cobre, ATP7A y ATP7B:
- Líneas celulares HBEC-5i (células de la barrera hematoencefálica): En estas células, ATP7A y ATP7B se localizan en la red del Golgi. Estas células presentan resistencia al tratamiento con CuHis (histidinato de cobre).
- Líneas celulares SH-SY5Y: ATP7A y ATP7B también se encuentran en la red del Golgi, pero estas células responden favorablemente al tratamiento con CuHis.
- Fibroblastos de pacientes: En fibroblastos de pacientes, ATP7A y ATP7B se localizan en el Golgi y responden al tratamiento con CuHis y el quelante BCS (bicinchoninic acid).
Enfermedades Asociadas a la Disfunción del Metabolismo del Cobre
Enfermedad de Menkes y Síndrome del Cuerno Occipital (OHS) (ATP7A)
En la enfermedad de Menkes, causada por mutaciones en el gen ATP7A, se observan alteraciones significativas:
- Niveles anómalos de los transportadores de cobre.
- Estrés oxidativo mitocondrial.
- Potencial de membrana mitocondrial alterado.
- Estrés oxidativo celular.
Se han identificado diferencias en estos parámetros entre niños y niñas, entre gemelos, entre la enfermedad de Menkes y el OHS, y se ha observado una posible compensación por parte de ATP7B.
Enfermedad de Wilson (ATP7B)
En contraste, en la enfermedad de Wilson, asociada a mutaciones en el gen ATP7B, los hallazgos son:
- Niveles normales de ATP7A y ATP7B.
- Estrés oxidativo mitocondrial presente.
- Potencial de membrana mitocondrial normal.
- Ausencia de estrés oxidativo celular.
El Cobre: Un Oligoelemento Esencial y Potencialmente Tóxico
Los oligoelementos son elementos químicos vitales para los seres vivos, presentes en cantidades mínimas pero indispensables para el correcto funcionamiento del organismo. Tanto su deficiencia como su exceso pueden acarrear consecuencias negativas para la salud.
El cobre (Cu), con número atómico 29, es un metal de transición crucial en múltiples procesos biológicos. Interviene en la síntesis de glóbulos rojos, la producción de energía en las mitocondrias, la formación de tejido conectivo a través de la enzima lisil-oxidasa, actúa como antioxidante mediante la superóxido dismutasa (SOD), y es fundamental en la formación de melanina.
A pesar de su esencialidad, el cobre presenta una dualidad: es altamente tóxico en su estado oxidado (Cu2+), participando en reacciones que generan especies reactivas de oxígeno (ROS) y provocan peroxidación lipídica, dañando biomembranas y organelas celulares.
Para mantener un equilibrio, existen mecanismos de homeostasis del cobre que regulan su captación, distribución y eliminación. La homeostasis del cobre implica un balance delicado entre la absorción, distribución y excreción del metal.
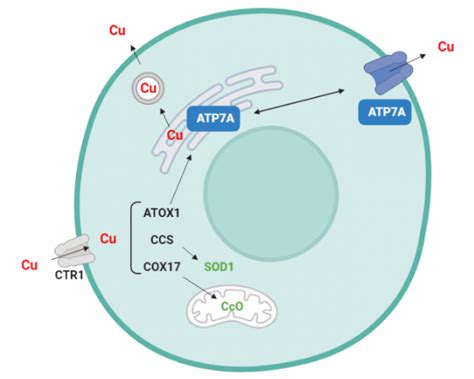
Mecanismos de Transporte y Regulación del Cobre
El mecanismo de transporte del cobre en la célula es complejo y no está completamente dilucidado. Se describen varias vías:
- Reducción y Entrada Celular: La primera etapa involucra la reducción del cobre en la membrana plasmática y su entrada a la célula a través del transportador Ctr1. En levaduras, esta reducción es catalizada por la proteína reductasa FRE1. El transportador humano hCtr1, altamente glicosilado, presenta tres segmentos transmembrana y motivos de metionina (MXXM, MXM) esenciales para la unión y transporte de Cu+. Este proceso no requiere ATP y la proteína Ctr1 se recicla entre la membrana plasmática y los endosomas.
- Distribución Intracelular y Vías de Chaperonas: Una vez dentro de la célula, el Cu+ se distribuye a través de chaperonas específicas hacia diferentes destinos:
- Vía CCS - Cu/Zn superóxido dismutasa (SOD1): La chaperona CCS cede el cobre a la SOD1, una enzima antioxidante crucial localizada en el citoplasma, núcleo y espacio intermembrana de la mitocondria.
- Vía COX17/COX11 - citocromo C oxidasa (COX 1): Las chaperonas COX17 y COX11 facilitan la incorporación del cobre a los centros Cu A y Cu B de la citocromo C oxidasa mitocondrial, una enzima clave en la cadena transportadora de electrones.
- Vía ATOX1-ATP7A/ATP7B: La chaperona ATOX1 (también conocida como HAH1) transfiere el cobre a los transportadores de cobre ATP7A y ATP7B, pertenecientes a la familia de ATPasas tipo P.
- Transportadores ATP7A y ATP7B: Estas ATPasas, localizadas en la red del Golgi y la membrana plasmática, tienen una doble función: suministrar cobre a las cuproenzimas (como la tirosinasa y la ceruloplasmina) y eliminar el exceso de cobre por la bilis. Utilizan la energía de la hidrólisis del ATP para translocar el cobre (Cu+). Su función está acoplada a la fosforilación cíclica, mediada por el motivo DKTG.
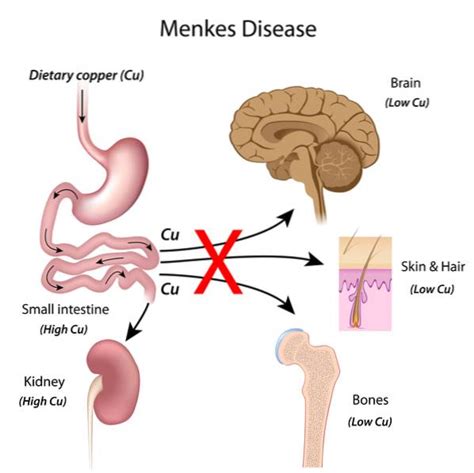
Enfermedad de Menkes (EM): Un Trastorno Grave del Metabolismo del Cobre
La enfermedad de Menkes es un trastorno grave del metabolismo del cobre, causado por mutaciones en el gen ATP7A, localizado en el cromosoma X (Xq13.3). Este gen codifica la proteína ATP7A, responsable de la regulación de los niveles de cobre.
El gen ATP7A se expresa en todos los tejidos excepto en el hígado. Un defecto en esta proteína conduce a deficiencias en el transporte de cobre desde el intestino a la circulación, al sistema nervioso central y al aparato de Golgi para su incorporación en enzimas dependientes de cobre.
Características principales de la Enfermedad de Menkes:
- Herencia: Ligada al cromosoma X con patrón de herencia recesivo. Esto significa que en mujeres, se requieren mutaciones en ambas copias del gen para manifestar la enfermedad, mientras que en hombres, una sola copia mutada es suficiente.
- Síntomas: Afecta el desarrollo físico y mental, manifestándose con cabello ralo y ensortijado, retraso del crecimiento, deterioro progresivo del sistema nervioso, hipotonía muscular, flacidez facial, convulsiones, retraso en el desarrollo y discapacidad intelectual.
- Diagnóstico: Se sospecha por la presencia de síntomas característicos, especialmente cambios típicos del cabello, y niveles reducidos de cobre y ceruloplasmina en sangre. El análisis de catecolaminas en sangre, indicativo de déficit en dopamina beta-hidroxilasa (DBH), una enzima dependiente de cobre, puede ser un examen diagnóstico rápido. La confirmación se realiza mediante pruebas genéticas que identifican mutaciones en el gen ATP7A. Radiografías pueden mostrar alteraciones óseas como osteoporosis y metafisis ensanchadas.
- Tratamiento: No existe cura. El tratamiento es sintomático y se centra en paliar los síntomas y mejorar la calidad de vida. La administración temprana de histidinato de cobre (inyecciones subcutáneas o intravenosas, ya que la absorción oral es defectuosa) puede prevenir signos neurológicos y prolongar la supervivencia, aunque su éxito es variable y depende del tipo de mutación. Se pueden emplear tubos de gastrostomía para asegurar una nutrición adecuada. La penicilamina puede ser administrada junto con el cobre para eliminar el exceso. La terapia génica también se investiga.
- Pronóstico: Generalmente desfavorable, con una alta mortalidad en la primera década de vida. La detección temprana y el inicio del tratamiento en los primeros días de vida son cruciales para un mejor pronóstico.
Una forma más leve de la enfermedad es el Síndrome del Cuerno Occipital (OHS), donde los síntomas aparecen más tarde en la niñez.
La Enfermedad de Menkes
Enfermedad de Wilson (EW): Un Trastorno del Metabolismo del Cobre con Herencia Autosómica Recesiva
La enfermedad de Wilson, también conocida como degeneración hepatolenticular, es un trastorno del metabolismo del cobre con herencia autosómica recesiva, causado por mutaciones en el gen ATP7B (cromosoma 13, región q14.3-q21). Su incidencia es de aproximadamente 1 de cada 30.000 habitantes, con variabilidad geográfica.
El gen ATP7B codifica una ATPasa tipo P implicada en el transporte del cobre al canalículo biliar y al aparato Trans-Golgi. Las mutaciones en este gen impiden la correcta excreción del cobre a la bilis, provocando su acumulación tóxica en diversos tejidos, principalmente en el hígado, el sistema nervioso central, los riñones y la córnea.
Manifestaciones clínicas y diagnóstico:
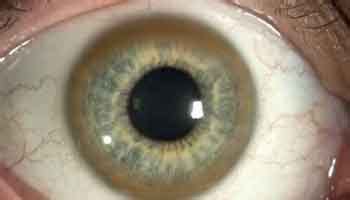
- Síntomas: La EW presenta una gran heterogeneidad clínica, incluso dentro de la misma familia. Las manifestaciones pueden ser hepáticas (ictericia, hepatitis no infecciosa, cirrosis, fallo hepático agudo), neurológicas (temblores, disartria, distonía) y psiquiátricas (cambios de personalidad, irritabilidad, depresión, psicosis). Otras manifestaciones incluyen litiasis biliar, anillo de Kayser-Fleischer en la córnea, cataratas en girasol, alteraciones endocrinológicas, cardiovasculares y renales (síndrome de Fanconi).
- Diagnóstico: Se basa en la combinación de hallazgos clínicos, bioquímicos y genéticos.
- Ceruloplasmina: Niveles < 5 mg/dl son casi diagnósticos. Niveles < 20 mg/dl se observan en el 95% de los pacientes. Sin embargo, puede ser normal en algunos casos o estar descendida en otras condiciones.
- Cobre en tejido hepático: La medición de cobre en biopsia hepática (> 250 μg/g de peso seco) es la prueba más específica.
- Cobre urinario de 24 horas: Suele ser > 40 μg, aumentando significativamente tras la administración de D-penicilamina.
- Anillo de Kayser-Fleischer: Típico, pero no patognomónico, presente en la mayoría de los pacientes con manifestaciones neurológicas.
- Diagnóstico genético: Identificación de mutaciones en el gen ATP7B.
- Tratamiento: Se enfoca en eliminar los depósitos tóxicos de cobre y prevenir su reacumulación. Se utilizan quelantes de cobre como la D-penicilamina o el trietilentetramina, y el acetato de zinc.
La mutación más frecuente en pacientes europeos es la H1069Q, mientras que en España destaca la M645R.
Otros Trastornos Relacionados con el Metabolismo del Cobre
Además de la enfermedad de Menkes y Wilson, existen otros síndromes asociados a alteraciones en el metabolismo del cobre:
- Síndromes Huppke-Brendel: Con herencia autosómica recesiva, se caracterizan por cataratas congénitas y bajos niveles de cobre y ceruloplasmina, causados por mutaciones en el gen slc33a1.
- Síndrome MEDNIK: Se manifiesta con retraso mental, afectación hepática y neuropatías. La toxicidad por cobre es rara y puede deberse a contaminación o ingestión accidental de compuestos de cobre.
Interacción del Cobre con Otros Nutrientes y Procesos Metabólicos
La homeostasis del cobre está intrínsecamente ligada al metabolismo de otros nutrientes y procesos celulares:
- Metabolismo del Hierro: El cobre, a través de la ceruloplasmina (una oxidasa multicobre), es esencial para la correcta movilización y transporte del hierro. La deficiencia de cobre puede llevar a una anemia secundaria por deficiencia de hierro y a una sobrecarga hepática de este metal.
- Interacción con Zinc: Altas ingestas de zinc pueden inducir la síntesis de metalotioneína, una proteína que se une al cobre y reduce su absorción, pudiendo llevar a una deficiencia de cobre.
- Vitamina C: Dosis elevadas de vitamina C suplementaria podrían afectar la actividad oxidasa de la ceruloplasmina, aunque su efecto en la absorción de cobre en humanos es menos claro.
- Metabolismo del Colesterol: Algunos estudios sugieren que en las fases iniciales de la EW, las lesiones podrían estar relacionadas con alteraciones en el metabolismo del colesterol.
Investigación y Avances en el Estudio del Metabolismo del Cobre
La investigación en el campo del metabolismo del cobre es fundamental para comprender las bases moleculares de enfermedades genéticas como la de Menkes y Wilson, y para desarrollar estrategias terapéuticas más efectivas.
Se están llevando a cabo esfuerzos colaborativos, como grupos de trabajo de investigación y registros internacionales, para recopilar información, mejorar el diagnóstico y avanzar en el conocimiento de estas patologías. La medicina de precisión y la ampliación de la formación del personal médico en este ámbito son clave para un mejor abordaje clínico.
La Enfermedad de Menkes
tags: #metabolismo #del #cobre #atp7a