El metanol, también conocido como alcohol metílico, alcohol de madera o espíritus de madera, es el alcohol saturado monohídrico más simple. Su fórmula química es CH3OH, con un peso molecular de 32.04 y un punto de ebullición de 64.7 °C. Históricamente, se obtenía por destilación seca de la madera, de ahí su nombre común "alcohol de madera". Actualmente, su producción industrial se basa en un proceso catalítico a partir de monóxido de carbono, dióxido de carbono e hidrógeno.
Este compuesto se presenta como un líquido ligero, incoloro, volátil, inflamable y con un olor similar al del etanol, pero a diferencia de este último, el metanol es altamente tóxico y no es apto para el consumo. Se utiliza ampliamente como disolvente, anticongelante, combustible y desnaturalizante del etanol. También juega un papel en la producción de biodiésel mediante reacciones de transesterificación.
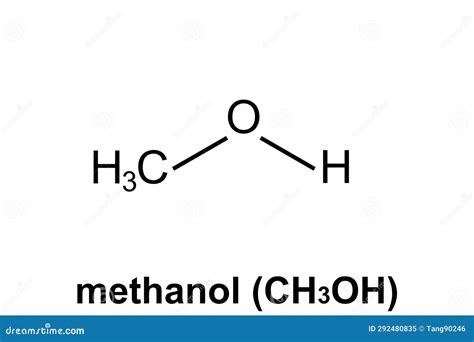
Propiedades fisicoquímicas del metanol
El metanol posee una serie de propiedades fisicoquímicas que determinan su comportamiento y aplicaciones:
- Apariencia: Líquido incoloro y transparente, con olor irritante.
- Punto de fusión: -97.8 °C
- Punto de ebullición: 64.7 °C
- Densidad relativa (agua = 1): 0.792
- Densidad del vapor (aire = 1): 1.16
- Presión de vapor saturada: 12.3 kPa (a 20 °C)
- Calor de combustión: -7238 kJ/mol
- Solubilidad: Soluble en agua, miscible con alcoholes, éter etílico y la mayoría de los disolventes orgánicos.
- Punto de inflamación: 12 °C (cerrado) / 11 °C (abierto)
- Temperatura de ignición: 464 °C
- Límites de explosividad: Límite inferior 6.5%, Límite superior 36.5%
Otras propiedades relevantes incluyen su índice de refracción, viscosidad, calor de vaporización y conductividad térmica, que varían con la temperatura.
Reactividad y reacciones químicas
El metanol exhibe las propiedades químicas características de los alcoholes saturados monohídricos, aunque su simplicidad estructural le confiere reacciones particulares:
Reacciones de combustión
El metanol reacciona con el oxígeno, quemándose violentamente en oxígeno puro para generar vapor de agua y dióxido de carbono:
2CH3OH + 3O2 → 2CO2 + 4H2O
En el aire, la combustión es:
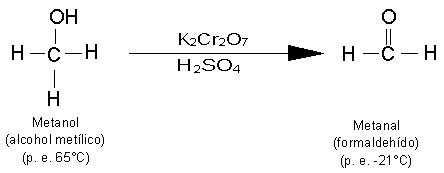
2CH3OH + O2 → 2HCHO + 2H2O
Esta reacción inicial produce formaldehído (HCHO), que a su vez puede oxidarse a ácido fórmico (HCOOH) y finalmente a dióxido de carbono y agua:
2HCHO + O2 → 2HCOOH
2HCOOH + O2 → 2H2O + 2CO2
Otras reacciones
- Formación de compuestos de coordinación: El metanol forma sustancias cristalinas con sales como el cloruro de calcio (CaCl2·4CH3OH) y compuestos moleculares con óxido de bario (2CH3OH·BaO).
- Aminación: A altas temperaturas (370℃~420℃), el metanol puede reaccionar con amoníaco para formar metilaminas: NH3 + CH3OH → CH3NH2 + H2O NH3 + 2CH3OH → (CH3)2NH + 2H2O NH3 + 3CH3OH → (CH3)3N + 3H2O
- Reacción con halógenos: Aunque no reacciona fácilmente con cloro o bromo elementales, sus soluciones acuosas pueden generar éter diclorometílico, que se hidroliza a formaldehído y ácido clorhídrico.
- Descomposición: Al calentarse con álcalis o cal, produce hidrógeno y formiato de sodio. La destilación con polvo de zinc lo descompone en monóxido de carbono y agua.
Usos y aplicaciones industriales
El metanol es una materia prima orgánica fundamental con una amplia gama de aplicaciones industriales:
- Producción de formaldehído: Es su principal aplicación, generando formaldehído que se utiliza en la fabricación de adhesivos para la industria maderera, así como en plásticos, recubrimientos, textiles y papel.
- Producción de ácido acético: Constituye aproximadamente el 7% de la demanda mundial de metanol y se emplea en la producción de acetato de vinilo, fibras de acetato y ésteres.
- Síntesis de otros compuestos:
- Cloruro de metilo, metilamina y sulfato de dimetilo.
- Pesticidas (insecticidas, acaricidas) y productos farmacéuticos.
- Dimetil tereftalato, metil metacrilato y acrilato de metilo.
- Formiato de metilo, utilizado para producir ácido fórmico y formamida.
- Carbonato de dimetilo, un compuesto ecológico.
- Etilenglicol, materia prima para poliéster y anticongelante.
- Dimetil éter, un combustible limpio y eficiente.
- Combustible: Se utiliza como combustible alternativo, en mezclas con gasolina (como aditivo para mejorar el índice de octano, por ejemplo, MTBE), y en vehículos de combustible flexible. También se emplea en estufas de camping y náuticas debido a su combustión limpia y eficiente.
- Proteína de metanol: Obtenida por fermentación microbiana, es una fuente proteica de alto valor nutricional, utilizada como sustituto de harinas de pescado y soja.
- Disolvente y agente de limpieza: Se emplea en la industria electrónica, como reactivo analítico y en síntesis orgánica.
- Promotor de crecimiento de cultivos: Puede mejorar el rendimiento de los cultivos y la eficiencia del uso del agua.
Procesos Petroquímicos - Metanol Parte 2
Toxicología y efectos en la salud
El metanol es altamente tóxico para los seres humanos y animales, principalmente debido a sus metabolitos.
Metabolismo y toxicidad
Una vez ingerido, inhalado o absorbido a través de la piel, el metanol es metabolizado en el hígado por la enzima alcohol deshidrogenasa (ADH) a formaldehído. Posteriormente, la aldehído deshidrogenasa (ALDH) convierte el formaldehído en ácido fórmico. Es el ácido fórmico el principal responsable de la toxicidad del metanol, ya que interfiere con la cadena respiratoria mitocondrial, inhibe la citocromo oxidasa y provoca hipoxia tisular y acidosis metabólica severa.
La toxicidad del metanol afecta principalmente al sistema nervioso central (SNC) y al sistema óptico. Las células de la retina son particularmente sensibles al ácido fórmico, ya que no poseen mecanismos alternativos eficientes para la producción de ATP, lo que conduce a la necrosis retiniana.
Dosis tóxica y efectos clínicos
La dosis letal de metanol varía, pero se estima que alrededor de 70 ml pueden ser mortales. La intoxicación por metanol puede ocurrir por ingestión de bebidas alcohólicas adulteradas, exposición ocupacional o gestos autolíticos.
Los síntomas de intoxicación pueden manifestarse con un período de latencia de 12 a 24 horas, y pueden incluir:
- Síntomas iniciales: Malestar gastrointestinal inespecífico, náuseas, vómitos, dolor abdominal, mareos y embriaguez.
- Alteraciones visuales: Visión borrosa, moteada, fotofobia, disminución de la agudeza visual, y en casos graves, ceguera total.
- Acidosis metabólica: Caracterizada por un aumento del anion gap (normalmente entre 10-16 mmol/l) debido a la acumulación de ácido fórmico.
- Deterioro neurológico: Dolor de cabeza, somnolencia, confusión, convulsiones, coma y en casos extremos, muerte por parada cardiorrespiratoria.
Toxicidad ecológica
El metanol es biodegradable y su toxicidad ecológica es relativamente baja en comparación con otras sustancias. Su vida media en aguas subterráneas es corta (1-7 días).
Diagnóstico y tratamiento de la intoxicación por metanol
El diagnóstico de la intoxicación por metanol puede ser un desafío, especialmente si la sospecha clínica no es temprana. La confirmación analítica mediante cromatografía de gases suele realizarse en sangre u orina.
Diagnóstico
Ante la sospecha clínica, especialmente ante síntomas visuales o neurológicos acompañados de acidosis metabólica, se deben considerar las siguientes aproximaciones:
- Historia clínica y examen físico: Evaluación de síntomas, antecedentes de exposición y examen neurológico y oftalmológico.
- Gasometría arterial: Para detectar acidosis metabólica y calcular el anion gap.
- Osmolaridad sérica: Cálculo del osmolar gap para estimar la presencia de sustancias osmóticamente activas.
- Análisis toxicológico específico: Cuantificación de metanol en sangre.
Tratamiento
El tratamiento de la intoxicación por metanol es una emergencia médica y debe iniciarse lo antes posible para evitar la formación de metabolitos tóxicos.
- Antídotos:
- Etanol: Compite con el metanol por la enzima alcohol deshidrogenasa, bloqueando su metabolismo. Se administra hasta que los niveles de metanol en sangre sean indetectables y la acidosis se corrija.
- Fomepizol (4-MP): Un inhibidor más potente y con menos efectos secundarios que el etanol.
- Soporte metabólico:
- Bicarbonato sódico: Para corregir la acidosis metabólica.
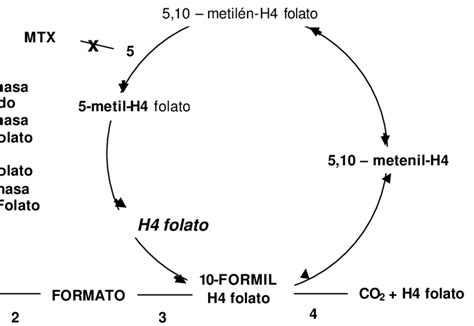
- Ácido fólico: Estimula la metabolización del ácido fórmico a CO2.
- Hemodiálisis: Considerada en casos de alteración visual severa, acidosis metabólica grave, o niveles elevados de metanol en sangre.
tags: #metabolismo #global #del #metanol