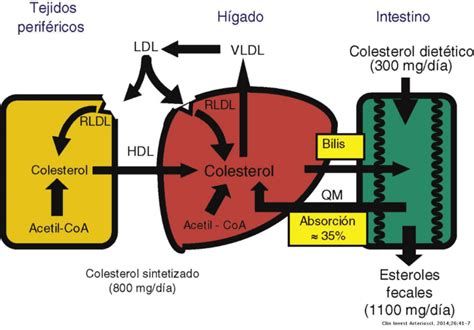
Las estatinas, inhibidores de la 3-hidroxi-3 metilglutaril-coenzima A-reductasa, han sido fundamentales en la reducción del colesterol unido a las lipoproteínas de baja densidad (LDL) y, consecuentemente, en la disminución de la morbimortalidad cardiovascular. A pesar de su eficacia y perfil de seguridad general, no están exentas de efectos indeseables, siendo el riesgo de diabetes de nuevo comienzo una preocupación creciente.
Estatinas y el Riesgo de Diabetes
El descubrimiento en 2008 de una elevada tasa de diabetes de nuevo comienzo en pacientes tratados con rosuvastatina en el estudio JUPITER, con un incremento del riesgo del 26% respecto al placebo, puso de manifiesto esta potencial asociación. Un subanálisis posterior evidenció un mayor incremento del riesgo en mujeres. En contraste, el estudio WOSCOPS, con pravastatina, sugirió una reducción del riesgo de diabetes, aunque con criterios diagnósticos no estandarizados.
Estos hallazgos sugieren que el efecto diabetogénico de las estatinas puede ser dependiente del tipo de estatina y de la dosis empleada. Un análisis de 2015, que incluyó a cerca de 500.000 pacientes, proporcionó datos sobre el riesgo de diabetes mellitus tipo 2 asociado a diferentes estatinas:
- Rosuvastatina: 42%
- Atorvastatina: 25%
- Simvastatina: 14%
- Fluvastatina: 4%
- Pravastatina: 2%
En cuanto a la pitavastatina, los estudios comparativos son limitados. Sin embargo, al evaluar su efecto sobre el control glucémico (2 mg/día) frente a otras estatinas (atorvastatina o pravastatina), se ha demostrado que no aumenta la glucemia plasmática ni la hemoglobina glucosilada. Metanálisis posteriores han intentado robustecer estas observaciones. Un estudio clave de 2010, que analizó trece ensayos clínicos randomizados con más de 91.000 pacientes, situó el riesgo de aparición de diabetes en un 9%.
Un metaanálisis reciente, centrado en los efectos individualizados de la pitavastatina en comparación con placebo y otras estatinas en individuos sin antecedentes de diabetes, constató un nulo efecto de la pitavastatina en el metabolismo glucídico, independientemente de la dosis.
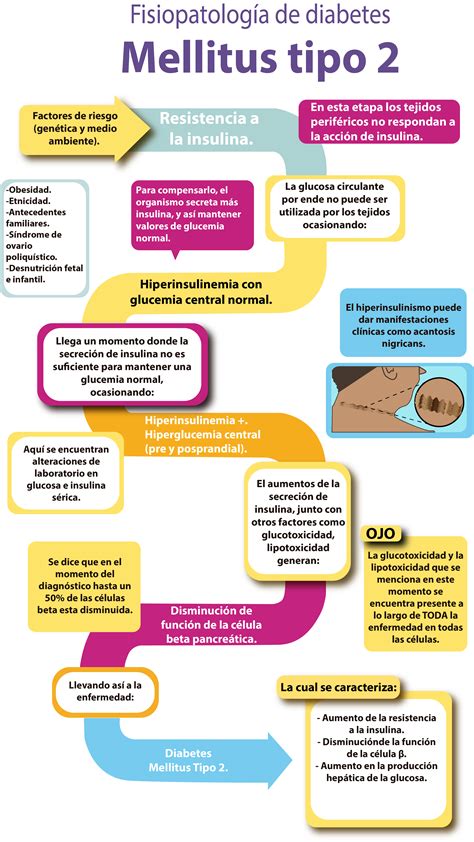
Factores de Riesgo para el Desarrollo de Diabetes con Estatinas
Independientemente del tipo, potencia, dosis o duración del tratamiento con estatina, ciertas personas son más susceptibles a desarrollar diabetes. Se incluyen aquí individuos con factores de riesgo de síndrome metabólico, particularmente aquellos asociados a un mayor riesgo de diabetes:
- Índice de Masa Corporal (IMC) superior a 30 kg/m²
- Hipertensión arterial
- Niveles de triglicéridos superiores a 150 mg/dl
- Glucemia plasmática en ayunas superior a 100 mg/dl
El género también es un factor diferencial; el subanálisis del estudio JUPITER mostró un riesgo del 14% para los hombres y del 49% para las mujeres posmenopáusicas. La raza es otro factor a considerar.
Mecanismos Moleculares de la Diabetogenicidad de las Estatinas
Las estatinas bloquean la producción de intermediarios en la vía del colesterol, como los isoprenoides, geranilpirofosfato, farnesilpirofosfato y coenzima Q10. Estos productos regulan la producción de transportadores de glucosa como GLUT4. Al bloquear su síntesis, se reduce la expresión de GLUT4, lo que disminuye la captación celular de glucosa en tejido adiposo, músculo e hígado, generando un perfil metabólico de resistencia a la insulina. La reducción de la coenzima Q10 es particularmente relevante, y su suplementación ha demostrado revertir esta situación.
La Pitavastatina como Excepción
La pitavastatina, a pesar de ser una estatina de potencia media-alta, ha demostrado un efecto nulo en los parámetros del metabolismo hidrocarbonado y una menor progresión a la diabetes en prediabéticos. Esto la convierte en una opción a considerar en pacientes con riesgo de desarrollar diabetes.
Dada la evidencia, es crucial establecer criterios para minimizar el riesgo de diabetes en pacientes tratados con estatinas, especialmente en aquellos con factores de riesgo metabólicos o en situación de prediabetes. Esto debe complementarse con la optimización de un estilo de vida saludable y el control de otros factores de riesgo, como la hipertensión, teniendo en cuenta el efecto sobre el metabolismo hidrocarbonado de ciertos fármacos antihipertensivos, como los betabloqueantes y los diuréticos tiazídicos.
Betabloqueantes y el Metabolismo Glucídico
Los betabloqueantes, utilizados comúnmente para tratar la hipertensión y otras afecciones cardiovasculares, también pueden influir en el metabolismo de la glucosa. Los receptores beta-2 desempeñan un papel en la producción hepática de glucosa, y su bloqueo no selectivo (ej. propranolol) puede contribuir a la hipoglucemia. Aunque los betabloqueantes beta-1 selectivos (ej. atenolol, metoprolol) se creía que no provocaban hipoglucemia, se ha observado que en pacientes con necesidades energéticas o metabolismo anormales, su administración puede asociarse a hipoglucemia.
Estudios como el LIFE (con atenolol) y el COMET (con metoprolol) han mostrado un aumento del 22% al 28% en la diabetes de nueva aparición con betabloqueantes tradicionales, que pueden incrementar la resistencia a la insulina y empeorar el control glucémico.
Efectos Secundarios de los Betabloqueantes en Pacientes Diabéticos
Los efectos secundarios de los betabloqueantes en pacientes diabéticos incluyen:
- Aumento de la resistencia a la insulina con empeoramiento del control glucémico.
- Mayor frecuencia de hipoglucemia y dificultad en su reconocimiento (aunque este problema es menor en pacientes con diabetes tipo 2).
Sin embargo, existen pruebas de que algunos betabloqueantes pueden tener "propiedades de sensibilización a la insulina". El carvedilol, un betabloqueante no selectivo con propiedades vasodilatadoras y sensibilizantes a la insulina, se considera una opción ideal para pacientes diabéticos.
En el estudio comparativo entre carvedilol y metoprolol, se observó que la hemoglobina glicosilada aumentó con metoprolol pero no con carvedilol. La sensibilidad a la insulina mejoró con carvedilol pero no con metoprolol, y se evidenció una menor incidencia de microalbuminuria en pacientes que recibieron carvedilol.
BLOQUEADORES ALFA Y BETA ADRENÉRGICOS (FÁRMACOS ANTIHIPERTENSIVOS) | GuiaMed
El Riñón y la Homeostasis de la Glucosa
Históricamente, el riñón no se consideraba un órgano clave en la homeostasis de la glucosa. Sin embargo, ahora se sabe que participa a través de la gluconeogénesis y la reabsorción de glucosa en los túbulos contorneados proximales. Los glomérulos filtran aproximadamente 180 g de glucosa al día, y en circunstancias normales, casi toda se reabsorbe. El transportador SGLT2 es responsable del 90% de esta reabsorción, mientras que SGLT1 se encarga del 10% restante.
En pacientes con diabetes mellitus tipo 2, se ha observado un incremento en la expresión y actividad de SGLT2, lo que podría contribuir a una mayor reabsorción de glucosa y, por ende, a la hiperglucemia. La glucosuria renal familiar, una condición genética que afecta al transportador SGLT2, ha servido como modelo para estudiar los efectos de su inhibición.
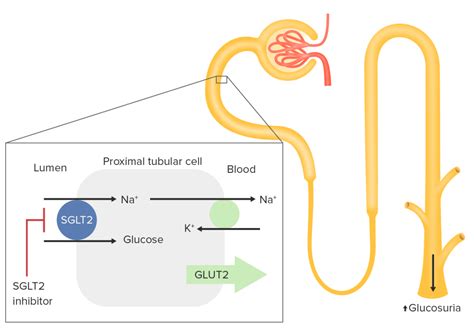
Inhibidores del Transportador SGLT2 para el Tratamiento de la Diabetes Tipo 2
Los inhibidores del transportador SGLT2, derivados de la florizina, representan una nueva clase de fármacos para el tratamiento de la diabetes mellitus tipo 2. Al bloquear la reabsorción de glucosa en el riñón, estos fármacos inducen glucosuria, reduciendo así los niveles de glucosa plasmática y la glucotoxicidad. Fármacos como la dapaglifozina y la canaglifozina se encuentran en ensayos clínicos avanzados.
La dapaglifozina, por ejemplo, se absorbe rápidamente y tiene una vida media de aproximadamente 16 horas. Ha demostrado un efecto hipoglucemiante en ensayos clínicos de fase II y III, con dosis diarias de 2.5, 5 y 10 mg.
tags: #metabolismo #glucidico #con #beta #bloqueadores