Introducción a los Gases Ideales y Reales
La comprensión del comportamiento de los gases es fundamental en química y física. Si bien el modelo de gas ideal proporciona una base simplificada para muchos cálculos, los gases reales presentan desviaciones que requieren modelos más complejos, como la ecuación de Van der Waals.
Comportamiento de Gases Específicos
Dióxido de Carbono (CO2)
En un escenario dado, 1 mol de dióxido de carbono a 373 K ocupa un volumen de 536 mL a una presión de 50,0 atmósferas. Este dato permite analizar su comportamiento bajo condiciones específicas.
Aire como Gas Ideal y Real
Se sabe que a una presión de 127 atm y a una temperatura de 27 °C, el aire se comporta de forma ideal. Las fracciones molares de los componentes del aire son aproximadamente: N2: 0,78; O2: 0,21; otros: 0,01, y el peso molecular medio del aire es 28,96 g/mol. A partir de esta información, se pueden realizar varios cálculos:
- El volumen molar teórico del aire en condiciones ideales.
- La masa de aire en un volumen determinado.
- La densidad del aire bajo ciertas condiciones.
Helio y Hidrógeno en Globos Aerostáticos
Se desea llenar un globo esférico con helio, con un diámetro de 30 metros, una presión interna de 740 mmHg y una temperatura de 27 °C. Suponiendo comportamiento ideal, se puede determinar la masa de helio necesaria.
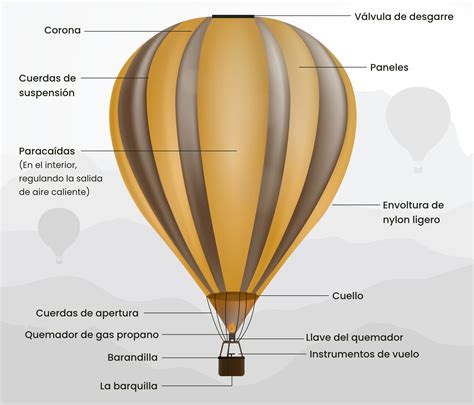
Posteriormente, se analiza qué volumen alcanzaría el globo si se reemplaza el helio por el mismo número de moles de hidrógeno, manteniendo las mismas condiciones de presión y temperatura. Se considera el peso atómico del hidrógeno como 1.
Adicionalmente, se estudia la extracción de helio de un globo para mantener su diámetro constante (30 m) mediante un aumento de la temperatura a 127 °C, manteniendo la presión constante.
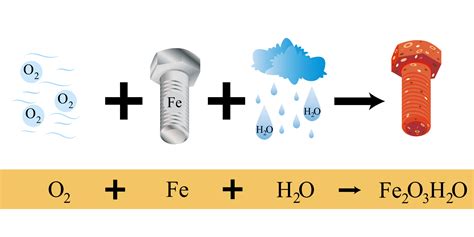
Ozono (O3)
Considerando al ozono como un gas ideal, se calcula el volumen que ocuparán 48 g de ozono a presión atmosférica y temperatura de 0 °C. Esto equivale a un volumen molar estándar.
Se explora el volumen que ocuparía el producto de la atomización completa de las moléculas de ozono, asumiendo que cada molécula de O3 se disocia en átomos de oxígeno.
Se analiza la reacción del ozono gaseoso con cobre metálico en un reactor con émbolo móvil, manteniendo la presión atmosférica (1 atm) y la temperatura constante (0 °C). Se determina el volumen que ocupará el producto gaseoso de la reacción, asumiendo una conversión del 100% del ozono y la estequiometría exacta de la reacción.
Hidrógeno en un Globo Aerostático en Altitud
Se desea llenar con hidrógeno un globo aerostático en la cima de una montaña, donde la temperatura ambiente es de -12 ºC y la presión es de 628 mmHg. El globo vacío (incluida la barquilla) pesa 216 kg y comienza a elevarse cuando el volumen de hidrógeno alcanza los 210 m³ en esas condiciones de presión y temperatura. Se calcula la masa de hidrógeno introducida, asumiendo un comportamiento ideal.
Se determina qué volumen de helio se habría necesitado para que el globo alcanzara el mismo peso que en el apartado anterior, en las mismas condiciones de presión y temperatura.
Ecuación de Van der Waals y Comportamiento de Gases Reales
Aplicación a CCl4
La ecuación de Van der Waals (p + n²a/V²) (V - nb) = nRT se propone para explicar el comportamiento de los gases reales. Para el gas CCl4, los coeficientes son: a = 20,4 L²atm/mol² y b = 0,1383 L/mol. Se calcula la presión ejercida por 153,81 g de CCl4 contenidos en un recipiente de 22,4 L a 273 K, asumiendo primero un comportamiento ideal.
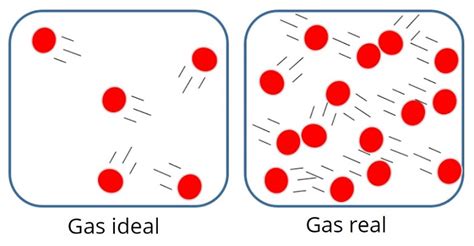
Posteriormente, se compara la presión calculada con la que ejercería el mismo gas si se considerara el modelo de Van der Waals, analizando si es mayor o menor que la del gas ideal y por qué.
Se identifican los valores de los coeficientes 'a' y 'b' para CCl4, así como una unidad de presión común en experimentos de gases.
Análisis de Mezclas Gaseosas
Mezcla de Nitrógeno, Argón y un Gas Desconocido
Una mezcla de 14 g de nitrógeno, 40 g de argón y 44 g de un gas desconocido ocupa un volumen de 99,9 L bajo una presión de 1 atm a una temperatura de 25 °C. Se determina la masa molecular del gas desconocido, asumiendo comportamiento de gas ideal.
Se analiza la presión de la mezcla en mmHg si se encontrara en condiciones estándar de volumen molar (22,4 L) y masa molecular del gas desconocido.
A la mezcla inicial se añaden 14 g de un cuarto gas con fórmula empírica CH2. Manteniendo la presión a 1 atm y la temperatura a 25 °C, se determina si es posible calcular el volumen que ocupará la nueva mezcla y cuál sería este volumen.
Densidad y Presión del Aire
La densidad del aire seco es de 1,204 g L⁻¹ a 20 °C y 1 atm de presión. Se comprime isotérmicamente una cierta cantidad de aire seco a 1 atm hasta un volumen tal que la nueva densidad es de 3,6 g L⁻¹. Se calcula la nueva presión del gas.
Se describe la relación gráfica entre la densidad de un gas y su presión bajo compresión isotérmica.
Se determina la masa molecular aproximada del aire seco basándose en la información proporcionada.