El estudio de las reacciones químicas a nivel industrial o de laboratorio requiere un conocimiento previo de la energía involucrada. Es fundamental determinar si un proceso será exotérmico (libera calor) o endotérmico (absorbe calor), así como la magnitud de dicha energía. Sin esta información, el desarrollo y la implementación de cualquier proceso químico a gran escala serían inviables.
Los datos obtenidos tanto teórica como experimentalmente presentan una alta correlación. Es importante destacar que nunca se encontrará una discrepancia drástica donde un cálculo teórico prediga un calor de reacción endotérmico y un experimento arroje un valor exotérmico, o viceversa. Los valores experimentales y teóricos de calor de reacción son consistentes.
Entalpía Estándar de Formación y Reacción
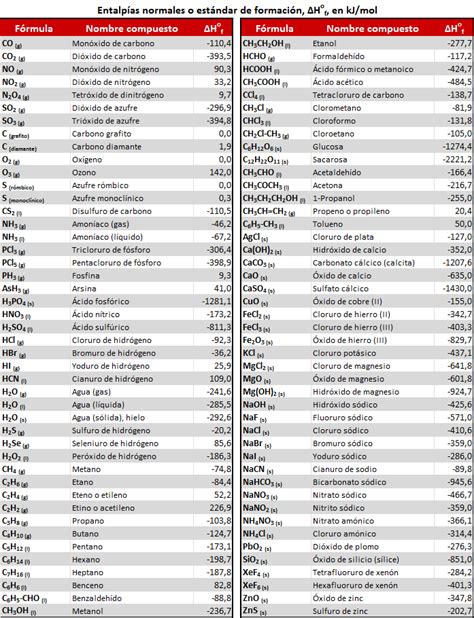
Las entalpías estándar de formación de diversas sustancias se presentan comúnmente en tablas. Estas entalpías son cruciales para calcular la entalpía de reacción estándar. La fórmula general para este cálculo es la diferencia entre la sumatoria de las entalpías de formación de los productos y la sumatoria de las entalpías de formación de los reactantes:
ΔH°reacción = Σ ΔH°f (productos) - Σ ΔH°f (reactantes)
Es imperativo tener en cuenta que cada valor de entalpía de formación, tanto de reactantes como de productos, debe ser multiplicado por su respectivo índice estequiométrico presente en la reacción balanceada.
Reacción de Combustión del Acetileno (C₂H₂)
El acetileno (C₂H₂) es un compuesto que, al reaccionar con oxígeno, libera una cantidad significativa de energía. La reacción de combustión del acetileno es la siguiente:
$$C_{2}H_{2(g)} + \frac{5}{2}O_{2(g)} \rightarrow 2CO_{2(g)} + H_{2}O_{(l)}$$
Esta ecuación nos indica que por cada mol de acetileno que reacciona, se producen 2 moles de dióxido de carbono (CO₂) y 1 mol de agua (H₂O), liberando una cantidad específica de calor.
Cálculo del Calor de Combustión
Se ha determinado que el calor de combustión del acetileno (C₂H₂) es de 312.0 kcal/mol. Este valor representa la energía liberada cuando un mol de acetileno se quema completamente.

Entalpía de Formación del Acetileno
La entalpía de formación del acetileno (C₂H₂) es de -312.0 kcal/mol. Este valor negativo indica que la formación de un mol de acetileno a partir de sus elementos en estado estándar es un proceso exotérmico, es decir, libera energía.
Determinación de la Producción de CO₂ por Kilocaloría
Para calcular la cantidad de litros de dióxido de carbono (CO₂) a Temperatura y Presión Normales (TPN) que se desprenden por cada kilocaloría producida durante la combustión del acetileno, seguimos los siguientes pasos:
- Relación Molar: A partir de la ecuación balanceada de combustión, sabemos que 1 mol de C₂H₂ produce 2 moles de CO₂.
- Energía Liberada: El calor de combustión del acetileno es de 312.0 kcal por cada mol de C₂H₂ que reacciona.
- Conversión de Unidades (Opcional pero útil para otros cálculos): Si fuera necesario convertir la energía a kilojulios (kJ), se utiliza el factor de conversión 1 kcal = 4.184 kJ. Por lo tanto, 312.0 kcal/mol equivalen a 1305.408 kJ/mol (312.0 kcal/mol * 4.184 kJ/kcal).
- Cálculo de Litros de CO₂ por Mol de Acetileno: A TPN, 1 mol de cualquier gas ocupa 22.4 litros. Dado que 1 mol de C₂H₂ produce 2 moles de CO₂, se desprenden 2 moles * 22.4 L/mol = 44.8 L de CO₂ por cada mol de acetileno.
- Producción de CO₂ por Kilocaloría: Para encontrar los litros de CO₂ por kilocaloría, dividimos el volumen total de CO₂ producido por mol de acetileno entre la energía liberada por mol de acetileno:
Litros de CO₂ / kcal = 44.8 L / 312.0 kcal ≈ 0.1436 L/kcal
Por lo tanto, se desprenden aproximadamente 0.1436 litros de CO₂ a TPN por cada kilocaloría producida en la combustión del acetileno.