El calor específico es una propiedad fundamental de la materia que describe la cantidad de calor necesaria para elevar la temperatura de una unidad de masa de una sustancia en un grado. Este valor varía significativamente según el estado físico de la materia (sólido, líquido o gaseoso), ya que la estructura molecular de cada estado influye en la transmisión del calor. Por ejemplo, el calor específico del agua es de 1 cal/g°C, lo que significa que se requiere una caloría para aumentar la temperatura de un gramo de agua en un grado Celsius.
En la medición del calor específico, se emplean diversas unidades. Comúnmente se utiliza la caloría por gramo y por grado Celsius (cal/g°C). En el sistema anglosajón, se recurre a las Unidades Térmicas Británicas (BTU) por libra y por grado Fahrenheit.
Matemáticamente, el calor específico (c) se define como el límite de la relación entre el cambio de calor (ΔQ) y el producto de la masa (m) y el cambio de temperatura (ΔT), cuando el cambio de temperatura tiende a cero:
c = lim (Δt→0) . ΔQ / m.ΔT = 1/m . dQ/dT
Una sustancia con un mayor calor específico experimentará una menor variación de temperatura ante un suministro de calor determinado. El agua es un excelente ejemplo de esta propiedad.
Factores que influyen en la variación de temperatura
La variación de temperatura de un objeto al recibir o ceder energía térmica depende de varios factores:
- El material del objeto: Diferentes materiales poseen distintas capacidades para almacenar calor.
- La cantidad de calor suministrada: A mayor suministro de calor, mayor será la elevación de temperatura, asumiendo que los demás factores son constantes.
- La cantidad de materia (masa): Un objeto con mayor masa requerirá más calor para experimentar la misma elevación de temperatura que uno con menor masa.
La característica intrínseca de un material que determina su resistencia a cambiar de temperatura cuando se le suministra o retira calor se denomina calor específico.
Definición y unidades del Calor Específico
El calor específico (ce) se define formalmente como la cantidad de calor que necesita un gramo de una sustancia para elevar su temperatura en un grado centígrado. La unidad de medida más utilizada para el calor específico es cal/g°C.
Es importante distinguir entre calor y temperatura:
- Calor: Es la energía térmica en tránsito entre dos cuerpos con diferentes temperaturas.
- Temperatura: Es el estado termodinámico de un cuerpo, asociado al nivel medio de agitación de sus partículas.
Cuando un cuerpo recibe o cede energía térmica, puede ocurrir una variación de temperatura (calor sensible) o un cambio en su estado físico (calor latente). El calor sensible está relacionado con la agitación de las partículas, mientras que el calor latente es responsable de los cambios de agregación.
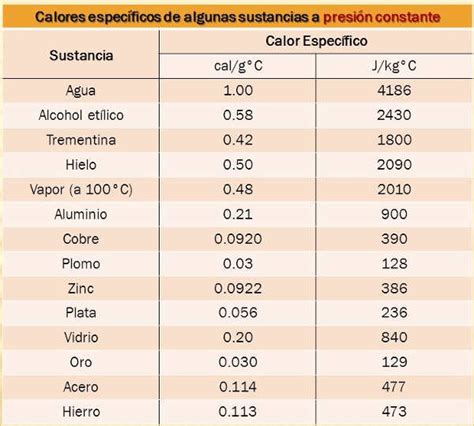
Tabla de Calores Específicos de Algunas Sustancias
La tabla de calores específicos ilustra cómo la variación de temperatura de un cuerpo, al intercambiar energía térmica, depende tanto de su material (calor específico) como de su masa. Se observa que sustancias como el agua poseen un calor específico elevado, lo que las hace más difíciles de calentar.
| Sustancia | Calor Específico (cal/g°C) |
|---|---|
| Aluminio | 0.217 |
| Cobre | 0.093 |
| Oro | 0.031 |
| Hierro | 0.113 |
| Silicio | 0.177 |
| Potasio | 0.169 |
| Vidrio | 0.199 |
| Mármol | 0.210 |
| Madera | 0.420 |
| Alcohol etílico | 0.581 |
| Mercurio | 0.033 |
| Aceite de oliva | 0.470 |
| Agua | 1.000 |
Fórmulas del Calor Específico y Capacidad Calorífica
La relación matemática para el calor específico es:
c = ΔQ / (m * ΔT)
Donde:
- ΔQ es el incremento de calor (en calorías).
- m es la masa (en gramos).
- ΔT es el incremento de temperatura (en °C).
Esta fórmula deriva de la capacidad calorífica (C), que se expresa como:
C = ΔQ / ΔT
Donde C es la capacidad calorífica (en cal/°C).
Ejercicios Resueltos de Calor Específico
Problema 1: Cálculo de temperatura final del hierro
Enunciado: 600 gramos de hierro se encuentran a una temperatura de 19°C. ¿Cuál será su temperatura final si se le suministran 1300 calorías?
Solución:
Datos:
- Calor específico del hierro ($C {{e}_{Fe}}$) = 0.113 cal/g°C
- Masa (m) = 600 g
- Temperatura inicial ($T_0$) = 19°C
- Calor suministrado (ΔQ) = 1300 cal
La fórmula del calor específico es: $c = \frac{\Delta Q}{m\Delta T}$. Despejando $\Delta T$: $\Delta T = \frac{\Delta Q}{m \cdot C_e}$.
La variación de temperatura se puede expresar como: $T_f - T_0 = \Delta T$. Por lo tanto, la temperatura final ($T_f$) es: $T_f = \frac{\Delta Q}{m \cdot C_e} + T_0$.
Sustituyendo los valores:
$\displaystyle {{T}_{f}}=\frac{1300cal}{\left( 600g \right)\left( 0.113\frac{cal}{g{}^\circ C} \right)}+19{}^\circ C = \frac{1300cal}{67.8\frac{cal}{{}^\circ C}}+19{}^\circ C = 19.17{}^\circ C+19{}^\circ C = 38.17{}^\circ C$
Resultado: La temperatura final del hierro será de 38.17°C.
Problema 2: Cantidad de calor para calentar una barra de plata
Enunciado: ¿Qué cantidad de calor se debe aplicar a una barra de plata de 24 kg para que eleve su temperatura de 31°C a 110°C?
Solución:
Datos:
- Masa (m) = 24 kg = 24000 g
- Temperatura inicial ($T_0$) = 31°C
- Temperatura final ($T_f$) = 110°C
- Calor específico de la plata ($C {{e}_{Ag}}$) = 0.056 cal/g°C
A partir de la fórmula del calor específico, despejamos $\Delta Q$: $\Delta Q = m \cdot C_e \cdot \Delta T$. La variación de temperatura es $\Delta T = T_f - T_0$.
Sustituyendo los valores:
$\displaystyle \Delta Q=\left( 24000g \right)\left( 0.056\frac{cal}{g{}^\circ C} \right)\left( {{110}^{{}^\circ }}C-{{31}^{{}^\circ }}C \right) = \left( 24000g \right)\left( 0.056\frac{cal}{g{}^\circ C} \right)\left( 79{}^\circ C \right) = 106176cal$
Resultado: Se deben aplicar 106176 calorías.
Problema 3: Calor cedido por una barra de plata
Enunciado: Determinar la cantidad de calor que cede al ambiente una barra de plata de 5200 gramos al enfriarse de 130°C a 10°C.
Solución:
Datos:
- Masa (m) = 5200 g
- Temperatura inicial ($T_0$) = 130°C
- Temperatura final ($T_f$) = 10°C
- Calor específico de la plata ($C {{e}_{Ag}}$) = 0.056 cal/g°C
Utilizamos la misma fórmula despejada para $\Delta Q$: $\Delta Q = m \cdot C_e \cdot (T_f - T_0)$.
Sustituyendo los valores:
$\displaystyle \Delta Q=\left( 5200g \right)\left( 0.056\frac{cal}{g{}^\circ C} \right)\left( 10{}^\circ C-130{}^\circ C \right) = \left( 5200g \right)\left( 0.056\frac{cal}{g{}^\circ C} \right)\left( -120{}^\circ C \right) = -34944cal$
Resultado: La barra de plata cede 34944 calorías al ambiente. El signo negativo indica la cesión de calor.
Ejercicios para Practicar
Problema 4: ¿Qué cantidad de calor se necesita suministrar a 600 gramos de agua para que eleve su temperatura de 25°C a 100°C?
Solución: 46750 cal
Problema 5: ¿Cuántas calorías se deben suministrar para que un pedazo de metal de hierro de 3.5 kg eleve su temperatura de 26°C a 140°C?
Solución: 48682 cal
Problema 6: Determine el calor específico de una pieza de 720.325 gramos que requiere 2300 calorias para elevar su temperatura de 37°C a 140°C. Consulte el cuadro de calores específicos para identificar que tipo de sustancia se trata.
Solución: 0.021 cal/g°C (aproximadamente Magnesio, aunque los valores pueden variar ligeramente)
Calorimetría y Resistencia Eléctrica
En el ámbito de la calorimetría, la determinación del calor específico de un sólido puede realizarse mediante el uso de resistencia eléctrica. Este método implica suministrar una cantidad de energía eléctrica conocida a una muestra del sólido y medir el aumento de temperatura resultante. La energía eléctrica suministrada (Q) se calcula a partir de la potencia de la resistencia (P) y el tiempo (t) durante el cual se aplica: Q = P * t. Conocida la masa del sólido (m) y la variación de temperatura (ΔT), se puede calcular el calor específico utilizando la fórmula:
c = Q / (m * ΔT)
Este enfoque permite mediciones precisas del calor específico, especialmente útil para materiales que son difíciles de manipular o para los cuales otros métodos calorimétricos no son prácticos.