Introducción a la Transferencia de Energía y Calor
En termodinámica química, el análisis de procesos de cambio de estado es fundamental. Un ejemplo clásico es el cálculo del trabajo de expansión y la variación de energía interna cuando una sustancia cambia de estado, como la vaporización del agua. Para comprender estos procesos, es esencial determinar volúmenes en estados inicial y final y considerar la energía absorbida.
La energía es un concepto central en física, y el calor es una forma de transferencia de energía que ocurre debido a una diferencia de temperatura. Esta transferencia de calor puede alterar la temperatura de un objeto y es crucial tanto en actividades cotidianas como en procesos industriales.
La energía interna de un sistema, que es la suma de las energías mecánicas de sus moléculas, puede modificarse mediante la transferencia de calor o la realización de trabajo sobre el sistema. La energía interna es proporcional a la temperatura. Cuando dos objetos a diferentes temperaturas entran en contacto, la energía se transfiere del más caliente al más frío hasta alcanzar el equilibrio térmico.
Es importante distinguir el uso científico del término "calor" de su uso coloquial. En física, el calor es un flujo de energía, mientras que la temperatura es una medida de la energía cinética promedio de las moléculas. La unidad del SI para el calor es el julio (J), aunque también se utiliza comúnmente la caloría (cal) y la kilocaloría (kcal).
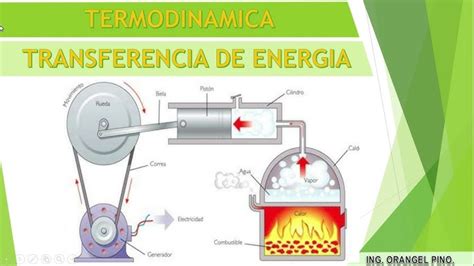
Equivalente Mecánico del Calor y Calor Específico
Los experimentos de James Prescott Joule demostraron que el trabajo y el calor pueden producir efectos similares y establecieron el equivalente mecánico del calor. El trabajo realizado para mover masas descendentes en agua, por ejemplo, resultó en un aumento de la temperatura del agua, similar al efecto de la transferencia de calor.
Conceptos como la variable de estado son cruciales. La temperatura y la energía interna son variables de estado porque su valor depende únicamente del estado actual del sistema, no de su historia. Sin embargo, un aumento en la energía interna no siempre resulta en un aumento de temperatura; esto ocurre, por ejemplo, durante un cambio de fase.
Cuando no hay cambio de fase ni trabajo realizado, el calor transferido ($Q$) es directamente proporcional a la masa ($m$) del sistema y al cambio de temperatura ($\Delta T$). La relación se expresa como:
$Q = mc\Delta T$
Donde $c$ es el calor específico (o capacidad calorífica específica), una propiedad que depende del material y su fase. El calor específico es la cantidad de calor necesaria para elevar la temperatura de 1 kg de una sustancia en 1°C. Las unidades comunes son J/(kg·K) o J/(kg·°C).
Los valores del calor específico varían significativamente entre sustancias. Por ejemplo, el agua tiene un calor específico considerablemente mayor que el vidrio o el hierro, lo que significa que se necesita más calor para elevar su temperatura.
Los calores específicos de los gases dependen de si el calentamiento se realiza a volumen constante o a presión constante. En general, el calor específico también puede depender de la temperatura, especialmente en gases, aunque para la mayoría de las sustancias a temperaturas normales, esta dependencia es débil.
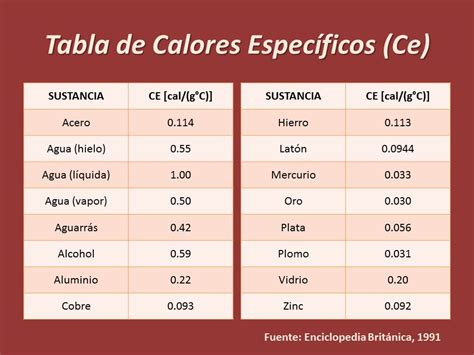
Ejemplo de Cálculo de Calor Específico
Consideremos una olla de aluminio calentada junto con agua. Para calcular el calor total necesario, debemos sumar el calor transferido al agua y al aluminio, teniendo en cuenta sus masas y calores específicos.
- Calcular la masa del agua.
- Calcular el calor transferido al agua usando $Q_{agua} = m_{agua} c_{agua} \Delta T$.
- Calcular el calor transferido al aluminio usando $Q_{aluminio} = m_{aluminio} c_{aluminio} \Delta T$.
- El calor total es $Q_{total} = Q_{agua} + Q_{aluminio}$.
Este ejemplo resalta la importancia de considerar el calor absorbido por los recipientes en los cálculos de transferencia de calor.
Problemas de Calorimetría y Cambios de Fase
Los problemas de calorimetría involucran sistemas aislados térmicamente donde los objetos intercambian calor hasta alcanzar el equilibrio. Un ejemplo es mezclar agua fría con una olla caliente.
En estos escenarios, la suma de las transferencias de calor es cero: $\sum Q = 0$. La temperatura final de la mezcla se acerca más al valor de la sustancia con mayor capacidad calorífica y/o mayor masa, como el agua en comparación con el aluminio.
La gran capacidad calorífica del agua explica por qué los cuerpos de agua como lagos mantienen temperaturas relativamente estables, mitigando los cambios drásticos de temperatura ambiental.
Calor Latente y Calor de Vaporización
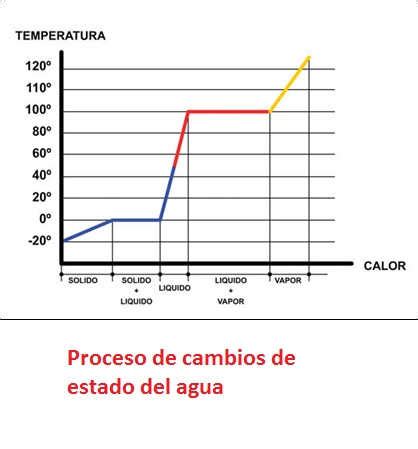
Cuando una sustancia cambia de estado (fase), la energía requerida se denomina calor latente. Durante un cambio de fase, la temperatura de la sustancia permanece constante a pesar de la adición o eliminación de calor.
El calor de vaporización (o calor de evaporación) es la energía necesaria para convertir una sustancia de estado líquido a gaseoso sin cambiar su temperatura. Para el agua a 100°C y 1 atm, este valor es de aproximadamente 2260 J/kg.
La fórmula para el calor transferido durante un cambio de fase es:
$Q = mL$
Donde $m$ es la masa y $L$ es el calor latente de la sustancia. Para el agua, el calor latente de fusión (hielo a líquido) es de 334 J/kg, y el calor latente de vaporización es de 2260 J/kg.
A diferencia del calor latente, el calor sensible es la energía que causa un cambio de temperatura sin alterar la estructura molecular o el estado de agregación de la sustancia.
Procesos de Vaporización y Purificación del Glicerol
El glicerol (1,2,3-propanotriol) es un producto químico versátil obtenido tanto por síntesis química como como subproducto de la metanólisis de aceites vegetales. Con el aumento de los biocombustibles, la producción de glicerol a partir de fuentes renovables ha crecido significativamente.
El glicerol crudo, a menudo obtenido de aceites vegetales, contiene impurezas como agua, sales y compuestos orgánicos no glicerinados. Estas impurezas pueden ser perjudiciales para aplicaciones posteriores, como la producción de acroleína, donde las sales de sodio o potasio pueden envenenar los catalizadores.
Por ello, las soluciones acuosas de glicerol brutas a menudo requieren tratamientos de purificación y concentración, incluyendo la vaporización.
Tecnologías de Purificación y Evaporación del Glicerol
Se han desarrollado diversas tecnologías para la purificación y evaporación del glicerol, adaptadas a sus más de 1.500 aplicaciones, que exigen diferentes grados de pureza.
- Evaporadores de múltiples efectos: Se utilizan para concentrar soluciones diluidas de glicerol, permitiendo evaporar grandes cantidades de agua con vapor.
- Destilación: Dado que el glicerol se descompone a temperaturas relativamente bajas (alrededor de 202°C), la destilación se realiza bajo presión reducida y en múltiples etapas para evitar la degradación. Se emplean presiones de aproximadamente 10 mm de Hg a temperaturas de 160-165°C para lograr bajas presiones parciales de glicerol en fase de vapor.
- Decoloración: La glicerina destilada puede contener compuestos coloreados, requiriendo tratamientos con carbón activado para aplicaciones farmacéuticas y alimentarias.
- Exclusión iónica y resinas de intercambio iónico: Estas técnicas separan sales iónicas solubles y otros compuestos no iónicos del glicerol. Las soluciones débilmente contaminadas pueden tratarse con resinas ácidas y básicas.
- Ósmosis inversa: Utiliza membranas semipermeables y presión para concentrar flujos de glicerol diluidos.
- Electrodiálisis: Técnica de membrana para desmineralizar soluciones de glicerol, utilizada para producir glicerina pura.
¿Cómo funciona el sistema de purificación de agua por osmosis inversa?
Procedimientos de Vaporización en Lecho Fluidizado
Los procedimientos de evaporación tradicionales a menudo no permiten altas presiones parciales de glicerol en fase de vapor, lo que limita la productividad. Además, el glicerol puede descomponerse a altas temperaturas, formando acroleína o polímeros, y las altas temperaturas prolongadas deben evitarse.
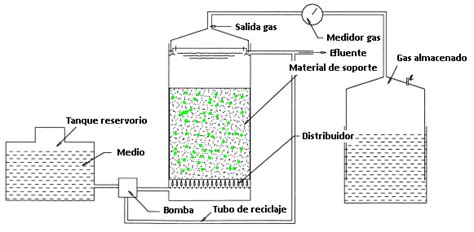
Se ha desarrollado un procedimiento innovador que utiliza un lecho fluidizado con un sólido inerte para vaporizar soluciones acuosas de glicerol y eliminar simultáneamente las impurezas.
En este proceso:
- La solución acuosa de glicerol se inyecta directamente en un lecho fluidizado de un sólido inerte (como arena, sílice o carburo de silicio) mantenido a una temperatura suficiente (generalmente entre 220 y 350°C, preferiblemente 260-320°C) para la vaporización instantánea.
- La fluidización se mantiene mediante la vaporización de la solución o una corriente de gas inerte (nitrógeno, CO2, aire).
- Este método permite altas presiones parciales de glicerol en fase de vapor, aumentando la productividad.
- Las impurezas, como sales y productos de descomposición (coque), se depositan sobre el sólido inerte.
- El sólido inerte, contaminado con impurezas, se puede retirar continuamente para su regeneración (por ejemplo, mediante combustión en otro reactor) y posterior reintroducción en el lecho fluidizado.
- El desgaste natural de las partículas en el lecho fluidizado también contribuye a la eliminación de depósitos.
Ejemplo de Proceso de Vaporización en Lecho Fluidizado
Un experimento realizado con una solución acuosa de glicerol al 18% en peso y 2% en peso de NaCl demostró una eficacia del 99.9% en la separación de sal. La solución de glicerol y NaCl se introdujo en un lecho fluidizado de sílice a 310°C con un flujo de aire y nitrógeno.
Los productos se recolectaron y condensaron. El análisis de conductividad de la solución condensada mostró un contenido de sal extremadamente bajo, confirmando la alta eficiencia del lecho fluidizado para eliminar impurezas inorgánicas.
Los vapores de glicerol obtenidos por este procedimiento son directamente utilizables en procesos posteriores que requieren glicerol en fase gaseosa, como la producción de acroleína o ácido acrílico.