El metabolismo lipídico juega un papel fundamental en la vida, siendo los lípidos esenciales para la estructura celular y el suministro de energía. El colesterol y los fosfolípidos son componentes clave de las membranas celulares, garantizando su funcionalidad y supervivencia. Además, el colesterol es la base para la síntesis de hormonas esteroides. Por otro lado, los triglicéridos almacenan ácidos grasos, que sirven como fuente de energía para el organismo y constituyen el tejido adiposo, una reserva energética crucial para períodos de ayuno y la supervivencia de la especie.
Existe una aparente paradoja con el colesterol: si bien es vital para todas las células, incluyendo el cerebro, y las células pueden sintetizarlo si no lo obtienen del exterior (vía de las lipoproteínas de baja densidad, LDL), su exceso, derivado de alteraciones en el metabolismo lipídico, puede desencadenar aterosclerosis, la principal causa de muerte a nivel mundial, especialmente en países desarrollados.
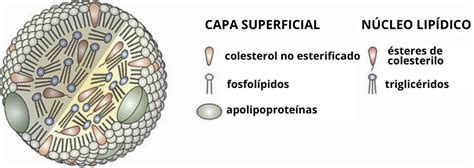
Dado su vínculo con la patología, este artículo se centrará en el metabolismo del colesterol y los triglicéridos. Al ser ambos lípidos insolubles en agua (sangre), su transporte requiere la unión a proteínas específicas, las apolipoproteínas (apo), formando las lipoproteínas. Estas estructuras poseen un núcleo compuesto por colesterol esterificado y triglicéridos, y una capa externa de colesterol libre, fosfolípidos y apolipoproteínas, que les confiere miscibilidad en medios acuosos.
Principales Lipoproteínas
Las lipoproteínas son diversas y cumplen funciones específicas en el transporte de lípidos. Las principales incluyen:
- Quilomicrones (QM)
- Remanentes de QM (QMR)
- Lipoproteínas de muy baja densidad (VLDL)
- Remanentes de VLDL (VLDLR)
- Lipoproteínas de densidad intermedia (IDL)
- Lipoproteínas de baja densidad (LDL)
- Lipoproteína (a) [Lp(a)]
- Lipoproteínas de alta densidad (HDL)
La tabla 1 resume las características y composición de estas lipoproteínas.
| Lipoproteína | Composición Principal | Función |
|---|---|---|
| Quilomicrones (QM) | Triglicéridos (TG), Colesterol, ApoB48 | Transporte de TG de la dieta desde el intestino al cuerpo. |
| VLDL | TG, Colesterol, ApoB100 | Transporte de TG sintetizados en el hígado al cuerpo. |
| LDL | Colesterol, ApoB100 | Transporte de colesterol a las células periféricas. |
| HDL | Proteínas, Fosfolípidos, Colesterol libre y esterificado | Transporte inverso de colesterol desde los tejidos al hígado. |
Metabolismo Exógeno de las Lipoproteínas
La vía exógena se encarga del transporte de lípidos desde el intestino, principalmente de la dieta y de la bilis, hacia el hígado y las células periféricas, especialmente el tejido adiposo.
Los triglicéridos de la dieta son hidrolizados en el intestino por las lipasas pancreáticas y emulsionados con ácidos biliares para formar micelas. Estas micelas son captadas por las células intestinales a través del transportador FAT/CD36. El colesterol es absorbido mediante la proteína Niemann-Pick C1-like 1 (NPC1L1). Dentro de los enterocitos, el colesterol se esterifica (formando colesterol esterificado) por la enzima acyl-CoA:cholesterol acyltransferase (ACAT). Junto con los triglicéridos sintetizados, se unen a la apoB48 gracias a la proteína de transferencia microsómica (MTP), formando los quilomicrones (QM). Posteriormente, proteínas como SAR1a y SAR1b son esenciales para el transporte de los QM al aparato de Golgi.
Los QM formados son secretados a la linfa intestinal y luego a la circulación general. Allí sufren modificaciones, principalmente por la acción de la lipoproteína-lipasa (LPL), una enzima localizada en el endotelio vascular de diversos tejidos. La LPL hidroliza los TG de los QM, liberando ácidos grasos libres que son captados por el tejido adiposo y muscular para obtener energía o ser almacenados como TG. Esta hidrólisis requiere la activación de la LPL y su regulación es compleja, involucrando múltiples enzimas, proteínas, apolipoproteínas y hormonas.
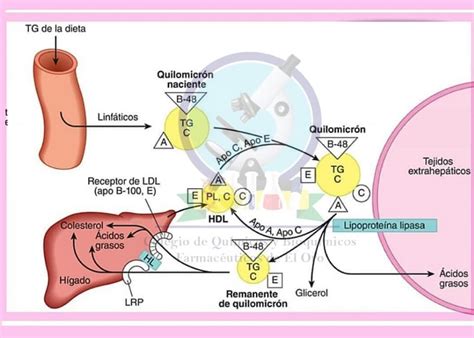
Los QM, al ser hidrolizados por la LPL, disminuyen su contenido de TG y modifican su composición mediante la transferencia de colesterol y fosfolípidos a las HDL, y el intercambio de apolipoproteínas, enriqueciéndose en apoE. Las partículas resultantes, más pequeñas y ricas en ésteres de colesterol, se denominan quilomicrones remanentes (QMR). Estos QMR son rápidamente retirados de la circulación por el hígado, uniéndose a receptores específicos donde interviene la apoE. Diversos receptores hepáticos, como los proteoglicanos, receptores de VLDL, LDL (R-LDL) y LRP1, participan en esta captación. En condiciones normales, los QMR desaparecen del torrente circulatorio en pocas horas.
Bioquímica en 2 minutos: LDL y HDL
Metabolismo Endógeno de las Lipoproteínas
El hígado es el centro del metabolismo lipoproteico. La vía endógena comienza con la síntesis y secreción de las VLDL por el hígado, que luego se transforman en plasma en VLDLR, IDL y LDL.
Las VLDL, al igual que los QM, son ricas en TG y contienen apoB100. Los TG de las VLDL provienen principalmente de la esterificación hepática de ácidos grasos. El empaquetamiento de los componentes de las VLDL (TG, ésteres de colesterol, colesterol libre, fosfolípidos y apoB100) requiere la acción de la proteína de transporte microsómico (MTP), de forma similar a la formación de QM. Las VLDL adquieren apoE y otras apolipoproteínas del grupo C.
Tras su secreción, las VLDL son hidrolizadas por la LPL en el endotelio vascular, liberando TG que llegan a los tejidos periféricos. Con la pérdida de TG, las VLDL intercambian componentes con las HDL, volviéndose más ricas en colesterol y apoE, transformándose en VLDL remanentes (VLDLR) e IDL. Entre el 40% y el 60% de estas partículas son captadas por el hígado a través de receptores de LDL (R-LDL), mediante la unión a apoE y otros receptores. El resto de las IDL son remodeladas por la acción de la LPL y la lipasa hepática (HL) para formar LDL. Durante este proceso, la mayoría de los TG se hidrolizan y todas las apolipoproteínas, excepto la apoB100, se transfieren a otras lipoproteínas, resultando en partículas LDL muy ricas en colesterol y con apoB100 como única apolipoproteína.
El colesterol de las LDL constituye la mayor parte del colesterol plasmático. Aproximadamente el 70% de las LDL son captadas por el hígado a través del R-LDL, donde la apoB juega un papel crucial. El 30% restante es captado por las células periféricas a través de R-LDL similares a los hepáticos. El R-LDL es un receptor saturable; cuando se satura por exceso de LDL en plasma, su capacidad de captación disminuye. La regulación de este proceso involucra la reducción en la producción de R-LDL cuando el contenido celular de colesterol aumenta, controlada por factores de transcripción como SREBP-1c y SREBP-2.
El receptor LDL (hepático y periférico) fue identificado por Goldstein y Brown, quienes describieron el mecanismo de endocitosis mediada por clatrina. Tras la endocitosis, los endosomas disocian las LDL y los R-LDL, permitiendo el reciclaje del receptor o su degradación lisosomal. La proteína PCSK9 interviene en este proceso. Las LDL son degradadas en los lisosomas por la acción de la lipasa ácida lisosomal (LAL).
El exceso de LDL no captada, junto con otras partículas lipídicas como VLDLR e IDL de pequeño tamaño, pueden atravesar la pared endotelial, ser retenidas por los proteoglicanos subendoteliales y captadas por los macrófagos (receptor scavenger), iniciando el proceso aterosclerótico.
La lipoproteína (a) [Lp(a)] es similar a la LDL pero contiene una apolipoproteína adicional, la apo(a). La Lp(a) puede atravesar la barrera endotelial y contribuir a la arteriosclerosis, aunque su mecanismo de retirada de la circulación no está completamente aclarado.
Transporte Inverso del Colesterol
El colesterol depositado en las células o en la pared arterial no puede ser catabolizado por el organismo. La única vía de eliminación es a través de las HDL, mediante el transporte inverso del colesterol. Las HDL extraen y vehiculizan el colesterol tisular hacia el hígado.
Las partículas de HDL nacientes, sintetizadas en intestino, hígado y plasma, tienen una estructura discoidal y contienen apoAI y fosfolípidos. Captan colesterol no esterificado y fosfolípidos de las células periféricas a través de proteínas de membrana como ABCA1, ABCG1 y el receptor SR-BI. Este eflujo de colesterol es vital para la homeostasis del colesterol y la prevención de la aterosclerosis.
Tras incorporar colesterol, las HDL se vuelven esféricas. El colesterol es esterificado por la lecitin-colesterol aciltransferasa (LCAT), y las HDL se enriquecen en lípidos y apolipoproteínas (A, C, E) por intercambio con VLDL y QM. Estas HDL son captadas por los hepatocitos de forma directa (a través de SR-BI) o indirecta. También pueden ser captadas por otros receptores como CD36.
El colesterol hepático proveniente de las HDL es reutilizado para la síntesis de nuevas VLDL o excretado por vía biliar como ácidos biliares o colesterol, a través de los cotransportadores ABCG5/G8.
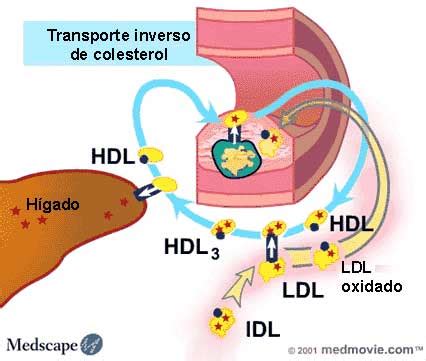
Durante mucho tiempo, las HDL se consideraron el "colesterol bueno" por su rol protector cardiovascular. Sin embargo, las HDL son partículas complejas con funciones dinámicas que pueden ser alteradas, llegando a ser potencialmente perjudiciales. Además de la extracción de colesterol, las HDL poseen acciones antiinflamatorias, antioxidantes, antiapoptóticas, y contribuyen al mantenimiento del endotelio.
El Hipercorisolismo y su Relación con el Metabolismo Lipídico
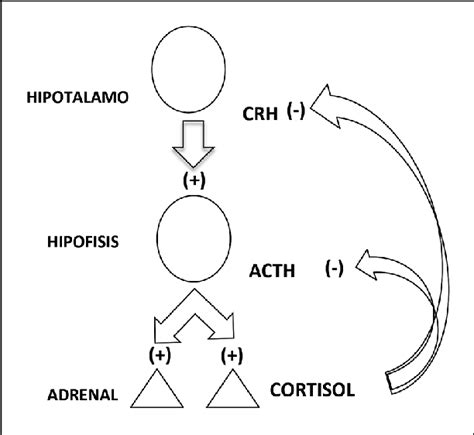
El cortisol, a menudo llamado la "hormona del estrés", se produce en las glándulas suprarrenales y desempeña un papel crucial en el metabolismo, la regulación de la presión arterial, la respuesta inflamatoria y la adaptación al estrés. Su secreción está controlada por el eje hipotálamo-hipófisis-adrenal (HHA).
El estrés crónico puede llevar a una alteración en la actividad del eje HHA, resultando en niveles elevados de cortisol (hipercorisolismo). Esta condición tiene implicaciones significativas en el metabolismo lipídico y la ingesta de alimentos.
El hipercorisolismo se asocia con un fenotipo caracterizado por obesidad centrípeta (acumulación de grasa en el tronco), resistencia a la insulina, hipertensión arterial y dislipidemia, características que comparten similitudes con el síndrome metabólico (SM).
Se ha planteado que el tejido adiposo, especialmente el visceral, puede actuar como un órgano endocrino que modula la regulación del cortisol a nivel local. La enzima 11β-hidroxiesteroide deshidrogenasa tipo 1 (11β-HSD1) convierte la cortisona inactiva en cortisol, incrementando la actividad de glucocorticoides en tejidos como el hígado y el tejido adiposo. En la obesidad, se observa una sobreexpresión de 11β-HSD1 en el tejido graso, lo que puede perpetuar la acumulación de grasa y contribuir a la resistencia a la insulina y otros trastornos metabólicos.
La relación entre el estrés crónico, el cortisol elevado y el aumento de la ingesta de alimentos, particularmente de alta densidad energética, es un factor que puede favorecer la conducta alimentaria compulsiva, la disrupción del balance energético y la obesidad. El consumo de alimentos apetitosos puede ser una forma de "automedicación" para aliviar el estrés, proporcionando confort.
Los datos epidemiológicos respaldan un fuerte vínculo entre los glucocorticoides y el síndrome metabólico. La adiposidad visceral y la resistencia a la insulina son factores predisponentes a la disrupción metabólica que puede surgir de la interacción entre estrés crónico, cortisol y una ingesta elevada de alimentos.
El síndrome de Cushing, causado por una exposición prolongada a niveles excesivos de cortisol, ejemplifica las consecuencias del hipercorisolismo. Las manifestaciones clínicas incluyen obesidad central, cara de luna llena, estrías violáceas, hipertensión arterial y debilidad muscular. Las pruebas bioquímicas, como la medición del cortisol libre en orina de 24 horas y la determinación de ACTH, son fundamentales para el diagnóstico y la identificación de la causa subyacente (adenoma hipofisario, tumores suprarrenales, etc.). El tratamiento varía según la causa e incluye cirugía, radioterapia o terapia farmacológica.
En niños con obesidad, se ha observado una relación entre los niveles de cortisol sérico y un mayor número de componentes del síndrome metabólico. También se ha encontrado una asociación entre el cortisol y la ingesta excesiva de alimentos de origen animal, azúcares y grasas, aunque la relación con la ansiedad no ha sido concluyente en todos los estudios.
Bioquímica en 2 minutos: LDL y HDL
tags: #hipercortisolismo #metabolismo #lipidos