La entalpía, representada por H, es una medida de la energía potencial contenida en un enlace químico o en una interacción química que se libera en forma de calor. La energía potencial es la energía que posee una molécula debido a la disposición espacial de sus átomos en un momento dado. Por otro lado, un enlace químico es la fuerza de atracción que mantiene unidos a los átomos dentro de una molécula, asegurando la orientación y valencia adecuadas.
La valencia de enlace se refiere al número de pares de electrones presentes en un enlace químico.
Definición de Entalpía Estándar de Formación
La entalpía estándar de formación, denotada como ΔHf°, se define como el cambio de entalpía que ocurre durante la formación de un mol de una sustancia en su estado estándar, a partir de sus elementos constituyentes en su forma de referencia y en sus respectivos estados estándar.
El estado estándar se refiere a las condiciones termodinámicas estándar bajo las cuales se registran los datos termodinámicos. Típicamente, estas condiciones son una presión de 1 atmósfera (atm) y una temperatura de 25 °C.
La forma de referencia de un elemento es su forma más estable en condiciones estándar. Los coeficientes estequiométricos son los números que preceden a las especies químicas en una ecuación química balanceada.
Entalpía Estándar de Reacción
La entalpía estándar de formación (ΔHf°) se integra dentro del concepto más amplio de la entalpía global de una reacción química, también conocida como entalpía estándar de reacción (ΔH°). Esta se calcula mediante la siguiente ecuación:
$$ \Delta{H^\circ}=\Sigma_{i=1}^n\,[q\Delta{H_f^\circ}(Productos)]_i-\Sigma_{i=1}^n\,[r\Delta{H_f^\circ}(Reactants)]_i $$
Donde:
- Σ representa el símbolo de sumatoria.
- q y r son los coeficientes estequiométricos de los productos y reactantes, respectivamente, en la ecuación química balanceada.
- ΔHf°(Productos) es la entalpía estándar de formación de los productos.
- ΔHf°(Reactivos) es la entalpía estándar de formación de los reactantes.
El símbolo de sumatoria (Σ) indica que se deben sumar los términos correspondientes. Por ejemplo, \(\Sigma_{i=1}^4 a_i = a_1 + a_2 + a_3 + a_4\), lo que significa que se suman los términos desde el índice 1 hasta el índice 4.
Tablas de Entalpía Estándar de Formación
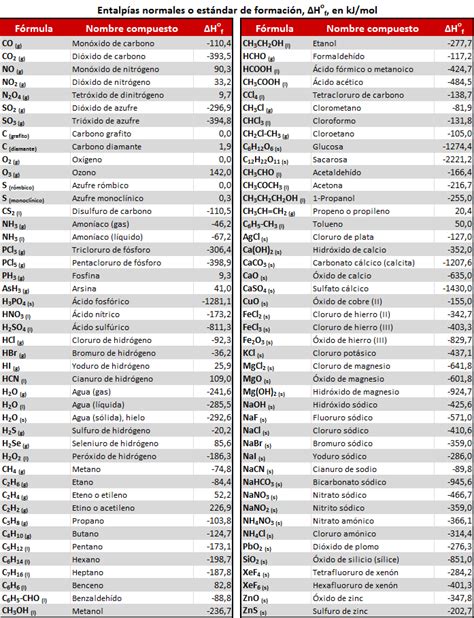
Para determinar la entalpía estándar de formación de una sustancia, es necesario consultar tablas de datos termodinámicos. A continuación, se presenta una tabla con las entalpías estándar de formación de compuestos comunes:
Tabla 1: Entalpías Estándar de Formación (a 25°C)
| Fórmula | ΔHf° (kJ mol⁻¹) | Fórmula | ΔHf° (kJ mol⁻¹) |
|---|---|---|---|
| e⁻, Electrón Gas (g) | 0 | C (g), grafito (forma elemental) | 0 |
| H⁺ (aq) | 0 | CO (g) | -110.5 |
| H (g), Hidrógeno atómico gaseoso | 218.0 | CO₂ (g) | -393.5 |
| H₂ (g), Hidrógeno gaseoso (forma elemental) | 0 | CH₄ (g) | -74.9 |
| Na (g) | 107.8 | C₆H₆ (l) | 49.0 |
| Na (s) (forma elemental) | 0 | HCHO (g) | -116 |
| NaCl (s) | -411.1 | HCN (g) | 135 |
| NaHCO₃ (s) | -947.7 | HCN (l) | 105 |
| Na₂CO₃ (s) | -1130.8 | CH₃CHO(g) | -166 |
| Cl (g), Atómico Cloro gaseoso | 121.0 | CCl₄ (l) | -139 |
| Cl₂ (g), Cloro gas (forma elemental) | 0 | HCl (g) | -92.3 |
| Cristales de yodo, I₂ (s) (forma elemental) | 0 | Yoduro gaseoso, I⁻(g) | -197.7 |
| O₂ (g), Oxígeno gas (forma elemental) | 0 | O (g) | 249.2 |
| H₂O(g) | -241.8 | H₂O(l) | -285.8 |
Es importante notar que los compuestos que se encuentran en su estado elemental (forma de referencia) tienen una entalpía estándar de formación igual a cero.
Cálculo de la Entalpía Estándar de Reacción
La ecuación para calcular la entalpía estándar de reacción (ΔH°) es:
$$ \Delta{H^\circ}=\Sigma_{i=1}^n\,[q\Delta{H_f^\circ}(Products)]_i-\Sigma_{i=1}^n\,[r\Delta{H_f^\circ}(Reactants)]_i $$
Como ejemplo, consideremos la reacción entre el metano gaseoso (CH₄ (g)) y el cloro gaseoso (Cl₂ (g)) para producir tetracloruro de carbono líquido (CCl₄ (l)) y ácido clorhídrico gaseoso (HCl (g)):
$$ 1CH_4(g) + 4Cl_2(g) \rightarrow 1CCl_4(l) + 4HCl(g) $$
Aplicando la ecuación de la entalpía de formación:
\begin{align}\Delta{H^\circ} &= \Sigma_{i=1}^n\,[q\Delta{H_f^\circ}(Products)]_i - \Sigma_{i=1}^m\,[r\Delta{H_f^\circ}(Reactants)]_i \\&= [\Delta{H_f^\circ}(CCl_4) + \Delta{H_f^\circ}(HCl)] - [\Delta{H_f^\circ}(CH_4) + \Delta{H_f^\circ}(Cl_2)] \\&= [1 \cdot (-139 \text{ kJ/mol}) + 4 \cdot (-92.3 \text{ kJ/mol})] - [1 \cdot (-74.9 \text{ kJ/mol}) + 4 \cdot (0.0 \text{ kJ/mol})] \\&= -433 \text{ kJ/mol}\end{align}
Este cálculo demuestra que la entalpía de reacción para esta transformación es de -433 kJ/mol.
Cálculo de la Entalpía de Formación Específica
Para calcular la entalpía de formación de un compuesto específico, como el cloruro de hidrógeno (HCl (g)), a partir de sus elementos en condiciones estándar, se sigue un proceso similar, considerando la ruptura de enlaces existentes y la formación de nuevos enlaces.
Consideremos la formación de HCl (g) a partir de H₂ (g) y Cl₂ (g):
$$ H_2(g) + Cl_2(g) \rightarrow HCl(g) $$
Si bien la entalpía estándar de formación del H₂ (g) y Cl₂ (g) es cero, la reacción real implica la disociación de estas moléculas en átomos:
$$ H_2(g) + Cl_2(g) \rightarrow 2H(g) + 2Cl(g) \rightarrow 2HCl(g) $$
La entalpía estándar de formación de los reactantes (en este caso, los átomos formados) se calcula teniendo en cuenta los coeficientes estequiométricos:
\begin{align}\Delta{H_f^\circ}(Reactants) &= \Sigma_{i=1}^m\,[r\Delta{H_f^\circ}(Reactants)]_i \\&= 2 \cdot \Delta{H_f^\circ}(\text{Hidrógeno atómico gas}) + 2 \cdot \Delta{H_f^\circ}(\text{Cloro atómico gas}) \\&= 2 \cdot (218.0 \text{ kJ/mol}) + 2 \cdot (121.0 \text{ kJ/mol}) \\&= 678 \text{ kJ/mol}\end{align}
La entalpía estándar de formación para la producción de 2 moles de HCl (g) es:
$$ 2 \cdot \Delta{H_f^\circ}(\text{Cloruro de Hidrógeno gas}) = 678 \text{ kJ/mol} $$
Este proceso es endotérmico, lo que significa que absorbe energía.
Ley de Hess y Entalpía de Formación
La Ley de Hess, también conocida como la Ley de Hess de la Suma Constante del Calor, establece que el cambio total de entalpía en una reacción química es independiente de la ruta seguida, es decir, solo depende de los estados inicial y final.
Aplicando la Ley de Hess a la reacción entre metano y cloro:
$$ 1CH_4(g) + 4Cl_2(g) \rightarrow 1CCl_4(l) + 4HCl(g) $$
Se utilizan las siguientes ecuaciones termoquímicas:
\begin{align}C\,(\text{Grafito}) + 2\,H_2\,(g) &\rightarrow CH_4\,(g):\,\Delta{H_f^\circ} = -74.9\,kJ/mol \quad &(1) \\C\,(\text{Grafito}) + Cl_2\,(g) &\rightarrow CCl_4\,(l):\,\Delta{H_f^\circ} = -139\,kJ/mol \quad &(2) \\\frac{1}{2}H_2 + \frac{1}{2}Cl_2\,(g) &\rightarrow HCl\,(g):\,\Delta{H_f^\circ} = -92.3\,kJ/mol \quad &(3)\end{align}
Para obtener la reacción deseada, se invierte la ecuación (1), se suma la ecuación (2) y se multiplica la ecuación (3) por cuatro:
\begin{align}CH_4\,(g) &\rightarrow C\,(\text{Grafito}) + 2\,H_2\,(g) \quad &1 \cdot (+74.9\,kJ/mol) \\C\,(\text{Grafito}) + Cl_2\,(g) &\rightarrow CCl_4\,(l) \quad &+1 \cdot (-139\,kJ/mol) \\\underline{2H_2\,(g) + 2Cl_2\,(g)} &\rightarrow \underline{4HCl\,(g)} \quad &\underline{+4 \cdot (-92.3\,kJ/mol)} \\CH_4\,(g) + 4Cl_2\,(g) &\rightarrow CCl_4\,(l) + 4HCl\,(g) \quad &\Delta{H^\circ} = -433.3\,kJ/mol\end{align}
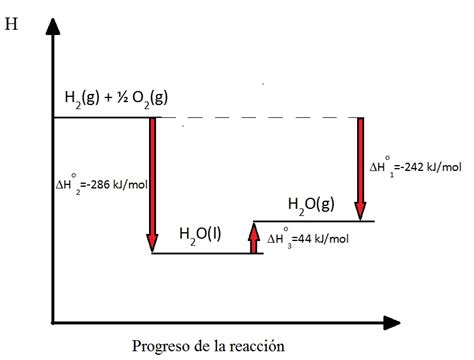
Entalpía de Formación del Agua
La entalpía estándar de formación del agua (H₂O (l)) a partir de hidrógeno gaseoso (H₂) y oxígeno gaseoso (O₂) se representa por la siguiente reacción:
$$ 2H_2(g) + O_2(g) \rightarrow 2H_2O(l):\,\Delta{H_f^\circ} = -571.6\,kJ/mol $$
Para obtener la entalpía de formación de 1 mol de agua líquida, la ecuación se multiplica por 1/2:
$$ \frac{1}{2} \cdot 2H_2(g) + \frac{1}{2} \cdot O_2(g) \rightarrow \frac{1}{2} \cdot 2H_2O(l):\,\Delta{H_f^\circ} = \frac{1}{2} \cdot (-571.6\,kJ/mol) = -285.8\,kJ/mol $$
Esta es la entalpía estándar de formación de 1 mol de agua líquida.
Puntos Clave sobre la Entalpía de Formación
- La entalpía es la energía potencial contenida en un enlace químico que se libera como calor.
- La entalpía global de una reacción química (ΔH°) se calcula a partir de las entalpías estándar de formación de productos y reactantes.
- La entalpía estándar de formación es el cambio de entalpía para formar un mol de una sustancia a partir de sus elementos en estado estándar.
- La Ley de Hess permite calcular cambios de entalpía sumando entalpías de reacciones conocidas.