Introducción
La detección de parámetros seminales con valor predictivo en el resultado de las técnicas de reproducción representa uno de los principales objetivos para los profesionales de un laboratorio de andrología. Si estos parámetros están alterados, es fundamental disponer de los recursos necesarios para poder dar solución o intentar disminuir el efecto negativo.
Entre los parámetros básicos de valoración del espermiograma, cabe destacar la importancia que ha adquirido la morfología espermática en el diagnóstico de la infertilidad masculina. A pesar de la controversia existente acerca de su función en la fecundación y el desarrollo embrionario, numerosos estudios han demostrado que la selección del mejor espermatozoide antes de una inyección intracitoplasmática de espermatozoides (ICSI) mejora el resultado del tratamiento.
La aparición de nuevas herramientas, como el microscopio de alta magnificación, ha permitido a los investigadores profundizar en el estudio de la morfología espermática y detectar defectos en el núcleo del espermatozoide, como la presencia de vacuolas nucleares que no pueden ser detectadas mediante una ICSI convencional a ×400. Se ha demostrado que estas vacuolas tienen un efecto directo en el desarrollo embrionario y el aborto temprano. Varios autores han demostrado una correlación negativa entre la presencia de grandes vacuolas en el núcleo del espermatozoide y la estabilidad de la cromatina espermática. Asimismo, se ha observado también que el aumento de la fragmentación del ácido desoxirribonucleico (ADN) espermático está asociado a la presencia de anomalías en la morfología espermática.
Los mecanismos exactos que dan lugar a estas alteraciones espermáticas son todavía objeto de estudio. Se han barajado diferentes teorías que implican la interrelación de diferentes mecanismos: empaquetamiento de la cromatina espermática, apoptosis, estrés oxidativo, anomalías genéticas y estrés crónico. Un ambiente testicular alterado (con presencia de leucocitos, células germinales inmaduras, etc.) puede causar disfunción en la espermatogénesis. Así pues, el daño en el ADN y el potencial de fertilidad espermático se han relacionado con la toxicidad provocada por el oxígeno y la acción de las especies reactivas de oxígeno (ROS). Una elevada producción de ROS que sobrepase los mecanismos de defensa de la célula puede dañar significativamente la función de la membrana espermática debido a la peroxidación lipídica, con lo que así se reduce la capacidad del espermatozoide para llevar a cabo la reacción acrosómica.
Debido a la escasa efectividad de los mecanismos endógenos de defensa en humanos, parece efectiva la administración de un tratamiento con antioxidantes para la mejora de la calidad espermática en pacientes que se someten a tratamiento de fertilización in vitro/ICSI. El objetivo de este estudio piloto fue investigar el efecto de la L-carnitina, la coenzima Q10 y las vitaminas C, E y B12 en la vacuolización en la cabeza del espermatozoide y la fragmentación del ADN espermático.
Material y Métodos
Para este estudio prospectivo se seleccionó a un total de 65 pacientes que acudieron a nuestro centro entre mayo y noviembre de 2009, de los cuales 33 finalizaron el estudio dentro de este período. La edad media ± desviación estándar fue de 37,2 ± 5,4 años. El presente estudio fue aprobado por el Comité Ético del centro y todos los pacientes firmaron el consentimiento informado.
Cada paciente entregó dos muestras de semen en un intervalo aproximado de 30 días. Las muestras se obtuvieron por masturbación después de mantener entre 3 y 5 días de abstinencia sexual. Las muestras se dejaron licuar a temperatura ambiente y tras 20 minutos se realizó un análisis de los parámetros seminales básicos siguiendo los criterios de la Organización Mundial de la Salud. Se consideraron las variables siguientes: volumen (ml), concentración espermática (n × 106/ml), movilidad espermática (porcentaje de espermatozoides a y b) y morfología espermática (porcentaje de formas normales).
Una vez entregada la primera muestra, los pacientes empezaron un tratamiento con Androferti® (Laboratorios Q Pharma SL, Alicante [España]), cuya composición por dosis es de 750 mg de L-carnitina fumarato, 250 mg de acetil-L-carnitina, 10 mg de coenzima Q10, 5 mg de cinc, 100 μg de ácido fólico, 25 μg de selenio, 0,50 μg de vitamina B12, 30 mg de vitamina C y 5 mg de vitamina E. La dosis administrada fue de un sobre cada 12 horas durante un mínimo de 30 días. Se decidió realizar el estudio con este intervalo de tiempo con la intención de valorar el efecto de este tratamiento en espermatozoides del mismo ciclo espermatogénico. Tras este período, cada paciente entregó una segunda muestra de semen que fue nuevamente analizada.
A cada una de las muestras se practicaron, además, los análisis siguientes:
- Índice de vacuolización en el núcleo del espermatozoide.
- Fragmentación del ADN espermático.
El análisis del índice de vacuolización se llevó a cabo mediante un microscopio invertido equipado con lentes Nomarski, que permite un grado de magnificación de ×8000. En cada una de las muestras se analizaron 100 espermatozoides, que se clasificaron en cuatro categorías, teniendo en cuenta el número y el tamaño de las vacuolas que contenía su núcleo:
- Grado I: Forma normal sin vacuolas.
- Grado II: Forma normal y un máximo de 2 vacuolas pequeñas.
- Grado III: Forma normal y al menos una vacuola grande.
- Grado IV: Forma anormal u otras anormalidades.
La fragmentación del ADN espermático se evaluó mediante el kit Halosperm® (Halotech DNA SL, Madrid [España]) siguiendo las instrucciones del fabricante. Se determinó el porcentaje de fragmentación mediante la evaluación de 500 espermatozoides de cada muestra, con microscopía óptica a ×1000. Se considera que el resultado del test de Halosperm tiene un valor predictivo negativo en el resultado de embarazo cuando más del 30% de los espermatozoides en la muestra en fresco presentan fragmentación del ADN.
Como principales indicadores de éxito del tratamiento antioxidante, se consideraron la mejora en el índice de vacuolización y en la fragmentación del ADN espermático.
Las comparaciones entre las muestras de semen pretratamiento y postratamiento se llevaron a cabo mediante el test Wilcoxon para datos pareados, considerándose estadísticamente significativo un valor de p < 0,05. Los datos se analizaron mediante software R v 2.9.0.
Resultados
Se observa un aumento estadísticamente significativo de espermatozoides con grados de vacuolización I y II después de un mes de tratamiento (5,85 ± 2,14; p = 0,01). El grado de fragmentación del ADN espermático también se ve significativamente reducido después del tratamiento (-4,91 ± 2,5; p = 0,03).
En la tabla 1 se muestran las variaciones estadísticamente significativas expresadas como el incremento resultante de comparar las variables estudiadas antes y después de un mes de tratamiento antioxidante.
| Parámetro | Variación Media ± DE | Valor p |
|---|---|---|
| Grados I y II de vacuolización | +5,85 ± 2,14 | 0,01 |
| Fragmentación ADN espermático | -4,91 ± 2,5 | 0,03 |
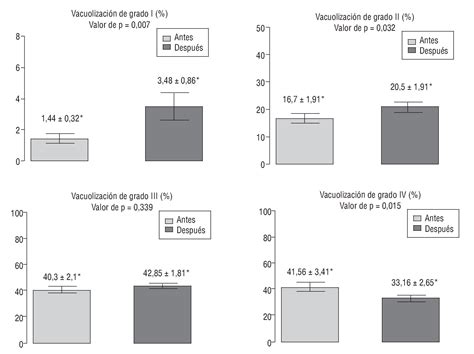
En la figura 2 se ilustran los valores de cada uno de los grados de vacuolización (grados I-IV) expresados como media ± desviación estándar de la media.
En la figura 3 se ilustra la variación del porcentaje de espermatozoides de los grados I y II (considerados los más adecuados para IMSI - microinyección intracitoplásmica de esperma seleccionado morfológicamente) antes y después del tratamiento con antioxidantes.

En la figura 4 se representan los valores del índice de fragmentación del ADN espermático obtenidos antes y después del tratamiento.
Discusión
Hay varias hipótesis acerca del momento en el que se produce el daño oxidativo sobre los espermatozoides. Tesarik et al. indicaron que había un mecanismo postesticular de daño del ADN espermático, pero no excluyeron la posibilidad de una acción directa en el testículo durante el período de desarrollo de las células germinales.
El período de tratamiento escogido para el estudio no es suficiente para afectar un ciclo de espermatogénesis completo, pero cabía esperar una mejora en la homeostasis y el microambiente del epidídimo que afectara directamente a los espermatozoides extratesticulares en período de maduración.
El tratamiento ofrecido a los pacientes contiene diferentes componentes que han sido comúnmente utilizados como tratamiento en varones con baja calidad espermática o infértiles. Se ha demostrado que la carnitina tiene una acción en el metabolismo energético del espermatozoide y como protector del daño oxidativo, y que evita el deterioro de la membrana espermática inducido por los radicales libres de oxígeno. Se ha establecido también la función de la coenzima Q10 como un componente de la cadena respiratoria mitocondrial, la cual desempeña un papel crucial en el metabolismo energético y como antioxidante liposoluble para membranas celulares y lipoproteínas. También se encuentran altos niveles de su forma reducida (ubiquinol) en los espermatozoides, hecho que indica un papel defensivo como antioxidante.
Además, estudios previos han demostrado que el tratamiento con antioxidantes orales, como las vitaminas E y C, dan lugar a una disminución en la fragmentación del ADN espermático.
Las variaciones de estos componentes en el plasma seminal o dentro de la célula se han correlacionado de forma positiva con una mejora en la integridad del ADN espermático. La contribución de estos componentes a la capacidad antioxidante del semen podría explicar el aumento de espermatozoides menos vacuolados en las muestras postratamiento.
Dado que el resultado de las técnicas de reproducción asistida está influido negativamente por la presencia de malformaciones en el núcleo espermático y por la fragmentación del ADN espermático -y coincidiendo con el trabajo publicado por Balmori et al. en esta misma revista-, parece concluyente que el uso de un tratamiento antioxidante puede aumentar el éxito de un ciclo de reproducción asistida.
A pesar de que se trata de un estudio clínico no aleatorizado, los datos obtenidos muestran claramente que el índice de vacuolización y la fragmentación del ADN espermático se reducen notablemente gracias al tratamiento combinado de antioxidantes orales, como la L-carnitina, la coenzima Q10 y las vitaminas C, E y B12.
No obstante, consideramos la necesidad de llevar a cabo estudios prospectivos aleatorizados para concluir si el tratamiento con estos antioxidantes tiene también un efecto positivo en los parámetros seminales básicos y en la consecución de embarazo tras la aplicación de un tratamiento de reproducción asistida.
Evaluación de la Fertilidad Masculina y Factores Relacionados
La fertilidad masculina es un aspecto vital de la salud reproductiva y la andrología, campo de la medicina que se enfoca en la salud del hombre, desempeña un papel esencial en su comprensión y tratamiento. Las pruebas de fertilidad masculina a las que puede someterse un paciente son diversas, siendo la principal el espermograma, que evalúa la calidad del semen. Existen también otros estudios adicionales, como el análisis hormonal, el cariotipo y el FISH de espermatozoides.
La detección de parámetros seminales con valor predictivo en el resultado de las técnicas de reproducción representa uno de los principales objetivos para los profesionales de un laboratorio de andrología. Si estos parámetros están alterados, es fundamental disponer de los recursos necesarios para poder dar solución o intentar disminuir el efecto negativo.
¿Cuándo es recomendable acudir a una clínica de fertilidad?
Enfrentar dificultades para concebir puede ser una experiencia desafiante para muchas parejas. Se recomienda acudir a un especialista después de un año de relaciones sexuales regulares sin protección sin lograr un embarazo. Ciertas condiciones de salud pueden afectar la fertilidad tanto en hombres como en mujeres. En hombres, problemas como el varicocele, infecciones testiculares, antecedentes de enfermedades genéticas o problemas de reproducción en la familia, y hábitos como el consumo de alcohol, tabaco o drogas pueden influir negativamente.
¿Qué pruebas de fertilidad masculina se realizan?
El primer paso para saber si eres estéril es visitar una clínica especializada con tu pareja. Las pruebas básicas para el diagnóstico de la fertilidad masculina incluyen:
- Exploración física: Consiste en el análisis del estado de salud del paciente y sus órganos sexuales, incluyendo registro de peso y altura, exploración del abdomen e ingles, evaluación del pene y la próstata, análisis de los testículos (volumen y consistencia) y ecografía testicular.
- Seminograma (espermograma): Análisis de la calidad del semen. La muestra debe analizarse dentro de la primera hora tras su obtención para evaluar la movilidad de los espermatozoides. Los parámetros analizados incluyen:
- Número de espermatozoides: Cantidad total en el eyaculado.
- Movilidad espermática: Capacidad de movimiento de los espermatozoides.
- Morfología: Forma de los espermatozoides.
- Análisis hormonal: Detección de alteraciones en las hormonas sexuales masculinas.
El análisis macroscópico del semen incluye:
- Volumen (normalmente entre 2 y 4 mL).
- Licuefacción (proceso que ocurre tras reposo de unos 20 minutos).
- Color (gris-amarillento).
- Viscosidad (presencia de hilos).
- pH (normalmente entre 7.2 y 8.0).
El análisis microscópico se realiza para estudiar parámetros como la movilidad espermática (evaluación del movimiento progresivo y rápido), concentración espermática (cantidad por mililitro), morfología, vitalidad (determinación de espermatozoides vivos e inmóviles) y leucocitos (indicativos de posibles infecciones).
Entre las distintas anomalías que pueden diagnosticarse a raíz de un seminograma se encuentran: Teratozoospermia, normozoospermia, oligozoospermia, criptozoospermia, azoospermia, necrozoospermia y astenozoospermia, entre otras.
Otras pruebas de fertilidad masculina
Cuando el seminograma muestra resultados anómalos, se requieren pruebas adicionales para confirmar la causa:
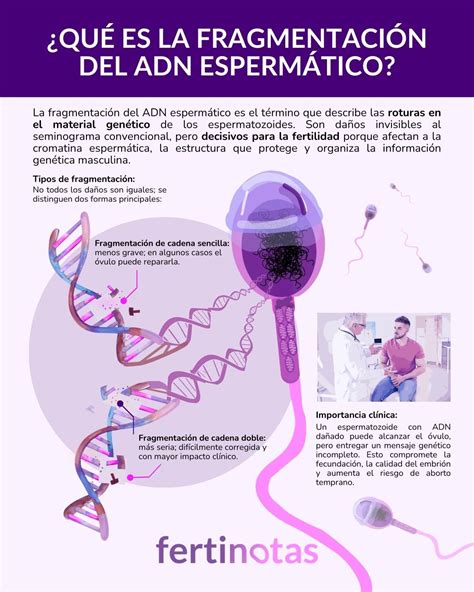
- Estudio de fragmentación del ADN espermático: Un alto grado de fragmentación del ADN espermático puede causar problemas de fecundación y desarrollo embrionario. Hombres con más del 30% de fragmentación espermática suelen necesitar técnicas de reproducción asistida.
- Espermocultivo: Se realiza cuando el seminograma detecta más de 1 millón de leucocitos/ml. Es un estudio bacteriológico para identificar microorganismos presentes en el semen.
- Cariotipo: Esencial en casos de infertilidad para detectar anomalías genéticas o cromosómicas.
- Prueba hiposmótica: Evalúa la integridad de la membrana de los espermatozoides.
- FISH de espermatozoides: Analiza cromosomas específicos en los espermatozoides.
- Biopsia testicular: Se realiza para verificar la producción de espermatozoides en casos de azoospermia.
Composición y Funciones del Semen
El semen masculino es una sustancia compleja y vital para la reproducción. Entender qué contiene el semen es fundamental para comprender la fertilidad masculina y su impacto en la concepción.
- Espermatozoides: Células reproductivas masculinas producidas en los testículos.
- Líquido seminal: Proviene de las vesículas seminales y representa la mayor parte del volumen del semen. Contiene fructosa y prostaglandinas.
- Líquido prostático: Secretado por la próstata, contiene enzimas, zinc y ácido cítrico.
- Moco de las glándulas de Cowper: Lubrica la uretra y neutraliza la acidez residual de la orina.
El semen no solo transporta espermatozoides, sino que también los protege y los nutre, creando un ambiente óptimo para su supervivencia y movimiento hacia el óvulo.
Mejora de la Fertilidad Masculina con Vitaminas y Suplementos
Los suplementos dietéticos se han convertido en una herramienta popular para mejorar la fertilidad masculina:
- Vitamina C: Mejora la calidad del esperma y reduce el daño oxidativo.
- Zinc: Crucial para la producción de testosterona y el mantenimiento de niveles saludables de esperma.
- Coenzima Q10: Puede incrementar la motilidad espermática.
- Ácido fólico: Vital para la espermatogénesis.
- Ácidos grasos omega-3: Apoyan la estructura de las membranas celulares en los espermatozoides.
- Selenio: Actúa como antioxidante, protegiendo las células reproductivas.
- L-carnitina: Mejora la energía y el movimiento espermático.
- Maca: Puede aumentar el volumen de semen, la concentración de esperma y la movilidad.
- Tribulus Terrestris: Puede aumentar el conteo de esperma y mejorar la motilidad.
Androferti® es un suplemento antioxidante formulado para optimizar la calidad del esperma, conteniendo vitamina C, vitamina E, zinc, selenio, L-carnitina y coenzima Q10. Sus beneficios incluyen la mejora del recuento, motilidad y morfología de los espermatozoides, protección contra el daño por radicales libres y aumento de la energía celular espermática.
Alimentación y Hábitos Saludables para la Fertilidad Masculina
Aproximadamente el 15% de las parejas en edad reproductiva enfrentan problemas de infertilidad, y el 30% de estos casos se debe a factores masculinos. Una dieta equilibrada es esencial para la salud general y la fertilidad.
La calidad del semen ha disminuido en los últimos años, influenciada por el estilo de vida y la alimentación. Una dieta mediterránea rica en verduras, frutas, pescado, carne de ave, cereales integrales, legumbres y frutos secos es beneficiosa. Mantener un peso adecuado también es crucial.
Alimentos beneficiosos:
- Nueces (ricas en omega-3, zinc, selenio, vitaminas C y E).
- Semillas de calabaza (ricas en zinc y omega-3).
- Anacardos (contienen zinc y selenio).
- Perejil, pimiento rojo, kiwi y naranjas (altos en vitamina C).
- Aguacate (rico en omega-3).
- Tomate (aporta licopeno).
- Pescado azul (fuente de omega-3).
Alimentos a evitar:
Se recomienda evitar alimentos procesados, comida rápida y grasas saturadas. Es importante moderar el consumo de alcohol, cafeína y eliminar el hábito de fumar.
Hábitos adicionales:
- Ejercicio moderado.
- Evitar el calor excesivo en la zona escrotal.
- Considerar el impacto del entorno laboral y el estrés crónico en la fertilidad.
Estrés Oxidativo y su Impacto en la Fertilidad Masculina
El estrés oxidativo ejerce un papel importante sobre el daño producido en la célula espermática. Es el desequilibrio entre antioxidantes y ROS el causante de alteraciones en el espermatozoide. La técnica del OxiSperm se utiliza para medir el nivel de estrés oxidativo presente en el eyaculado del paciente.
Los ROS, producidos por el metabolismo celular y por factores ambientales o clínicos, pueden dañar el ADN espermático, afectando la integridad de la membrana y disminuyendo la capacidad fecundante del espermatozoide. La LPO (peroxidación lipídica) producida por los ROS es un proceso autopropagable que lleva a una clara disminución de la capacidad fecundante del espermatozoide.
El plasma seminal contiene moléculas y enzimas antioxidantes. Sin embargo, si estos sistemas se encuentran reprimidos o se retira el plasma seminal durante el procesamiento de la muestra, la funcionalidad del espermatozoide puede verse gravemente afectada. Los espermatozoides y otras células están equipadas con sistemas enzimáticos antioxidantes como la superóxidodismutasa (SOD), glutatión peroxidasa (GPX) y catalasa (CAT), además de moléculas antioxidantes naturales.
La técnica del OxiSperm puede ser relevante para analizar correctamente aquellas muestras que presenten un grado de estrés oxidativo moderado/alto, en cuanto a la elección de la técnica y el tiempo que se tarda en procesarla. Se aconseja la utilización de muestra en fresco, ya que la criopreservación espermática puede inducir un incremento en los niveles de estrés oxidativo. Las muestras capacitadas por gradientes de densidad presentan niveles de oxidación más elevados que las capacitadas por Swim-up.
Las terapias y dietas ricas o enriquecidas con antioxidantes parecen prevenir o al menos disminuir el deterioro funcional espermático originado por un exceso de estrés oxidativo. Hay numerosos estudios que avalan el uso de antioxidantes en pacientes con infertilidad masculina, demostrando la mejoría en diferentes parámetros seminales e incluso en la tasa de embarazos.
Los antioxidantes más empleados para el tratamiento de la infertilidad masculina incluyen L-carnitina, coenzima Q10, zinc, selenio, ácido docosahexaenoico (DHA), ácido fólico, acetil-cisteína, aspartato, y vitaminas B, C y E.
Conclusiones y Perspectivas
A pesar de que se trata de un estudio clínico no aleatorizado, parece concluyente la importancia del uso de un tratamiento antioxidante para aumentar el éxito de un ciclo de reproducción asistida, con el objetivo de disminuir la influencia negativa de malformaciones en el núcleo espermático y de la fragmentación del ADN. Los datos obtenidos muestran claramente que el índice de vacuolización y la fragmentación del ADN espermático se reducen notablemente gracias al tratamiento combinado de antioxidantes orales.
No obstante, se considera necesaria la realización de estudios prospectivos aleatorizados para concluir si el tratamiento con estos antioxidantes tiene también un efecto positivo en los parámetros seminales básicos y en la consecución de embarazo tras la aplicación de un tratamiento de reproducción asistida.
tags: #l #carnitina #para #fertilidad